
【题目】元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表,思考扇形元素周期表的填充规律,推出图中标记的11种元素,回答下列问题:
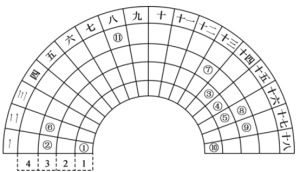
(1)⑤的简单阴离子的结构示意图为_______,的原子序数为___________。
(2)④的简单氢化物的电子式为__________________。
(3)在11种元素中,单质的化学性质最不活泼的是__________(填化学式)。
(4)⑧、⑨两种元素形成的最高价氧化物的水化物中,酸性较强的是_______(填化学式)。
(5)加热时,③的单质能和⑧的最高价氧化物的水化物的浓溶液发生反应,化学方程式为___________。
(6)⑦在元素周期表中的位置是_____________。
【答案】![]() 26
26 ![]() He HC1O4 C+2H2SO4 (浓)
He HC1O4 C+2H2SO4 (浓)![]() CO2↑+2H2 O+2SO2 ↑ 第三周期第III A 族
CO2↑+2H2 O+2SO2 ↑ 第三周期第III A 族
【解析】
①在第一周期第一列,①是H元素;⑩在第一周期第18列,⑩是He元素;②、⑥、⑦、⑧、⑨在第三周期第1、2、13、16、17列,②、⑥、⑦、⑧、⑨分别是Na、Mg、Al、S、Cl元素;③、④、⑤分别在第二周期第14、15、16列,③、④、⑤分别是C、N、O元素;在第四周期第8列,是Fe元素,据此分析解答。
(1)⑤是O元素,形成的简单阴离子是O2-,核外有10个电子,离子结构示意图为![]() ;是Fe元素,Fe的原子序数为26;
;是Fe元素,Fe的原子序数为26;
(2)④是N元素,其气态氢化物是氨气,电子式为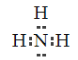 ;
;
(3)在11种元素中,元素He是稀有气体,结构稳定,所以化学性质最不活泼的是He;
(4)⑧⑨分别是S、Cl,同周期元素从左到右非金属性增强,非金属性S<Cl,非金属性越强,最高价氧化物对应水化物的酸性越强,所以两种元素形成的最高价氧化物的水化物中酸性较强的是HClO4;
(5)③的单质是C,⑧是S,硫元素的最高价氧化物的水化物是硫酸,碳与浓硫酸反应生成二氧化碳、二氧化硫、水,反应的化学方程式是C+2H2SO4(浓)![]() CO2↑+2H2O+2SO2↑;
CO2↑+2H2O+2SO2↑;
(6)⑦是Al元素,在元素周期表中的位置是第三周期ⅢA族。


科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.Xe元素的所在族的原子的价电子排布式均为ns2np6,属于非金属元素
B.在元素周期表中,s区,d区和ds区的元素都是金属(氢元素除外)
C.某基态原子的核外电子排布图为![]() ,它违背了泡利原理
,它违背了泡利原理
D.某价电子排布为3d14s2的基态原子,该元素位于周期表中第四周期第ⅢB族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图装置探究铜粉与下列试剂的反应,在试管中加入一定量铜粉,加入试剂后,立即塞上橡胶塞,实验现象如下表所示,下列推断不正确的是( )
资料:Cu2++4NH3![]() [Cu(NH3)4]2+, [Cu(NH3)4]2+呈绛蓝色。
[Cu(NH3)4]2+, [Cu(NH3)4]2+呈绛蓝色。
装置 | 序号 | 试剂 | 现象 |
| ① | 10 mL浓NH3·H2O,3 mLH2O | 溶液变为绛蓝色,左侧水柱上升 |
② | 10 mL浓NH3·H2O,3 mL H2O2 | 溶液变为绛蓝色,且比①深 | |
③ | 10 mL 20% HNO3溶液,3 mL H2O | 溶液快速变蓝,产生无色气体,左侧水柱下降 | |
④ | 10 mL 20% HNO3溶液,3 mL H2O2 | 溶液变蓝比③慢,产生无色气体,左侧水柱下降 |
A.①中实验现象说明O2参与了反应
B.②中溶液颜色比①深可能是由于H2O2氧化Cu生成Cu2+
C.③中左侧水柱下降可能是反应产生NO气体导致的
D.④比③变蓝慢是由于H2O2分解造成自身消耗
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锗是典型的半导体元素,在电子、材料等领域应用广泛。
(1)写出Ge原子结构示意图___。
(2)Ge与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键。从原子结构角度分析,原因是___。
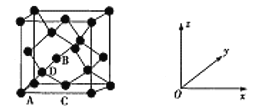
(3)Ge单晶具有金刚石型的结构,如图为晶胞结构,其中原子坐标参数A为(0,0,0),B为(![]() ,0,
,0,![]() ),C为(
),C为(![]() ,
,![]() ,0),D原子的坐标参数为___;若晶胞参数为anm,NA表示阿伏伽德罗常数,则其晶胞密度为___g/cm3(列出计算式即可)。
,0),D原子的坐标参数为___;若晶胞参数为anm,NA表示阿伏伽德罗常数,则其晶胞密度为___g/cm3(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中发生下列反应:I2(g)+H2(g)![]() 2HI(g)(正反应为放热反应)。起始时,n(H2)=a mol,n(I2)=b mol。只改变表中列出的条件,其他条件不变,试将化学反应速率的改变填入相关的表格中(填“增大”“减小”或“不变”)。
2HI(g)(正反应为放热反应)。起始时,n(H2)=a mol,n(I2)=b mol。只改变表中列出的条件,其他条件不变,试将化学反应速率的改变填入相关的表格中(填“增大”“减小”或“不变”)。
编号 | 改变的条件 | 反应速率 |
(1) | 升高温度 | ______ |
(2) | 加入正催化剂 | ______ |
(3) | 再充入a mol H2 | ______ |
(4) | 将容器的容积扩大到原来的2倍 | ______ |
(5) | 保持容积不变,通入b mol Ne | ______ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香兰素是重要的香料之一,它可由丁香酚经多步反应合成。
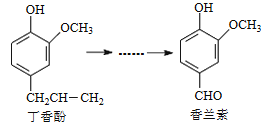
有关上述两种化合物的说法错误的是
A.丁香酚与香兰素都能与H2发生加成反应
B.常温下,1 mol丁香酚最多消耗1 mol Br2
C.丁香酚和香兰素遇FeCl3溶液都能发生显色反应
D.常温下,丁香酚与香兰素都能与浓溴水发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲同学设计并进行了如下实验,以探究乙炔与溴的加成反应:先取一定量工业用电石与水反应,将生成的气体通入足量的溴水中,发现溶液褪色,即证明乙炔与溴水发生了加成反应。乙同学发现在甲同学的实验中,褪色的溶液里有少许黄色浑浊,推测在制得乙炔中还可能含有少量还原性的杂质气体,由此他提出必须先除去之,再与溴水反应。请你回答下列问题:
(1)写出甲同学实验中的两个化学方程式:_______________、____________。
(2)乙认为甲设计的实验不能验证此反应为加成反应,其理由是________________。
A.使溴水褪色的物质,就是乙炔
B.使溴水褪色的反应就是加成反应
C.使溴水褪色的物质,未必是乙炔
D.使溴水褪色的反应未必是加成反应
(3)乙同学推测此乙炔中必定含有的一种杂质气体是_________,在验证过程中必须全部除去,它与溴水反应的化学方程式是________________________________________________________。
(4)请你选用下列三个装置(见下图)(可重复使用)来实现乙同学的实验方案,将它们的编号填入方框,并写出装置内所放的化学药品。
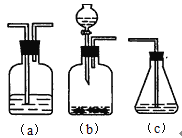
![]()
___、___、___、___
(5)为验证这一反应是加成而不是取代,丙同学提出可用pH试纸来测试反应后溶液的酸性,理由是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用0.10mol/L的氢氧化钠溶液滴定10.00mL0.10mol/L醋酸溶液,水的电离度随氢氧化钠溶液体积的变化曲线如图所示,下列说法正确的是( )

A.该滴定过程应该选择甲基橙作为指示剂
B.N点溶液中c(OH-)=c(CH3COO-)+c(CH3COOH)+c(H+)
C.从P点到N点,溶液中水的电离程度逐渐增大
D.M点对应的NaOH溶液的体积为10.00mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室从含碘废液![]() 除
除![]() 外,含有
外,含有![]() 、
、![]() 、
、![]() 等
等![]() 中回收碘,其实验过程如图1:
中回收碘,其实验过程如图1:
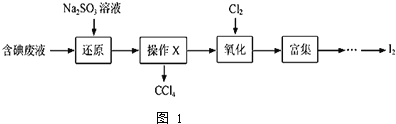
![]() 向含碘废液中加入稍过量的
向含碘废液中加入稍过量的![]() 溶液,将废液中的
溶液,将废液中的![]() 还原为
还原为![]() ,其离子方程式为 ______ ;该操作将
,其离子方程式为 ______ ;该操作将![]() 还原为
还原为![]() 的目的是 ______ .
的目的是 ______ .
![]() 操作X的名称为 ______ .
操作X的名称为 ______ .
![]() 氧化时,在三颈瓶中将含
氧化时,在三颈瓶中将含![]() 的水溶液用盐酸调至pH约为2,缓慢通入
的水溶液用盐酸调至pH约为2,缓慢通入![]() ,在
,在![]() 左右反应
左右反应![]() 实验装置如图2所示
实验装置如图2所示![]() 实验控制在较低温度下进行的原因是 ______ ;锥形瓶里盛放的溶液为 ______ .
实验控制在较低温度下进行的原因是 ______ ;锥形瓶里盛放的溶液为 ______ .
![]() 利用如图3所示装置
利用如图3所示装置![]() 电极均为惰性电极
电极均为惰性电极![]() 也可吸收
也可吸收![]() ,并用阴极排出的溶液吸收
,并用阴极排出的溶液吸收![]() .
.
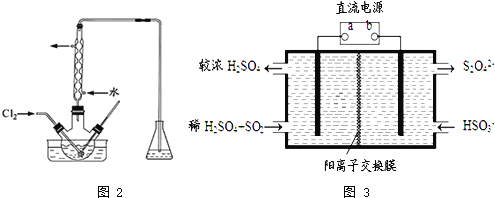
![]() 为电源的 ______
为电源的 ______ ![]() 填“正极”或“负极”
填“正极”或“负极”![]() ,阳极的电极反应式为 ______ .
,阳极的电极反应式为 ______ .
![]() 在碱性条件下,用阴极排出的溶液吸收
在碱性条件下,用阴极排出的溶液吸收![]() ,使其转化为无害气体,同时有
,使其转化为无害气体,同时有![]() 生成.该反应中氧化剂与还原剂的物质的量之比为 ______ .
生成.该反应中氧化剂与还原剂的物质的量之比为 ______ .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com