
【题目】下图为有机物之间的转化关系。
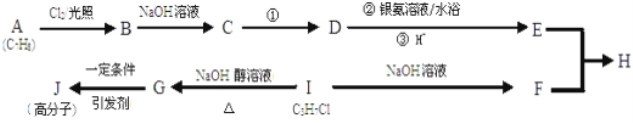
已知:E属于芳香族化合物;F的核磁共振氢谱为三组峰,且面积比为6:1:1。
请回答下列问题:
(1)B的结构简式为__________。F的名称为__________,
(2)C中官能团的名称为__________,G→J的反应类型__________,发生反应①的条件是_______________。
(3)反应B→C的化学方程式为__________。
(4)E的一种同系物X比E的相对分子质量大14;X同分异构体有很多种。
①若X的同分异构体为芳香族化合物,它与E具有相同的官能团,则符合此条件的X的同分异构体有__________种。
②若X的同分异构体能与新制氢氧化铜悬浊液反应,生成砖红色沉淀,也能使FeCl3溶液显紫色,且苯环上的一元取代物有两种,则X的这种同分异构体的结构简式为__________。
【答案】 ![]() 2—丙醇 羟基 加聚反应 O2 Cu/Ag 加热
2—丙醇 羟基 加聚反应 O2 Cu/Ag 加热 ![]() +NaOH
+NaOH![]()
![]() +NaCl 4
+NaCl 4 ![]()
【解析】根据已知信息①结合A→B→C→D→E的反应条件可知,A为甲苯,B为![]() ,C为苯甲醇,D为苯甲醛,E为苯甲酸;根据已知信息②结合I→F,I→G的反应条件可知,I为CH3CHClCH3,F为CH3CHOHCH3,G为CH2=CHCH3。(1)B的结构简式为
,C为苯甲醇,D为苯甲醛,E为苯甲酸;根据已知信息②结合I→F,I→G的反应条件可知,I为CH3CHClCH3,F为CH3CHOHCH3,G为CH2=CHCH3。(1)B的结构简式为![]() ;F为CH3CHOHCH3,名称为2—丙醇;(2)C为苯甲醇,官能团的名称为羟基,G→J是CH2=CHCH3发生加聚反应生成聚丙烯,反应类型为加聚反应,反应①苯甲醇催化氧化生成苯甲醛,发生反应①的条件是O2 Cu/Ag 加热;(3)反应B→C是
;F为CH3CHOHCH3,名称为2—丙醇;(2)C为苯甲醇,官能团的名称为羟基,G→J是CH2=CHCH3发生加聚反应生成聚丙烯,反应类型为加聚反应,反应①苯甲醇催化氧化生成苯甲醛,发生反应①的条件是O2 Cu/Ag 加热;(3)反应B→C是![]() 在氢氧化钠的水溶液中发生水解反应生成苯甲醇,反应的化学方程式为
在氢氧化钠的水溶液中发生水解反应生成苯甲醇,反应的化学方程式为![]() +NaOH
+NaOH![]()
![]() +NaCl;(4)E(苯甲酸)的一种同系物X比E的相对分子质量大14,则多一个CH2,X同分异构体有很多种。①若X的同分异构体为芳香族化合物,它与E具有相同的官能团(羧基),则符合此条件的X的同分异构体有苯乙酸、邻甲基苯甲酸、对甲基苯甲酸、间甲基苯甲酸4种;②若X的同分异构体能与新制氢氧化铜悬浊液反应,生成砖红色沉淀则含有醛基,也能使FeCl3溶液显紫色则含有酚羟基,只有两个氧,则不可能是甲酸酯类,且苯环上的一元取代物有两种则两个取代基在对位,则X的这种同分异构体的结构简式为
+NaCl;(4)E(苯甲酸)的一种同系物X比E的相对分子质量大14,则多一个CH2,X同分异构体有很多种。①若X的同分异构体为芳香族化合物,它与E具有相同的官能团(羧基),则符合此条件的X的同分异构体有苯乙酸、邻甲基苯甲酸、对甲基苯甲酸、间甲基苯甲酸4种;②若X的同分异构体能与新制氢氧化铜悬浊液反应,生成砖红色沉淀则含有醛基,也能使FeCl3溶液显紫色则含有酚羟基,只有两个氧,则不可能是甲酸酯类,且苯环上的一元取代物有两种则两个取代基在对位,则X的这种同分异构体的结构简式为![]() 。
。


 每课必练系列答案
每课必练系列答案科目:高中化学 来源: 题型:
【题目】
(1)氯化铁溶液用于检验食用香精乙酰乙酯时,会生成紫色配合物,其配离子结构如图所示。
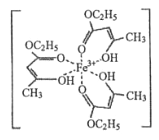
①此配合物中,基态铁离子的价电子排布式为________________。
②此配合物中碳原子的杂化轨道类型有________________。
③此配离子中含有的化学键有____________(填字母)。
A. 离子键 B. 金属键 C. 极性键 D. 非极性键 E. 配位键 F. 氢键 G.σ键 H. π键
④氯化铁在常温下是固体,熔点为 306℃,沸点为 315℃,在 300℃以上升华,易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断氯化铁的晶体类型为________________。
(2)基态 A 原子的价电子排布式为 3s23p5,铜与A 形成化合物的晶胞如图所示(黑球代表铜原子)。
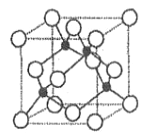
①该化合物的化学式为________________,A原子的配位数是______________。
②该化合物难溶于水,但易溶于氨水,其原因可能是________________;与NH3 互为等电子体的分子有________________(写化学式,一种即可)。 NH3 的键角大于H2O的键角的主要原因是_______________________。
③已知该化合物晶体的密度为ρg·cm-3,阿伏加德罗常数的值为 NA,则该晶体中 Cu 原子和A 原子之间的最短距离为________________pm(列出计算表达式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固体A在一定温度下分解生成气体B、C、D反应为:2A![]() B+2C+3D,若测得生成气体的质量是相同体积的H2的15倍,则固体A的摩尔质量是( )
B+2C+3D,若测得生成气体的质量是相同体积的H2的15倍,则固体A的摩尔质量是( )
A. 30 g/mol B. 60 g/mol
C. 90 g/mol D. 120 g/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】麦考酚酸是一种有效的免疫抑制剂,能有效地防止肾移植排斥,其结构简式如下图所示。下列有关麦考酚酸说法正确的是( )

A. 分子式为C17H23O6
B. 不能与FeCl3溶液发生显色反应
C. 在一定条件下可发生加成、取代、消去反应
D. 1 mol麦考酚酸最多能与3 mol NaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种低成本的储能电池,电池结构如下图所示,电池工作原理为:Fe3++Cr2+ ![]() Fe2++Cr3+。下列说法正确的是( )
Fe2++Cr3+。下列说法正确的是( )
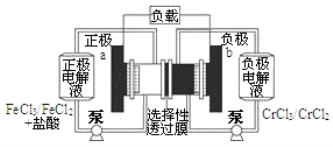
A. 电池放电时,Cl﹣从b极穿过选择性透过膜移向a极
B. 电池放电时,b极的电极反应式为Cr3++e﹣=Cr2+
C. 电池充电时,a极的电极反应式为Fe2+-e﹣=Fe3+
D. 电池充电时,电路中每通过0.1mol电子,Fe2+浓度降低0.1molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有中学化学常见的物质A、B、C、D、E、F、G、H,满足如下图所示转化关系。其中A、F为气体单质,A呈黄绿色,C为淡黄色固体化合物。B为生活中常见的液体化合物。回答下列问题:

(1)写出下列物质的化学式:C________,H______________。
(2)出下列化学反应方程式:
①______________________________________。
③______________________________________。
(3)写出D的一种用途__________________________。但由于D易于发生③反应而不易于保存,故生产生活中往往用A与石灰乳反应生成易于保存运输的固体,其在潮湿空气中可以反应生成D,请写出这两个反应方程式_________________,_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com