
����Ŀ��һ�ֵͳɱ��Ĵ��ܵ�أ���ؽṹ����ͼ��ʾ����ع���ԭ��Ϊ��Fe3++Cr2+ ![]() Fe2++Cr3+������˵����ȷ���ǣ� ��
Fe2++Cr3+������˵����ȷ���ǣ� ��
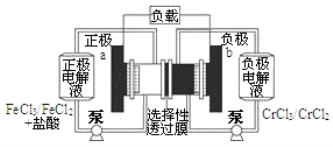
A. ��طŵ�ʱ��Cl����b������ѡ������Ĥ����a��
B. ��طŵ�ʱ��b���ĵ缫��ӦʽΪCr3++e��=Cr2+
C. ��س��ʱ��a���ĵ缫��ӦʽΪFe2+-e��=Fe3+
D. ��س��ʱ����·��ÿͨ��0.1mol���ӣ�Fe2+Ũ�Ƚ���0.1molL��1
���𰸡�C
��������A����طŵ�ʱ��Cl���������Ҵ���ѡ������Ĥ�����ң�����a��b�� ѡ��A����B���ŵ�ʱ��bΪ����������ʧ���ӵ�������Ӧ���缫��ӦʽΪCr2+-e��= Cr3+�� ѡ��B����C����س��ʱ��a����������ʧ���ӵ�������Ӧ���缫��ӦʽΪFe2+��e��=Fe3+��ѡ��C��ȷ��D����·��ÿ����0.1mol���ӣ��ͻ���0.1mol����������ʧ���ӣ���СŨ�Ⱥ�����йأ�ѡ��D����ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ܱ������з�����Ӧ��N2(g)��3H2(g)![]() 2NH3(g)'��H����92.4 kJ��mol��1��NH3��ƽ�������е��������(��)���¶�(T)��ѹǿ(p)�Ĺ�ϵ��ͼ��ʾ�������ж���ȷ����(����)
2NH3(g)'��H����92.4 kJ��mol��1��NH3��ƽ�������е��������(��)���¶�(T)��ѹǿ(p)�Ĺ�ϵ��ͼ��ʾ�������ж���ȷ����(����)
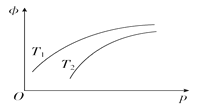
A. T1����T2
B. �����¶ȣ��÷�Ӧ�Ļ�ѧƽ�ⳣ������
C. ��n(N2)��n(H2)��n(NH3)��1��3��2ʱ����Ӧһ���ﵽƽ��״̬
D. �����������䣬��С�������ѹǿ������ߵ�λʱ����NH3�IJ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ʾ�����İ����������ڳ����¿ɺϳ�����ɰ(��Ҫ�ɷ�ΪNH4Cl)��ijʵ��С��Ը÷�Ӧ����̽������������ɰ����Ԫ�زⶨ���ش��������⣺
(1)����ɰ���Ʊ�
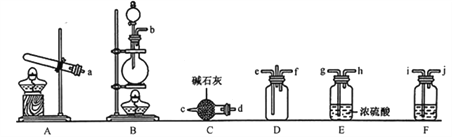
������װ��A��ȡʵ������İ�����д����Ӧ�Ļ�ѧ����ʽ��_______________________��
�ڸ�ʵ������Ũ������MnO2��Ӧ��ȡ������������װ�DF�е��Լ���_______________(��д�Լ�����)��
��Ϊ��ʹ������������D�г�ֻ�ϣ���ȷ������װ�õĺ�������˳��________��-ef��_________(��Сд��ĸ�ͼ�ͷ��ʾ����ͷ��������������һ��)��
��֤��������������Ӧ������ɰ���ɣ���Ҫ�ļ����Լ��У���������ˮ��ϡHNO3��NaOH��Һ�⣬����Ҫ___________��
(2)����ɰ��Ԫ�صIJⶨ��ȷ��ȡa g����ɰ��������������ͭ��ϼ���(�����ķ�ӦΪ��2NH4Cl+3CuO![]() 3Cu+N2��+2HCl��+3H2O)����������װ�òⶨ����ɰ�е�Ԫ������Ԫ�ص�����֮�ȡ�
3Cu+N2��+2HCl��+3H2O)����������װ�òⶨ����ɰ�е�Ԫ������Ԫ�ص�����֮�ȡ�
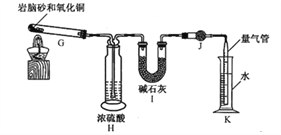
������װ��H��Ŀ����_____________��
����װ�â�����b g������װ��K����������ΪV L(��֪���³�ѹ������Ħ�����Ϊ24.5 L��mol-1)��������ɰ��m(N)��m(Cl)=_____________(�ú�b��V�Ĵ���ʽ��ʾ�����ػ���)��
���������ʱ�����¶ȸ��ڳ���(������������ȷ)����m(N)������ֵ_____________(�ƫ�ߡ���ƫ�͡�����Ӱ�족)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪ�л���֮���ת����ϵ��
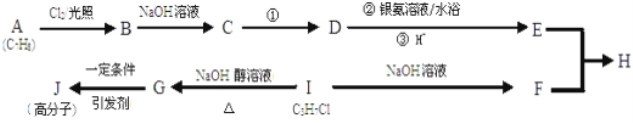
��֪��E���ڷ����廯������F�ĺ˴Ź�������Ϊ����壬�������Ϊ6��1��1��
��ش���������:
��1��B�Ľṹ��ʽΪ__________��F������Ϊ__________��
��2��C�й����ŵ�����Ϊ__________��G��J�ķ�Ӧ����__________��������Ӧ����������_______________��
��3����ӦB��C�Ļ�ѧ����ʽΪ__________��
��4��E��һ��ͬϵ��X��E����Է���������14��Xͬ���칹���кܶ��֡�
����X��ͬ���칹��Ϊ�����廯�������E������ͬ�Ĺ����ţ�����ϴ�������X��ͬ���칹����__________�֡�
����X��ͬ���칹����������������ͭ����Һ��Ӧ������ש��ɫ������Ҳ��ʹFeCl3��Һ����ɫ���ұ����ϵ�һԪȡ���������֣���X������ͬ���칹��Ľṹ��ʽΪ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)����ʹ�����ʴ�ˮ��Һ���������ֲ��ı�������Ҫ���ʣ�Ӧ����________(����ĸ)��
a. �������֡� b. ������������Һ�� c. ����ͭ��Һ
�ڼ��𱽺ͼױ��ķ������Լ���________(����ĸ)��
a. Ũ��ˮ �� b. �ữ��KMnO4��Һ �� c. �ڿ����е�ȼ
�����л������У����³�ѹ��Һ̬����________(����ĸ)��
a. �״� �� b. ��Ȳ �� c. ��ϩ
(2)�Ʊ�������������Ҫ�����������ʣ�

�� ���в�����ԭ�ӵĹ�������________(������)��
�� ����ͨ������ת�����Եõ���(����A��D��Ϊ�л���)��

A�Ļ�ѧʽ��________��C��D�ķ�Ӧ������________��
�� �������Ӿ۷�Ӧ��������Ϊ________________________(д�ṹ��ʽ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������Al2��SO4����ȡAl��OH��3 �� ����ʵ��Լ��ǣ� ��
A.NaOH
B.H2SO4
C.NH3H2O
D.KOH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��3d �ܼ������ֻ���Ų� 10 ���������ݵ�ԭ����
A.����������ԭ��
B.���ع���
C.�������ԭ��ͺ��ع���
D.�������ԭ�������������ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2HCHO+NaOH(Ũ)��HCOONa+CH3OH�У�HCHO
A.��������B.������ԭC.�ȱ��������ֱ���ԭD.δ��������δ����ԭ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£����ݻ��ɱ���ܱ�������ͨ��N2��H2,������Ӧ:N2(g)+3H2(g) ![]() 2NH3(g)��H<0�ﵽƽ����Իش���������:
2NH3(g)��H<0�ﵽƽ����Իش���������:
��1���������£���Ӧ��ƽ�ⳣ������ʽK=______;�������¶ȣ�Kֵ��______(����������������С������������)��
��2���ﵽƽ����������������䣬�����������Сһ��,ƽ�⽫____(�������淴Ӧ����������������Ӧ��������������)�ƶ���ƽ�ⳣ��K��_____ (����������������С������������)��
��3���ﵽƽ���,�ں�ѹ�����£���������ͨ�˺���(He),������ת���ʽ�___������������������С������������)��
��4����������ͬ�������и�����1molN2��3molH2,�ڲ�ͬ�����·ֱ�ﵽƽ�⣬���������������ʱ��仯��ͼ��ʾ������˵����ȷ����_______ (�����)��
a.ͼI�����Dz�ͬѹǿ�Է�Ӧ��Ӱ�죬��P2>P1
b.ͼ��������ͬ��ͬѹ�´����Է�Ӧ��Ӱ�죬�Ҵ�����1>2
c.ͼ�������Dz�ͬ�¶ȶԷ�Ӧ��Ӱ�죬��T1>T2
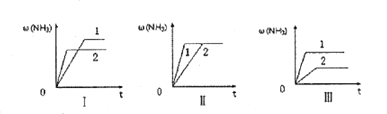
��5��A��B�����ݻ���ͬ�������и�����1molN2��3molH2,A�������ֺ��º��ݴﵽƽ��ʱ���������ʵ���Ϊx,B�������ֺ��º�ѹ�ﵽƽ��ʱ���������ʵ���Ϊy,��x____y(��>����<������=��)��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com