
| A. | 用锌和稀硫酸反应制取氢气 | B. | 用氢气高温还原氧化铜得到单质铜 | ||
| C. | 用碳和高温水蒸气反应制取氢气 | D. | 用氯气和溴化钠溶液反应制取溴 |
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | m-13=n | B. | n+5=m | C. | m+8=n | D. | n-11=m |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数:Z>Y>X>W | |
| B. | X、Y、Z、W 形成的单质最多有 6 种 | |
| C. | X 元素最高价氧化物对应水化物的化学式为:H3XO4 | |
| D. | 四种元素的气态氢化物中,W 的气态氢化物最稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 18g 冰(图甲)中含 O-H 键数目为 4NA | |
| B. | 28g 晶体硅(图乙)中含有σ键数目为 2NA | |
| C. | 44g 干冰(图丙)中含有 NA个晶胞结构单元 | |
| D. | 石墨烯(图丁)是碳原子单层片状新材料,12g 石墨烯中含π键数目为 1.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.21mol | B. | 0.14mol | C. | 0.16mol | D. | 0.24mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在相同温度下,pH=1且体积为1L的硫酸溶液所含的H+数与pH=13且体积为1L的氢氧化钠溶液所含的OH-数一定均为0.1NA | |
| B. | 7.8gNa2S和Na2O2的混合物中所含离子数为0.3NA | |
| C. | 在反应KClO4+8HCl=KCl+4Cl2↑+4H2O中,每生成4molCl2,转移的电子数为8NA | |
| D. | 在标准状况下,2.24LHF中含有的电子数为NA |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西省高二上月考一化学卷(解析版)) 题型:选择题
某温度下,已知反应mX(g)+nY(g) 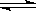 qZ(g)△H>0,m+n>q,在体积一定的密闭容器中达到平衡,下列叙述正确的是
qZ(g)△H>0,m+n>q,在体积一定的密闭容器中达到平衡,下列叙述正确的是
A.反应速率v正(X)=m/n v逆(Y)
B.降低温度,c(Y)/c(Z)的值变小
C.增加Y的物质的量,X的转化率增大
D.加入X,反应的△H增大
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
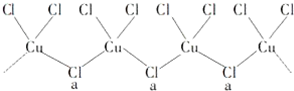
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com