
【题目】氧化镁在易燃材料中常被用作阻燃剂,碳酸镁高温分解法是工业上制备轻质氧化镁的常用方法。镁硅矿主要成分为Mg3(Si2O5)(OH)4和还有少量的Fe2O3、Al2O3等。以镁硅矿为原料制备碳酸镁晶体(MgCO3nH2O)的生产流程如下:
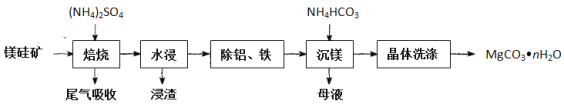
已知“焙烧”过程中的主要反应为:Mg3(Si2O5)(OH)4+5(NH4)2SO4![]() 3MgSO4+10NH3↑+2SiO2+7H2O↑+2SO3↑
3MgSO4+10NH3↑+2SiO2+7H2O↑+2SO3↑
(1)Mg3(Si2O5)(OH)4用氧化物的形式表示为___,焙烧产物NH3的电子式为__。
(2)为提高水浸速率,可采取的措施为__(任写一种)。“浸渣”的主要成分为__。
(3)“除铝、铁”时,需将溶液pH调至8.0左右,适宜作调节剂的是__(填字母代号)。
a.Ca(OH)2 b.Mg(OH)2 c.NH3H2O
(4)“沉镁”过程中反应的离子方程式为__。“沉镁”时若温度超过60℃,将会产生较多的碱式碳酸镁杂质,原因是___。
(5)流程中可以循环利用的物质是___(填化学式)。
(6)为测定产品MgCO3nH2O中的n值,称取15.6g产品进行充分加热至恒重,冷却,称得固体质量为4g,则n=__。
【答案】3MgO2SiO22H2O ![]() 将焙烧渣粉碎、加热或搅拌 SiO2 bc Mg2++2HCO3-+(n-1)H2O=MgCO3·nH2O↓+CO2↑ 升温促进Mg2+水解 (NH4)2SO4 3
将焙烧渣粉碎、加热或搅拌 SiO2 bc Mg2++2HCO3-+(n-1)H2O=MgCO3·nH2O↓+CO2↑ 升温促进Mg2+水解 (NH4)2SO4 3
【解析】
以石棉尾矿(主要含有Mg3(Si2O5)(OH)4和少量的Fe2O3、Al2O3)为原料制备碳酸镁晶体(MgCO3nH2O)的工艺流程:加入硫酸铵焙烧得到MgSO4、SiO2、Fe2O3、Al2O3,水浸,形成Mg2+、Fe3+、Al3+的溶液,SiO2不溶于水形成浸渣,加入Mg(OH)2或NH3H2O将pH调至8.0左右,将Fe3+、Al3+以氢氧化物的形式过滤除去,向含有镁离子的滤液中加入碳酸氢铵发生反应:Mg2++2HCO3-+(n-1)H2O=MgCO3nH2O↓+CO2↑,洗涤晶体可得,据此分析解答。
(1)化学式改写成相应的氧化物的形式,按照活泼金属氧化物、较活泼金属氧化物、SiO2、H2O的顺序来书写,Mg3(Si2O5)(OH)4用氧化物的形式表示为:3MgO2SiO22H2O;氨气为共价化合物,其电子式为:![]() ;故答案为:3MgO2SiO22H2O;
;故答案为:3MgO2SiO22H2O;![]() ;
;
(2)为提高水浸速率,可采取的措施有:将焙烧渣粉碎、加热或搅拌等;石棉尾矿加入硫酸铵焙烧得到MgSO4、SiO2、Fe2O3、Al2O3,水浸,SiO2不溶于水形成浸渣;故答案为:将焙烧渣粉碎、加热或搅拌;SiO2;
(3)“除铁、铝”时,需将pH调至8.0左右,选择不引入新杂质的试剂,故可选用Mg(OH)2或NH3H2O;故答案为:bc;
(4)“沉镁”过程中反应的离子方程式为:Mg2++2HCO3-+(n-1)H2O=MgCO3nH2O↓+CO2↑;升温促进Mg2+水解生成Mg(OH)2,Mg(OH)2与CO2反应生成碱式碳酸镁,故答案为:Mg2++2HCO3-+(n-1)H2O=MgCO3·nH2O↓+CO2↑;升温促进Mg2+水解;
(5)沉镁过程的滤液为(NH4)2SO4,可循环使用;故答案为:(NH4)2SO4;
(6)称取13.8gMgCO3nH2O进行受热分解,MgCO2nH2O受热分解生成MgO、CO2、H2O,最终剩余的固体为MgO4.0g,n(Mg)=![]() =0.1mol,则n(MgCO3)=n(Mg)=0.1mol,m(MgCO3)=8.4g,m(H2O)=13.8g-8.4g=5.4g,n(H2O)=
=0.1mol,则n(MgCO3)=n(Mg)=0.1mol,m(MgCO3)=8.4g,m(H2O)=13.8g-8.4g=5.4g,n(H2O)=![]() =0.3mol,1:n=n(MgCO3):n(H2O)=0.1:0.3,故n=3。
=0.3mol,1:n=n(MgCO3):n(H2O)=0.1:0.3,故n=3。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】染料化工企业产生的废水中含有高浓度的氨氮(氨和铵盐)成分,直接排放会造成环境污染。实验小组探索下列方法对氨氮废水进行处理。

(1)实验室检测上述废水中是否含有氨氮的方法是___。
(2)“吹脱”步骤中,在废水池的底部吹入大量热气泡,其目的是___。
(3)“氧化”步骤中加入了微生物,NH3被氧化为N2。反应的化学方程式为___。
(4)“沉淀"步骤中将剩余的NH3·H2O转化为NH4MgPO46H2O沉淀,发生反应的离子方程式为___。NH4MgPO46H2O在农业生产中具有重要应用价值,其原因是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可用一氧化碳合成可再生能源甲醇。
(1)已知:Ⅰ.3CO(g)+6H2(g)![]() CH3CH=CH2(g)+3H2O(g) △H1=-301.3kJ/mol;
CH3CH=CH2(g)+3H2O(g) △H1=-301.3kJ/mol;
Ⅱ.3CH3OH(g)![]() CH3CH=CH2(g)+3H2O(g) △H2=-31.0kJ/mol。
CH3CH=CH2(g)+3H2O(g) △H2=-31.0kJ/mol。
则CO与H2合成气态甲醇的热化学方程式为___________________________________
(2)某科研小组在Cu2O/ZnO作催化剂的条件下,在500℃时,研究了n(H2):n(CO)分别为2:1、5:2时CO的转化率变化情况(如图1所示),则图中表示n(H2):n(CO)=2:1的变化曲线为___________(填“曲线a”或“曲线b”),原因是_______________________________。
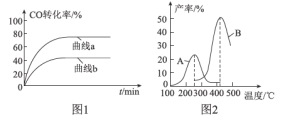
(3)某科研小组向密闭容器中充入一定量的CO和H2合成气态甲醇,分别在A、B两种不同催化剂作用下发生反应,一段时间后测得CH3OH的产率与温度的关系如图2所示。下列说法正确的是____________(填选项字母)。
a.使用催化剂A能加快相关化学反应速率,但催化剂A并未参与反应
b.在恒温恒压的平衡体系中充入氩气,CH3OH的产率降低
c.当2v(CO)正=v(H2)逆时,反应达到平衡状态
(4)一定温度下,在容积均为2L的两个恒容密闭容器中,按如下方式加入反应物,一段时间后达到平衡。

若甲容器平衡后气体的压强为开始时的![]() ,则该温度下,该反应的平衡常数K=______,要使平衡后乙容器与甲容器中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则乙容器中c的取值范围为_____________________________________。
,则该温度下,该反应的平衡常数K=______,要使平衡后乙容器与甲容器中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则乙容器中c的取值范围为_____________________________________。
(5)CO与日常生产生活相关。
①检测汽车尾气中CO含量,可用CO分析仪,工作原理类似于燃料电池,其中电解质是氧化钇(Y2O3)和氧化锆(ZrO2)晶体,能传导O2-。则负极的电极反应式为__________________。
②碳酸二甲醋[(CH3O)2CO]毒性小,是一种绿色化工产品,用CO合成(CH3O)2CO,其电化学合成原理为4CH3OH+2CO+O2![]() 2(CH3O)2CO+2H2O,装置如图3所示:
2(CH3O)2CO+2H2O,装置如图3所示:
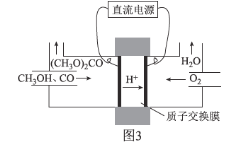
写出阳极的电极反应式:________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂废金属屑中主要成分为Cu、Fe和Al(含有少量Al2O3和Fe2O3),某化学兴趣小组设计了如下实验流程,用该工厂的合金废料制取氯化铝、绿矾晶体(FeSO4·7H2O)和胆矾晶体。
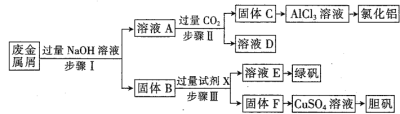
请回答:
(1)胆矾的化学式为___________________。
(2)溶液E为绿色溶液,则试剂X是______________。
(3)步骤I,首先加入温热NaOH溶液,作用是_________;-段时间后,再分批加入常温NaOH溶液,原因是___________。
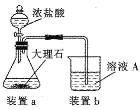
(4)在步骤II时,用如图装置制取CO2并通入溶液A中。-段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体C减少,可在a和b间加-个盛有饱和_________溶液的洗气瓶。
(5)保存FeSO4溶液时,需要滴加少量硫酸溶液,再加入适量_______(填化学式),防止变质。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、Q、R均为前四周期元素,且原子序数依次增大。其相关信息如下表所示:
X元素的基态原子中电子分布在三个不同的能级中,且每个能级中的电子总数相同 |
Y元素的气态氢化物与其最高价氧化物对应的水化物能发生化合反应 |
Z元素的族序数是其周期数的三倍 |
W原子的第一至第六电离能分别为:I1=578KJ·mol-1I2=1817KJ·mol-1I3=2745KJ·mol-1 I4=11575KJ·mol-1I5=14830KJ·mol-1I6=18376KJ·mol-1 |
Q为前四周期中电负性最小的元素 |
元素R位于周期表的第10列 |
回答下列问题:
(1)Y元素的基态原子中未成对电子数为______;X、Y、Z三种元素原子的第一电离能由小到大的顺序为____________(用元素符号表示)。
(2)W的氯化物的熔点比Q的氯化物的熔点__________(填“高”或“低”),理由是__________________________________________________。
(3)光谱证实元素W的单质与强碱性溶液反应有[W(OH)4]-生成,则[W(OH)4]-中存在(填字母)_____________。
a.极性共价键 b.非极性共价键 c.配位键 d.氢键
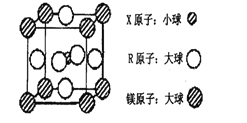
(4)含有X、R和镁三种元素的某种晶体具有超导性,其结构如下图所示。则该晶体的化学式为_______;晶体中每个镁原子周围距离最近的R原子有_______个。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人工肾脏可用电化学方法除去代谢产物中的尿素[CO(NH2)2],原理如图,下列有关说法不正确的是( )
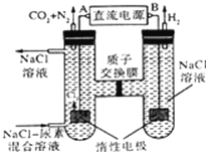
A.B为电源的正极
B.电解结束后,阴极室溶液的pH与电解前相比将升高
C.电子移动的方向是B→右侧惰性电极,左侧惰性电极→A
D.阳极室中发生的反应依次为2Cl﹣﹣2e﹣=Cl2↑、CO(NH2)2+3Cl2+H2O═N2+CO2+6HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着时代的发展,绿色环保理念越来越受到大家的认同,变废为宝是我们每一位公民应该养成的意识。某同学尝试用废旧的铝制易拉罐作为原材料、采用“氢氧化铝法”制取明矾晶体并进行一系列的性质探究。
制取明矾晶体主要涉及到以下四个步骤:
第一步:铝制品的溶解。取一定量铝制品,置于250mL锥形瓶中,加入一定浓度和体积的强碱溶液,水浴加热(约93℃),待反应完全后(不再有氢气生成),趁热减压抽滤,收集滤液于250mL烧杯中;
第二步:氢氧化铝沉淀的生成。将滤液重新置于水浴锅中,用3 mol/L H2SO4调节滤液pH至8~9,得到不溶性白色絮凝状Al(OH)3,减压抽滤得到沉淀;
第三步:硫酸铝溶液的生成。将沉淀转移至250mL烧杯中,边加热边滴入一定浓度和体积的H2SO4溶液;
第四步:硫酸铝钾溶液的形成。待沉淀全部溶解后加入一定量的固体K2SO4,将得到的饱和澄清溶液冷却降温直至晶体全部析出,减压抽滤、洗涤、抽干,获得产品明矾晶体[KAl(SO4)2·12H2O,M=474g/mol]。
回答下列问题:
(1)第一步铝的溶解过程中涉及到的主要反应的离子方程式为__________________________
(2)为了加快铝制品的溶解,应该对铝制品进行怎样的预处理:________________________
(3)第四步操作中,为了保证产品的纯度,同时又减少产品的损失,应选择下列溶液中的___(填选项字母)进行洗涤,实验效果最佳。
A.乙醇 B.饱和K2SO4溶液 C.蒸馏水 D.1:1乙醇水溶液
(4)为了测定所得明矾晶体的纯度,进行如下实验操作:准确称取明矾晶体试样4.0g于烧杯中,加入50mL 1mol/L盐酸进行溶解,将上述溶液转移至100mL容量瓶中,稀释至刻度线,摇匀;移取25.00 mL溶液干250 mL锥形瓶中,加入30 mL 0.10mol/L EDTA-2Na标准溶液,再滴加几滴2D二甲酚橙,此时溶液呈黄色;经过后续一系列操作,最终用0.20 mol/L锌标准溶液滴定至溶液由黄色变为紫红色,达到滴定终点时,共消耗5.00 mL锌标准溶液。滴定原理为H2Y2-+Al3+→AlY-+2H+,H2Y2-(过量)+Zn2+→ZnY2-+2H+(注:H2Y2-表示EDTA-2Na标准溶液离子)。则所得明矾晶体的纯度为_________%。
(5)明矾除了可以用作人们熟悉的净水剂之外,还常用作部分食品的膨松剂,例如油条(饼)的制作过程需要加入一定量的明矾,请简述明矾在面食制作过程作膨松剂的原理:_______
(6)为了探究明矾晶体的结晶水数目及分解产物,在N2气流中进行热分解实验,得到明矾晶体的热分解曲线如图所示(TG%代表的是分解后剩余固体质量占样品原始质量的百分率,失重百分率=![]() ×100%):
×100%):
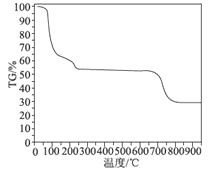
根据TG曲线出现的平台及失重百分率,30~270℃范围内,失重率约为45.57%,680~810℃范围内,失重百分率约为25.31%,总失重率约为70.88%,请分别写出所涉及到30~270℃、680~810℃温度范围内这两个阶段的热分解方程式:___________、_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示为常见气体制备、干燥、性质验证和尾气处理的部分仪器装置(加热设备及夹持固定装置均略去),请根据要求完成下列各题,仪器装置可任意选用,必要时可重复选择。
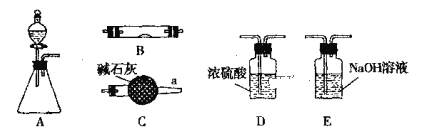
(1)若锥形瓶中盛装锌片,分液漏斗中盛装稀硫酸,可验证H2的还原性并检验其氧化产物。
①当仪器连接顺序为A→D→B→B→C时,两次使用B装置,其中所盛的药品依次是CuO、____________。
②检查好装置的气密性后加热B前必须进行的操作是_________________ 。
(2)若锥形瓶中盛装Na2O2固体,分液漏斗中盛装浓氨水,B中盛装固体催化剂,可进行氨的催化氧化,其反应产物为NO和H2O。
①各仪器装置按气流方向从左到右连接顺序A→C→B→C,请写出B中氨的催化氧化反应方程式____________________________ 。
②装置B中可能观察到的现象是_____________________________。
(3)若锥形瓶中盛装Na2SO3固体,分液漏斗中盛装H2SO4溶液,B中盛装Na2O2固体,可探究SO2气体与过氧化钠反应时是否有O2生成。根据气流方向,装置的连接顺序为:A→D→B→E,根据实验现象回答问题:
①若将带余烬的木条靠近E的导管口,木条复燃,SO2表现酸性氧化物的性质,则反应的方程式可能为:____________________;
②若在E的导管口未收集到任何气体,SO2只表现还原性,则反应的方程式可能为:____________________。
③装置B中观察到的现象是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2CO3溶液中存在平衡:CO32- + H2O![]() HCO3- + OH-,下列有关说法正确的是( )
HCO3- + OH-,下列有关说法正确的是( )
A.离子浓度:c(Na+) > c(CO32-) > c(OH-) > c(H+)
B.升高温度,平衡向逆反应方向移动
C.加入NaCl溶液,溶液的pH增大
D.加入NaOH固体,溶液的pH减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com