
【题目】常温下联氨(![]() )的水溶液中有:① N2H4+H2O
)的水溶液中有:① N2H4+H2O![]() N2H5++OH- K1
N2H5++OH- K1
② N2H5++H2O![]() N2H62++OH- K2,该溶液中微粒的物质的量分数
N2H62++OH- K2,该溶液中微粒的物质的量分数![]() 随
随![]() 变化的关系如图所示。下列叙述错误的是
变化的关系如图所示。下列叙述错误的是

A. 图中Ⅲ对应的液粒为![]()
B. 由图可知,![]()
C. 若![]() 点为
点为![]() 溶液,则存在:
溶液,则存在:![]()
D. 反应②为![]() 的水解方程式
的水解方程式
【答案】D
【解析】
横坐标为OH-浓度的负对数值,从左到右OH-的浓度越来越小,越能促进N2H4电离,纵坐标为微粒的物质的量分数δ(X),故Ⅰ对应的微粒为N2H4,Ⅱ对应的微粒为N2H5+,Ⅲ对应的微粒为N2H62+。
根据上述分析可知,
A. 图中Ⅲ对应的OH-的浓度最小,N2H4电离平衡正向移动的程度最大,则Ⅲ对应的微粒为N2H62+,A项正确;
B. 从图象可得B点N2H5+、N2H62+物质的量分数相等,说明它们的浓度相等,此时根据横坐标可知c(OH-)=![]() ,则
,则![]() =
=![]() =
=![]() =
=![]() , B项正确;
, B项正确;
C. 由电荷守恒可知:c(OH-)+c(Cl-)=c(N2H5+ )+2c(N2H62+)+c(H+),从图象可得C点c(OH-)<c(H+),故c(Cl-)>c(N2H5+ )+2c(N2H62+),C项正确;
D. 反应②为N2H4的二级电离方程式,D项错误;
答案选D。


科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁分别是Na2CO3溶液、AgNO3溶液、BaCl2 溶液、盐酸四种无色溶液中的一种,现进行了如图所示的实验。

(1)通过上述实验判断出各物质:甲___、乙___、丙___、丁____。写出甲与乙反应的离子方程式:___。
(2)实验室有一瓶标签破损(如图所示)的固体试剂。某同学应用(1)中的BaCl2溶液检验,取试剂瓶中的固体少量于试管中,加适量蒸馏水溶解,在所得溶液中加入过量BaCl2溶液,得到白色沉淀。由此,该同学推断这瓶试剂是硫酸钠。你认为他的结论是否正确? _____(填“正确”或“不正确”)。若正确,请写出相应反应的离子方程式__________;若不正确, 请说明可能的结论:_______(填物质的化学式)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氟化钙材料具有良好的透光性和较低的折射率,可用做紫外和红外光学元件、不可见光谱范围内的消色差镜头。如图为氟化钙晶胞,其中小球代表Ca2+,大球代表F-。
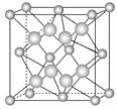
(1)每个晶胞实际含有________个Ca2+和________个F-。
(2)氟化钙晶体可以看作Ca2+按__________堆积排列,F-填入Ca2+堆积的部分空隙中。每个Ca2+周围有__________个F-,而每个F-周围有_________个Ca2+,每个F-周围与其距离最近的F-的数目是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示晶体结构是一种具有优良的电压、电光等功能的晶体材料的最小结构单元(晶胞).晶体内与每个“Ti”紧邻的氧原子数和这种晶体材料的化学式分别是(各元素所带电荷均已略去)( )
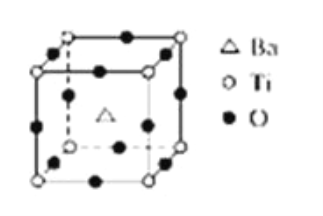
A. 8;BaTi8O12
B. 8;BaTi4O9
C. 6;BaTiO3
D. 3;BaTi2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可用如下方法制取Cl2,根据相关信息,回答下列问题:
(1)用双线桥法表示电子转移方向和数目_____:①MnO2 +4HCl(浓)=== Cl2↑+ MnCl2+ 2H2O
(2)若反应中有0.1mol的氧化剂被还原,则被氧化的物质为__(填化学式),被氧化的物质的量为 _____,同时转移电子数为_____。
(3)将(2)生成的氯气与 0.2mol H2 完全反应,生成的气体在标准状况下所占体积为_____L,将此产物溶于水配成100mL溶液,此溶液的物质的量浓度为_______。(已知:H2+Cl2![]() 2HCl)
2HCl)
(4)②KClO3+6HCl(浓)===3Cl2↑+KCl+3H2O③2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O
若要制得相同质量的氯气,①②③三个反应中电子转移的数目之比为____。
(5)已知反应4HCl(g)+O2 ![]() 2Cl2+2H2O(g),该反应也能制得氯气,则MnO2、O2、KMnO4三种物质氧化性由弱到强的顺序为_______。
2Cl2+2H2O(g),该反应也能制得氯气,则MnO2、O2、KMnO4三种物质氧化性由弱到强的顺序为_______。
(6)将不纯的NaOH样品2.50 g(样品含少量Na2CO3和水),放入50.0 mL 2.00mol/L盐酸中,充分反应后,溶液呈酸性,中和多余的酸又用去40.0 mL 1.00 mol/L的NaOH溶液。蒸发中和后的溶液,最终得到_____g固体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究和深度开发CO、CO2的应用具有重要的社会意义.回答下列问题:
I.CO可用于高炉炼铁,已知:
Fe3O4(s)+4CO(g)=3Fe(s)+4CO2 (g) △H1=akJ/mol
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2 (g) △ H2=bkJ/mol
则反应Fe2O3(s)+3CO(g)=2Fe(s)++3CO2 (g)的△H=______kJ/mol
Ⅱ.—定条件下,CO2和CO可以互相转化
(1)某温度下,在容积为2 L的密闭容器按甲、乙两种方式投入反应物发生反应:
CO2 (g)+H2(g) ![]() CO(g)+H2O(g)
CO(g)+H2O(g)

甲容器15 min后达到平衡,此时CO2的转化率为75%。则015 min内平均反应速率_______,此条件下该反应的平衡常数K= ____。欲使平衡后乙与甲中相同组分气体的体积分数相等,则w、x、y、z需满足的关系是: y____z(填或“>”“<”“ = ”),且y=_________(用含的等式表示)。
(2)研究表明,温度、压强对反应“C6H5CH2CH3 (g)+CO2(g) ![]() C6H5CH=CH2(g)+CO(g) + H2O(g)”中乙苯的平衡转化率影响如图所示:
C6H5CH=CH2(g)+CO(g) + H2O(g)”中乙苯的平衡转化率影响如图所示:

则△H_____(填“>”、“<”或“ = ”),压强p1、p2、p3从大到小的顺序是_____。
(3)CO可被NO2氧化:CO+NO2 =CO2+ NO。当温度高于225℃时,反应速率![]() 正=k正 c(CO) c(NO2),
正=k正 c(CO) c(NO2), ![]() 逆=k逆 c(CO2) c(NO), k正、k逆分别为正、逆反应速率常数。在上述温度范围内, k正、k逆与该反应的平衡常数K之间的关系为___________。
逆=k逆 c(CO2) c(NO), k正、k逆分别为正、逆反应速率常数。在上述温度范围内, k正、k逆与该反应的平衡常数K之间的关系为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水占地球总储水量的97.2%,若把海水淡化和化工生产结合起来,既可解决淡水资源缺乏的问题,又可充分利用海洋资源。
(1)海水中存在大量的氯化钠,氯化钠中的金属元素位于元素周期表第________族。
(2)目前,国际上实用的“海水淡化”主要技术之一是蒸馏法。蒸馏法是将海水变成蒸气,蒸气经冷却而得高纯度淡水。由此可判断蒸馏法是________________(填“物理变化”或“化学变化”)。
(3)工业上利用电解饱和食盐水可制得重要化工产品,反应式:食盐+H2O―→NaOH+H2↑+Cl2↑(未配平),该反应中食盐的化学式是________________________;利用电解所得气体制36.5%的浓盐酸1 000 t,最少需消耗食盐________ t。
(4)近年来,有人提出了一种利用氯碱工业产品及氯化钠循环治理含二氧化硫废气并回收二氧化硫的方法。该方法流程如下:

请写出②④的化学反应方程式:______,________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年3月,我国科学家研发出一种新型的锌碘单液流电池,其原理如图所示。下列说法不正确的是

A. 放电时B电极反应式为:I2+2e-=2I-
B. 放电时电解质储罐中离子总浓度增大
C. M为阳离子交换膜,N为阴离子交换膜
D. 充电时,A极增重65g时,C区增加离子数为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】①C(s)+O2(g)![]() CO2(g) ΔH=-393.5kJ/mol
CO2(g) ΔH=-393.5kJ/mol
②2H2(g)+O2(g)![]() 2H2O(1) ΔH=-571.6kJ/mol
2H2O(1) ΔH=-571.6kJ/mol
现在0.2mol炭粉和氢气组成的悬浮气,在氧气中完全燃烧,共放出67.93kJ的热量,则混合物中C与H2物质的量之比为
A.1︰1 B.1︰2 C.2︰3 D.3︰2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com