
【题目】实验室可用如下方法制取Cl2,根据相关信息,回答下列问题:
(1)用双线桥法表示电子转移方向和数目_____:①MnO2 +4HCl(浓)=== Cl2↑+ MnCl2+ 2H2O
(2)若反应中有0.1mol的氧化剂被还原,则被氧化的物质为__(填化学式),被氧化的物质的量为 _____,同时转移电子数为_____。
(3)将(2)生成的氯气与 0.2mol H2 完全反应,生成的气体在标准状况下所占体积为_____L,将此产物溶于水配成100mL溶液,此溶液的物质的量浓度为_______。(已知:H2+Cl2![]() 2HCl)
2HCl)
(4)②KClO3+6HCl(浓)===3Cl2↑+KCl+3H2O③2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O
若要制得相同质量的氯气,①②③三个反应中电子转移的数目之比为____。
(5)已知反应4HCl(g)+O2 ![]() 2Cl2+2H2O(g),该反应也能制得氯气,则MnO2、O2、KMnO4三种物质氧化性由弱到强的顺序为_______。
2Cl2+2H2O(g),该反应也能制得氯气,则MnO2、O2、KMnO4三种物质氧化性由弱到强的顺序为_______。
(6)将不纯的NaOH样品2.50 g(样品含少量Na2CO3和水),放入50.0 mL 2.00mol/L盐酸中,充分反应后,溶液呈酸性,中和多余的酸又用去40.0 mL 1.00 mol/L的NaOH溶液。蒸发中和后的溶液,最终得到_____g固体。
【答案】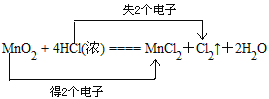
HCl 0.2mol 1.204×1023 4.48 2mol/L 6∶5∶6 O2﹤MnO2﹤KMnO4 5.85
【解析】
(1)利用化合价升降法判断氧化剂、还原剂、氧化产物及还原产物和转移电子数目;
(2)反应中二氧化锰作氧化剂,化合价降低,被还原,HCl为还原剂,被氧化,生成氯气;
(3)根据反应H2+ Cl2=2HCl,利用较少的物质完全反应进行计算;
(4)利用化合价升降法计算转移电子数目;
(5)氧化还原反应中氧化剂的氧化性越强,反应的条件越简单;
(6)根据元素守恒,反应的最终产物为NaCl进行计算。
(1)反应中Mn的化合价由+4价变为+2价,得电子,Cl的化合价由-1价变为0价,失电子,则最小公倍数为2,双线桥法为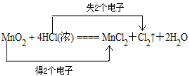 ;
;
(2)反应中二氧化锰作氧化剂,化合价降低,被还原,HCl为还原剂,被氧化,生成氯气;0.1mol MnO2反应,转移0.2mol电子,生成0.1mol氯气,则被氧化的HCl为0.2mol;
(3)n(H2):n(Cl2)=2:1,则氯气少量,为0.1mol,根据反应H2+ Cl2=2HCl,生成0.2molHCl,其标况下的体积为4.48L;c(HCl)=n/V=0.2mol/0.1L=2mol/L;
(4)若制取1mol氯气时,①转移2mol电子;②KClO3中Cl的化合价由+5变为0价,转移5个电子,生成3个氯气,则生成1mol氯气时,转移5/3mol电子;③KMnO4中Mn的化合价由+7变为+2价,转移10个电子,生成5个氯气,则生成1mol氯气时,转移2mol电子,制得相同质量的氯气,电子转移的数目之比为2:![]() :2=6:5:6;
:2=6:5:6;
(5)氧化还原反应中氧化剂的氧化性越强,反应的条件越简单,则氧化性由弱到强的顺序为O2﹤MnO2﹤KMnO4;
(6)加入的n(Cl-)=0.05mL× 2.00mol/L=0.1mol,反应的最终产物为NaCl,根据元素守恒,则n(NaCl)=0.1mol,其质量为5.85g。


科目:高中化学 来源: 题型:
【题目】对于可逆反应2A(?)+B(g)![]() 2C(g);下图是其它条件一定时反应中C的百分含量与压强的关系曲线。回答下列问题:
2C(g);下图是其它条件一定时反应中C的百分含量与压强的关系曲线。回答下列问题:

(1)物质A的状态是_________(填“气体”、“液体”或“固体”);
(2)图-1中a、b、c、d四点中表示未达到平衡状态且v正<v逆 的点是_____;
(3)v(a)、v(b)、v(c)按由大到小排序_________________;
(4)对于2SO2(g)+O2(g)![]() 2SO3(g);ΔH=-198 kJ/mol。在实际生产过程中,原料气中SO2为7%(体积分数)、O2为11%,常压下进行,控制温度在450℃左右。
2SO3(g);ΔH=-198 kJ/mol。在实际生产过程中,原料气中SO2为7%(体积分数)、O2为11%,常压下进行,控制温度在450℃左右。
请问原料气中SO2与O2的体积比不是2∶1,而要7∶11(大约2∶3)的原因是___________;如果在恒容容器中,仅把另外82%的其他气体“抽出来”,是否会减小SO2的转化率__________(填“会”或“不会”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,lmolCH3OH与一定量O2发生反应时,生成CO、CO2或HCHO的能量变化如下图所示[反应物O2(g)和生成物H2O(g)已略去]。

回答下列问题:
(1)在有催化剂作用下,CH3 OH与O2反应主要生成 ___(填“CO2、CO或HCHO”);计算:2HCHO(g)+O2(g)=2CO(g)+2H2O(g)![]() =_____________
=_____________
(2)已知:CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g) ![]()
①经测定不同温度下该反应的平衡常数如下:

该反应为 ___(填“放热”或“吸热”)反应;250℃时,某时刻测得该反应的反应物与生成物浓度为c(CO) =0.4mol/L、c(H2) =0. 4mol/L、c(CH3 OH) =0. 8mol/L,则此时υ(正)____υ(逆)(填“>”、“=”或“<”)。
②某温度下,在体积固定的2L密闭容器中将1molCO和2molH2混合,使反应得到平衡,实验测得平衡时与起始时的气体压强比值为0 .7,则该反应的平衡常数为____(保留l位小数)。
(3)利用钠碱循环法可除去SO2。常温下,若吸收液吸收一定量SO2后的溶液中,n(SO32-):n(HSO3-) =3:2,则此时溶液呈____(填“酸性”、“中性”或“碱性”)。(已知:H2SO3的电离常数为:Kal=l. 54×10-2、Ka2=l. 02×l0-7)
(4)利用电化学法处理工业尾气SO2的装置如图所示,写出Pt(2)电极反应式:______;当电路中转移0. 02 mol e-时(较浓H2SO4尚未排出),交换膜左侧溶液中约增加___ mol离子。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关有机化合物的说法正确的是
A. 麦芽糖的水解产物有两种,且互为同分异构体
B. 等质量的苯和苯乙烯完全燃烧,消耗氧气的体积在相同条件下不相同
C. 间二甲苯中苯环上的一个氢原子被“![]() ”取代时,有9种结构(不考虑立体异构)
”取代时,有9种结构(不考虑立体异构)
D. ![]() 与甲苯或甘油在一定条件下发生反应,其反应类型不同
与甲苯或甘油在一定条件下发生反应,其反应类型不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于晶体的说法一定正确的是( )

(图中Ca2+、O2-、Ti4+分别位于立方体的体心、面心和顶点)
A. 分子晶体中都存在共价键
B. CaTiO3晶体中每个Ti4+和12个O2-相紧邻
C. SiO2晶体中每个硅原子与两个氧原子以共价键相结合
D. 金属晶体的熔点都比分子晶体的熔点高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下联氨(![]() )的水溶液中有:① N2H4+H2O
)的水溶液中有:① N2H4+H2O![]() N2H5++OH- K1
N2H5++OH- K1
② N2H5++H2O![]() N2H62++OH- K2,该溶液中微粒的物质的量分数
N2H62++OH- K2,该溶液中微粒的物质的量分数![]() 随
随![]() 变化的关系如图所示。下列叙述错误的是
变化的关系如图所示。下列叙述错误的是

A. 图中Ⅲ对应的液粒为![]()
B. 由图可知,![]()
C. 若![]() 点为
点为![]() 溶液,则存在:
溶液,则存在:![]()
D. 反应②为![]() 的水解方程式
的水解方程式
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2001年是伟大的化学家、1954年诺贝尔化学奖得主、著名的化学结构大师、20世纪的科学怪杰鲍林(L.Pauling)教授的诞辰100周年。1994年这位老人谢世后,人们打开他的办公室,发现里面有一块黑板,画得满满的,其中一个结构式如图所示。老人为什么画这个结构式?它能合成吗?它有什么性质?不得而知。这是鲍林留给世人的一个谜,也许这是永远无法解开的谜,也许有朝一日你就能解开它。不管结果如何,让我们先对这个结构作一番了解。

(1)它的分子式是__________________________________________________________。
(2)它的所有原子是否可能处于同一个平面上?________(填“可能”或“不可能”)。
(3)它是否带有电荷?________(填“是”或“否”)。
(4)该分子中sp杂化的氮原子有___个;sp2杂化的氮原子有___个;sp3杂化的氮原子有_____个。
(5)为什么人们推测它是炸药?______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】决定物质性质的重要因素是物质结构.请回答下列问题.
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如下表所示:

则,A的化合价__B的化合价(填“>”、“<”或“=”).
(2)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如图所示),其中3种离子晶体的晶格能数据如下表:


则该 4种离子晶体(不包括NaCl)熔点从高到低的顺序是:__.
(3)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好.离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是___________________________.
(4)某配合物的分子结构如图所示,则N原子的杂化方式为__;基态Ni原子的电子排布式__.

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着我国汽车年销量的大幅增加,给空气环境造成了很大的污染。汽车尾气装置里,气体在催化剂表面吸附与解吸作用的过程如图所示,下列说法正确的是( )

A. 反应中NO为氧化剂,N2为氧化产物
B. 汽车尾气的主要污染成分包括CO、NO和N2
C. NO和O2必须在催化剂表面才能反应
D. 催化转化总化学方程式为2NO+O2+4CO ![]() 4CO2+N2
4CO2+N2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com