
【题目】测定平衡常数对定量认识化学反应具有重要意义。已知:I2能与I一反应成I3一,并在溶液中建立如下平衡:I2+I一 ![]() I3一。通过测平衡体系中c(12)、c(I-)和c(I3-),就可求得该反应的平衡常数。
I3一。通过测平衡体系中c(12)、c(I-)和c(I3-),就可求得该反应的平衡常数。
I、某同学为测定上述平衡体系中c (12),采用如下方法:取V1mL平衡混合溶液,用c mol/L的Na2S203溶液进行滴定(反应为I2+2Na2S203=2Nal+Na2S406),消耗V2mL的Na2S203溶液。根据V1、V2和c可求得c(I2)。
(1)上述滴定时,可采用____ 做指示剂,滴定终点的现象是____。
(2)下列对该同学设计方案的分析,正确的是______填字母)。
A.方案可行。能准确测定溶液中的c (12)
B.不可行。因为I一能与Na2S203发生反应
C.不可行。只能测得溶液中c(I2)与c(I3-)之和
Ⅱ、化学兴趣小组对上述方案进行改进,拟采用下述方法来测定该反应的平衡常数(室温条件下进行,溶液体积变化忽略不计):

已知:①I-和I3一不溶于CC14;②一定温度下碘单质在四氯化碳和水混合液体中,碘单质的浓度比值即是一个常数(用Kd表示,称为分配系数),且室温条件下Kd=85。回答下列问题:
(3)操作I使用的玻璃仪器中,除烧杯、玻璃棒外,还需要的仪器是____(填名称)。试指出该操作中应注意的事项为____。(任写一条)
(4)下层液体中碘单质的物质的量浓度是________。
(5)实验测得上层溶液中c(I3一)=0.049 mol/L,结合上述有关数据,计算室温条件下反应I2+I一![]() I3一的平衡常数K= ___(用具体数据列出计算式即可)。
I3一的平衡常数K= ___(用具体数据列出计算式即可)。
【答案】 淀粉 溶液由蓝色变无色,且半分钟内颜色不再改变 C 分液漏斗 分液时上层液体应从上口出,下层液体应从下口出(或分液漏斗末端应紧靠烧杯内壁或
打开上口活塞,使分液漏斗内外压强相等便于液体流下等(其他合理答案也给分) 0.085mol/L 961
【解析】(1)碘单质遇淀粉,溶液呈特殊的蓝色,即可用淀粉做指示剂。滴定终点碘被反应掉,现象是:溶液由蓝色变无色
(2)由于碘单质能与I-反应成I3-,并在溶液中建立如下平衡:I2+I-![]() I3-。随着碘单质浓度的减小,平衡向左移动,所以上述的方案只能测得溶液中c(I2)与c(I3-)之和,方案不可行。
I3-。随着碘单质浓度的减小,平衡向左移动,所以上述的方案只能测得溶液中c(I2)与c(I3-)之和,方案不可行。
(3)萃取后溶液分为有机层与水溶液层,操作I就是分液操作:用分液漏斗将其分离
分液过程的注意事项包括:一是上下层液体不能混合,分液时上层液体应从上口出,下层液体应从下口出;二是分液漏斗末端应紧靠烧杯内壁;三是打开上口活塞,使分液漏斗内外压强相等便于液体流下等
(4)根据:I2+2Na2S2O3=2NaI+Na2S4O6),则

解得下层液体中![]() = 0.085mol/L
= 0.085mol/L
(5) 由Kd=![]() =85求得上层溶液中
=85求得上层溶液中![]() = 0.085/85=0.001mol/L
= 0.085/85=0.001mol/L
又原溶液中c(I-)=0.1mol·L-1,所得到的上层溶液中c(I3-)="0.049" mol·L-1
由反应I2+I-![]() I3-可知,上层溶液中c(I-)=(0.1—0.049)mol·L-1=0.051mol·L-1
I3-可知,上层溶液中c(I-)=(0.1—0.049)mol·L-1=0.051mol·L-1
所以,在此温度下反应I2+I-![]() I3平衡常数K=
I3平衡常数K=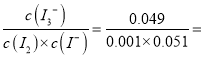 961
961


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
【题目】乙二酸俗名草酸,下面是化学学习小组的同学对草酸晶体(H2C2O4·xH2O)进行的探究性学习的过程,请你参与并协助他们完成相关学习任务。该组同学的研究课题是:探究测定草酸晶体(H2C2O4·xH2O)中的x值。通过查阅资料和网络查寻,得知草酸易溶于水,其水溶液可以用酸性KMnO4溶液进行滴定,反应原理为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。
学习小组的同学设计了如下滴定方法测定x值:
①称取1.260g草酸晶体,将其制成100.00mL水溶液为待测液;
②取25.00mL待测液放入锥形瓶中,再加入适量的稀硫酸;
③用浓度为0.1000mol·L-1的酸性KMnO4标准溶液进行滴定,达到滴定终点时消耗标准溶液10.00mL。
回答下列问题:
(1)滴定时,将酸性KMnO4标准液装在如右图中的___________ (填“甲”或“乙”)滴定管中。

(2)本实验到达滴定终点的标志是________________________________。
(3)通过上述数据,求得x=___________。
(4)若滴定到终点时俯视滴定管刻度线读数,则由此测得的x值会___________ (填“偏大”“偏小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验小组制备高铁酸钾(K2FeO4)并探究其性质。
资料:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4(夹持装置略)

①A为氯气发生装置。A中反应方程式是________________(锰被还原为Mn2+)。
②将除杂装置B补充完整并标明所用试剂。_______
③C中得到紫色固体和溶液。C中Cl2发生的反应有
3Cl2+2Fe(OH)3+10KOH![]() 2K2FeO4+6KCl+8H2O,另外还有________________。
2K2FeO4+6KCl+8H2O,另外还有________________。
(2)探究K2FeO4的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明是否K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
方案Ⅰ | 取少量a,滴加KSCN溶液至过量,溶液呈红色。 |
方案Ⅱ | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b。取少量b,滴加盐酸,有Cl2产生。 |
i.由方案Ⅰ中溶液变红可知a中含有______离子,但该离子的产生不能判断一定是K2FeO4将Cl-氧化,还可能由________________产生(用方程式表示)。
ii.方案Ⅱ可证明K2FeO4氧化了Cl-。用KOH溶液洗涤的目的是________________。
②根据K2FeO4的制备实验得出:氧化性Cl2________![]() (填“>”或“<”),而方案Ⅱ实验表明,Cl2和
(填“>”或“<”),而方案Ⅱ实验表明,Cl2和![]() 的氧化性强弱关系相反,原因是________________。
的氧化性强弱关系相反,原因是________________。
③资料表明,酸性溶液中的氧化性![]() >
>![]() ,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性
,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性![]() >
>![]() 。若能,请说明理由;若不能,进一步设计实验方案。
。若能,请说明理由;若不能,进一步设计实验方案。
理由或方案:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】活性ZnO在橡胶、塑料等工业中有重要应用,某工厂以含铅锌烟气(主要成分是ZnO、PbO,还有少量FeO、CuO)制备活性ZnO的工艺流程如下:

(1)下图为温度与Zn、Pb元素浸出率的关系图,“酸浸”时采用30℃而不是更高的温度的原因是:①减少盐酸挥发;②____。

(2)“氧化”的目的是除去酸浸液中的Fe2+,在pH约为5.1的溶液中,加入高锰酸钾溶液,生成MnO2和Fe(OH)3沉淀,该反应的离子方程式为____。
(3)①若“过滤I”所得的滤液浑浊,则处理的方法为____。
②“除杂”时,滤渣Ⅱ的主要成分是Cu、Pb,试剂X应为____。
(4)在“过滤Ⅱ”后的溶液中加入Na2CO3溶液,生成碱式碳酸锌[Zn2(OH)2CO3]等物质。
①该反应的化学方程式为____。
②检验碱式碳酸锌洗涤干净的操作为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮元素是造成水体富营养化的主要原因,在水中常以氨氮或NO3形式存在。
(1)在pH为4~6时,用H2在Pd-Cu催化下将NO3-还原为N2可消除水中NO3。该反应的离子方程式为____。若用H2和CO2的混合气体代替H2,NO3-去除效果更好,其原因是____。
(2)NaClO氧化可除去氨氮,反应机理如图1所示(其中H2O和NaCl略去),实验测得相同条件下,相同反应时间,pH与氨氮的去除率关系如图2所示,温度与氨氮去除率关系如图3所示。



图1 图2 图3
①NaClO氧化NH3的总反应的化学方程式为____。
②如图2所示,在pH>9时,pH越大去除率越小,其原因是____。
③如图3所示,温度低于15℃时,温度越低去除率越低其原因是____。当温度高于25℃时,温度越高去除率也越低,其原因是____。
(3)用电化学法可去除废水中的氨氮。在含NH4+的废水中加入氯化钠,用惰性电极电解。反应装置如图4所示,则电解时,a极的电极反应式为____。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)按如图所示操作,充分反应后:

①Ⅰ中发生反应的离子方程式为_____________________________________________;
②Ⅱ中铜丝上观察到的现象是________________________________________________;
③结合Ⅰ、Ⅱ实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为______________________。
(2)某一反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO、H2O。该反应物中还原产物是____________;若反应方程式中转移了0.3 mol电子,则氧化产物的质量是________g。
(3)将少量Cl2通入FeBr2的溶液中,反应的离子方程式为2Fe2++Cl2===2Fe3++2Cl-,这个事实说明具有还原性的粒子还原性强弱为_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胡椒酚是植物挥发油中的一种成分。关于胡椒酚的下列说法:①该化合物属于芳香烃;②分子中至少有7个碳原子处于同一平面;③它的部分同分异构体能发生银镜反应;④1 mol该化合物最多可与2 mol Br2发生反应。其中正确的是( )

A. ①③ B. ②③ C. ①②④ D. ②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 。分析下图变化,试回答下列问题:(E没有支链)
。分析下图变化,试回答下列问题:(E没有支链)

(1)写出下列有机物的结构简式:
A___________________C _______________________E ____________________F_________________。
(2)写出下列有关反应的化学方程式:
C →D_______________________;
D →E_______________________;
E→F_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以高硫铝土矿(主要成分为Al2O3、Fe2O3、SiO2,少量FeS2和金属硫酸盐)为原料,生产氧化铝并获得Fe3O4的部分工艺流程如下:

(1)焙烧过程均会产生SO2,用NaOH溶液吸收过量SO2的离子方程式为______________________。
(2)添加1%CaO和不添加CaO的矿粉焙烧,其硫去除率随温度变化曲线如题16图所示。

已知:多数金属硫酸盐的分解温度都高于600 ℃
硫去除率=(1—![]() )×100%
)×100%
①不添加CaO的矿粉在低于500 ℃焙烧时,去除的硫元素主要来源于__________________。
②700℃焙烧时,添加1%CaO的矿粉硫去除率比不添加CaO的矿粉硫去除率低,其主要原因是______________________________________________________。
(3)向“过滤”得到的滤液中通入过量CO2,铝元素存在的形式由_______________(填化学式)转化为_______________(填化学式)。
(4)“过滤”得到的滤渣中含大量的Fe2O3。Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,理论上完全反应消耗的n(FeS2)∶n(Fe2O3)=__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com