
【题目】(10分)某同学帮助水质检测站配制480 mL 0.5 mol·L-1NaOH溶液以备使用。
(1)该同学应选择________mL的容量瓶。
(2)其操作步骤如下图所示,
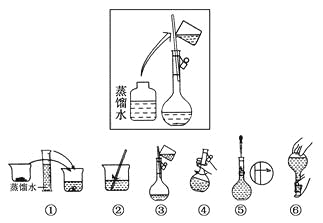
则如图操作应在下图中的________(填选项字母)之间。
A.②与③ B.①与② C.④与⑤
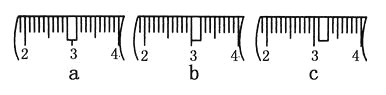
(3)该同学应称取NaOH固体________g,用质量为23.1 g的烧杯放在托盘天平上称取所需NaOH固体时,请在附表中选取所需的砝码大小________(填字母),并在下图中选出能正确表示游码位置的选项________(填字母)。
附表 砝码规格
a | b | c | d | e | |
砝码大小/g | 100 | 50 | 20 | 10 | 5 |
(4)下列操作对所配溶液的浓度大小有何影响?
①转移完溶液后未洗涤玻璃棒和烧杯,浓度会________(填“偏大”、“偏小”或“无影响”,下同)
②容量瓶中原来有少量蒸馏水,浓度会________。
【答案】20.(10分) (1) 500(2分) (2) C(2分) (3) 10.0(2分) c、d (1分)c(1分)
(4)①偏小(1分) ②无影响(1分)
【解析】试题(1)没有480mL容量瓶,选择500mL容量瓶;(2)操作步骤有计算、称量、溶解、移液、洗涤移液、摇匀、定容、摇匀等操作,所以如图操作应在④与⑤之间;(3)需氢氧化钠的质量为m=0.5L×0.5molL-1×40g/mol=10.0g.答案为10.0;质量为23.1的烧杯和10克NaOH总质量为33.1,所以用20g和10g的砝码,3.1g用游码,选c、d c (4)①没有洗涤烧杯和玻璃棒,导致溶质质量减少,所配溶液浓度偏低;②容量瓶不干燥,含有少量蒸馏水,对溶液浓度无影响。


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:
【题目】化合物Bilirubin在一定波长的光照射下发生分解反应,反应物浓度随反应时间变化如下图所示,计算反应4~8 min间的平均反应速率和推测反应16 min时反应物的浓度,结果应是( )
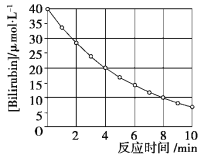
A.2.5 μmol·L-1·min-1和2.0 μmol·L-1
B.2.5 μmol·L-1·min-1和2.5 μmol·L-1
C.3.0 μmol·L-1·min-1和3.0 μmol·L-1
D.5.0 μmol·L-1·min-1和3.0 μmol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表隐含着许多信息和规律。以下所涉及的元素均为中学化学中常见的短周期元素,其原子半径及主要化合价列表如下,其中R2Q2用于呼吸面具或潜水艇中作为氧气来源。

下列说法正确的是
A. T、Z的最高价氧化物对应水化物的酸性T<Z
B. R、X、Y的单质失去电子能力最强的是X
C. M与Q形成的是离子化合物
D. M、Q、Z都在第2周期
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.1mol的KCl和0.1mol的AlCl3溶于水配成100mL混合溶液,下列溶液中Cl-浓度与该混合溶液中Cl-浓度相等的是
A. 3mol/L的NaCl溶液 B. 2mol/L的FeCl3溶液
C. 2mol/L的MgCl2溶液 D. 2mol/L的NaCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,2H2(g)+O2(g)![]() 2H2O(l)+566kJ。下列说法错误的是
2H2O(l)+566kJ。下列说法错误的是
A.H2![]() H+H的过程需要吸热
H+H的过程需要吸热
B.若生成2mol水蒸气,则放出的热量大于566kJ
C.2g氢气完全燃烧生成液态水所释放的能量为283kJ
D.2mol氢气与1mol氧气的能量之和大于2mol液态水的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知图一表示的是可逆反应 CO(g)+H2(g)![]() C(s)+H2O(g)-Q(Q>0)的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应2NO2(g)
C(s)+H2O(g)-Q(Q>0)的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应2NO2(g)![]() N2O4(g)+Q(Q>0)的浓度(c)随时间 t 的变化情况,下列 说法中正确的是
N2O4(g)+Q(Q>0)的浓度(c)随时间 t 的变化情况,下列 说法中正确的是
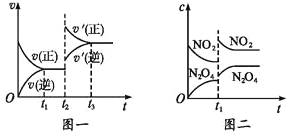
A.图一 t2 时刻改变的条件可能是升高了温度或增大了压强
B.图一 t2 时刻改变的条件可能是通入了 CO 气体
C.图二 t1 时刻改变的条件可能是升高了温度或增大了压强
D.图二 t1 时刻改变的条件是增大压强,则混合气体的平均相对分子质量将减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如图装置,研究非金属元素性质变化规律。
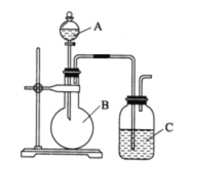
已知:高锰酸钾在常温下与浓盐酸反应产生氯气,离子方程式为______。
(1)如果C中装饱和的H2S溶液,A中装浓盐酸,B中装高锰酸钾溶液,反应开始后观察到现象是C中产生淡黄色沉淀,证明氯的非金属性比硫的非金属性________(填“强”或“弱”或“无法判断”;请用电子式表示H2S的形成过程:_____。
(2)利用如图装置证明Cl2氧化性强于I2的氧化性。则A中装浓盐酸,B中装入高锰酸钾粉末, C中装入淀粉KI溶液,则C中现象是______。
(3)现有浓硝酸、大理石、澄清石灰水、硅酸钠溶液,选择试剂用如图装置证明:非金属性:N > C > Si。C中装试剂______,实验现象为_________该装置存在不足之处,改进措施为:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨和制硫酸是中学阶段重要的化工生产反应。
(1)硫酸工业生产中接触室内发生的反应方程式为___;在实际生产过程中,操作温度选定400-500摄氏度,压强采用常压的原因分别是___。
(2)合成氨反应生成的氨气可用于工业制纯碱,写出以氨气、氯化钠、二氧化碳、水为原料制备纯碱的化学方程式___、___。
(3)合成氨每生成1g液氨,放出QkJ的热量,写出热化学反应方程式___。
(4)常用浓氨水来检查输氯管道是否泄漏,泄漏处会观察到大量的白烟(NH4Cl),还生成一种无色无味的单质气体,写出此反应的化学方程式并标出电子转移的方向和数目____,该反应中被还原的是___,还原产物是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.碳酸氢钠溶液与少量石灰水反应HCO3﹣+Ca2++OH﹣=CaCO3↓+H2O
B.氯化铵与氢氧化钠两种浓溶液混合加热OH﹣+NH4+![]() H2O+NH3↑
H2O+NH3↑
C.氢氧化铁与稀硫酸反应H++OH﹣=H2O
D.单质铜与稀硝酸反应Cu+2H++2NO3﹣=Cu2++2NO↑+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com