
【题目】室温下,2H2(g)+O2(g)![]() 2H2O(l)+566kJ。下列说法错误的是
2H2O(l)+566kJ。下列说法错误的是
A.H2![]() H+H的过程需要吸热
H+H的过程需要吸热
B.若生成2mol水蒸气,则放出的热量大于566kJ
C.2g氢气完全燃烧生成液态水所释放的能量为283kJ
D.2mol氢气与1mol氧气的能量之和大于2mol液态水的能量
 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:
【题目】碱式碳酸镁[4MgCO3·Mg(OH)2·4H2O]是一种重要的无机化工产品。一种由白云石[主要成分为CaMg(CO3)2,含少量SiO2、Fe2O3等]为原料制备碱式碳酸镁(国家标准中CaO的质量分数≤0.43%)的实验流程如下:
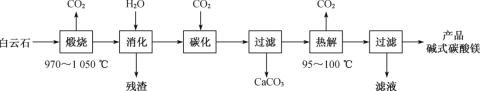
(1)“煅烧”时发生主要反应的化学方程式为___。
(2)常温常压下,“碳化”可使镁元素转化为Mg(HCO3)2,“碳化”时终点pH对最终产品中CaO含量及碱式碳酸镁产率的影响如图1和图2所示。
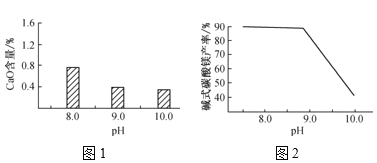
①应控制“碳化”终点pH约为___,钙元素的主要存在形式是___(填化学式)。
②根据图2,当pH=10.0时,镁元素的主要存在形式是___(填化学式)。
(3)“热解”生成碱式碳酸镁的化学方程式为___。
(4)该工艺为达到清洁生产,可以循环利用的物质是___(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图Ⅰ-Ⅳ所示。
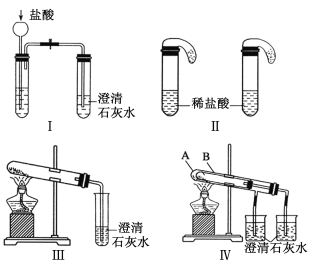
(1)只根据图Ⅰ、Ⅱ所示实验,能够达到实验目的的是(填装置序号)___________;
(2)图Ⅲ、Ⅳ所示实验均能鉴别这两种物质,其反应的化学方程式为___________;
与实验Ⅲ相比,实验Ⅳ的优点是(填选项序号)_____;
A.Ⅳ比Ⅲ复杂 B.Ⅳ比Ⅲ安全
C.Ⅳ比Ⅲ操作简便 D.Ⅳ可以做到一套装置同时进行两个对比实验,而Ⅲ不能
(3)若用实验装置Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是______;
(4)将碳酸氢钠溶液与澄清石灰水混合并充分反应,
①当石灰水过量时,其离子方程式是_____________;
②当碳酸氢钠与氢氧化钙物质的量之比为2:1时,所得溶液中溶质的化学式为______,请设计实验检验所得溶液中溶质的阴离子__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向四瓶盛有相同物质的量的NaOH溶液中通入体积不同的CO2气体,得到①②③④四瓶溶液。分别向四瓶溶液中逐滴加入等体积、等浓度的盐酸,产生的气体体积V(CO2)与所加盐酸体积V(HCl)的关系如下图所示,且图②③④中分别有0A<AB、0A=AB、0A>AB。则下列分析与判断正确的是(忽略CO2的溶解)( )

A.①中通入的CO2最少B.③中的溶质只有Na2CO3
C.有两种溶质的是②和③D.若④中AB>20A,则有c(Na2CO3)>c(NaHCO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列A、B、C、D是中学常见混合物分离或提纯的基本装置。请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置。将A、B、C、D填入适当的空格中。

(1)除去Ca(OH)2溶液中悬浮的CaCO3_________________;
(2)从碘水提取碘______________;
(3)用自来水制取蒸馏水_________________;
(4)分离植物油和水_____________;
(5)与海水晒盐原理相符的是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(10分)某同学帮助水质检测站配制480 mL 0.5 mol·L-1NaOH溶液以备使用。
(1)该同学应选择________mL的容量瓶。
(2)其操作步骤如下图所示,
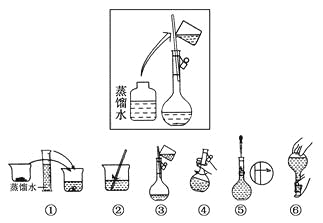
则如图操作应在下图中的________(填选项字母)之间。
A.②与③ B.①与② C.④与⑤
(3)该同学应称取NaOH固体________g,用质量为23.1 g的烧杯放在托盘天平上称取所需NaOH固体时,请在附表中选取所需的砝码大小________(填字母),并在下图中选出能正确表示游码位置的选项________(填字母)。
附表 砝码规格
a | b | c | d | e | |
砝码大小/g | 100 | 50 | 20 | 10 | 5 |
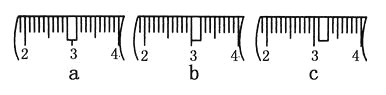
(4)下列操作对所配溶液的浓度大小有何影响?
①转移完溶液后未洗涤玻璃棒和烧杯,浓度会________(填“偏大”、“偏小”或“无影响”,下同)
②容量瓶中原来有少量蒸馏水,浓度会________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现定义pOH=![]() lg[OH],如图说法正确的是
lg[OH],如图说法正确的是
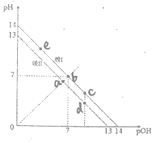
A.图中线II的温度低于室温
B.图中五点Kw间的关系是:e>b>c>a>d
C.c、d、e处的水溶液中的水的电离平衡一定被抑制
D.a点时,将pH=2的硫酸溶液与pH=12的KOH溶液等体积混合后,溶液显碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列所示的图像能反映相对应实验的是

A.向pH=13的NaOH溶液中不断加水稀释
B.向碳酸氢钠溶液中逐滴加入稀盐酸至过量
C.将60℃接近饱和的硝酸钾溶液恒温蒸发水分至有白色晶体析出
D.将足量的金属镁片和锌片分别和等质量、相同质量分数的稀硫酸混合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
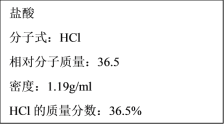
①该浓盐酸的物质的量浓度为___mol·L-1。
②某学生欲用上述浓盐酸和蒸馏水配制480ml物质的量浓度为0.4mol·L-1的稀盐酸,该学生需用量筒量取___mL上述浓盐酸进行配制,所需用的仪器除量筒、烧杯、胶头滴管和玻璃棒之外,还需要___。
(2)KClO3与浓盐酸在一定温度下反应会生成黄绿色的易爆物质二氧化氯,其变化可表述为:KClO3+HCl(浓)―KCl+ClO2↑+Cl2↑+
①请完成该化学方程式(将配平后的完整化学方程式写在答题卡上)___。
②浓盐酸在反应中显示出来的性质是__(填写编号)。
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
③若标况下产生了2.24LCl2,则生成ClO2的质量为__g。
④在KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O中,若标况下产生了6.72LCl2,则转移的电子数目为___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com