
【题目】2005年10月12日北京时间上午9时,中国酒泉卫星发射中心成功将“神舟6号”飞船送入太空,这一壮举又一次受到世界关注.火箭推进器中有强还原剂液体肼(N2H4)和强氧化剂液态双氧水.当它们混合时,即产生大量氮气和水蒸气并放出大量热.已知:0.4mol液态肼与足量的液态双氧水反应生成氮气和水蒸气,放出256.652kJ的热量.
(1)反应的热化学方程
(2)又已知H2O(l)=H2O(g)△H=44kJ.mol﹣1 . 则16g液态肼与足量的液态双氧水反应生成氮气和液态水时放出的热量是kJ.
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外还有一个很大优点是 .
(4)燃料电池在航天器得到大量应用;科研人员新近开发出一种由甲醇、氧气以及强碱作电解质溶液的新型手机电池,充电一次可供手机连续使用一个月,据此请回答以下问题:
①甲醇是极,电极反应
②电池反应的离子方程式为 .
【答案】
(1)N2H4(g)+2H2O2(l)=N2(g)+4H2O(g)△H=﹣641.63kJ/mol
(2)408.815
(3)产物无污染
(4)负;CH3OH+8OH﹣﹣6e﹣═CO32﹣+6H2O;2CH3OH+3O2+4OH﹣═2CO32﹣+6H2O
【解析】解:(1)反应方程式为:N2H4+2H2O2═N2+4H2O,0.4mol液态肼放出256.652KJ的热量,则1mol液态肼放出的热量为 ![]() =641.63kJ,所以反应的热化学方程式为:N2H4(g)+2H2O2(l)═N2(g)+4H2O(g)△H=﹣641.63kJ/mol,
=641.63kJ,所以反应的热化学方程式为:N2H4(g)+2H2O2(l)═N2(g)+4H2O(g)△H=﹣641.63kJ/mol,
故答案为:N2H4(g)+2H2O2(l)=N2(g)+4H2O(g)△H=﹣641.63kJ/mol;(2)①N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=﹣641.63kJ/mol;②H2O(g)=H2O(l)△H=﹣44kJ/mol;
依据盖斯定律①+②×4得到:N2H4(l)+2H2O2(l)═N2(g)+4H2O(l);△H=﹣817.63kJ/mol;
热化学方程式中32g全部反应放热817.63kJ,16g液态肼与足量双氧水反应生成氮气和液态水时,放出的热量为:817.63kJ× ![]() =408.815kJ,
=408.815kJ,
故答案为:408.815;(3)还原剂肼(N2H4)和强氧化剂H2O2 , 当它们混合时,即产生大量的氮气和水蒸气,除释放大量热量和快速产生大量气体外,还有很突出的优点是,产物为氮气和水,清洁无污染,
故答案为:产物无污染;(4)CH3OH和O2在电池中,肯定是O2氧化CH3OH,CH3OH是负极反应物,O2是正极反应物.CH3OH被氧化生成CO2和H2O,电解质溶液中有强碱(OH﹣),CO2要转化CO32﹣ .
①甲醇是负极,电极反应式为:CH3OH+8OH﹣﹣6e﹣═CO32﹣+6H2O,故答案为:负;CH3OH+8OH﹣﹣6e﹣═CO32﹣+6H2O;
②CH3OH被氧化生成CO2和H2O,电解质溶液中有强碱(OH﹣),则CO2要转化CO32﹣ , 电池反应为:2CH3OH+3O2+4OH﹣═2CO32﹣+6H2O,
故答案为:2CH3OH+3O2+4OH﹣═2CO32﹣+6H2O.
(1)反应方程式为:N2H4+2H2O2=N2+4H2O,根据0.4mol液态肼放出的热量,计算1mol液态肼放出的热量,进而写出热化学方程式;(2)根据盖斯定律合并写出生成液态水时的热化学方程式进行计算;(3)依据反应N2H4(g)+2H2O2(l)=N2(g)+4H2O(g)的产物是氮气和水分析该反应的优点;(4)甲醇燃料电池放电时,C元素的化合价升高,所以甲醇所在电极为原电池的负极,O元素的化合价降低,所以通入氧气的极为原电池的正极,负极上发生氧化反应,正极上发生还原反应,以此来解答.


科目:高中化学 来源: 题型:
【题目】一定温度下,在冰醋酸加水稀释的过程中,溶液的导电能力(I)随着加入水的体积V变化的曲线如图所示.下列说法正确的是( ) 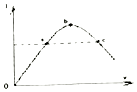
A.a、c两点pH不同
B.向c溶液中加水,溶液中所有离子浓度都减小
C.误用湿润的pH试纸测b点pH结果偏大
D.![]() b点大于c点
b点大于c点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向用盐酸酸化的MgCl2、FeCl3混合溶液中逐滴滴入NaOH溶液,生成的沉淀质量与滴入NaOH溶液体积关系如图,则原混合溶液中MgCl2与FeCl3的物质的量之比为

A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】50 mL 0.50 mol/L盐酸与50 mL 0.55 mol/L NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热,回答下列问题:
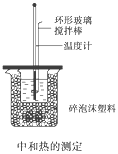
(1)烧杯间填满碎泡沫塑料的作用是_________________________________。
(2)大烧杯上如不盖硬纸板,求得的中和热数值________(填“偏大”“偏小”“无影响”)。
(3)实验中改用60 mL 0.50 mol·L-1盐酸进行反应,与上述实验相比,所放出的热量________(填“相等”、“不相等”),所求中和热__________(填“相等”、“不相等”),简述理由_________________。
(4)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会________(填“偏大”、“偏小”“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1g氢气燃烧生成液态水放出142.9kJ的热量,表示该反应的热化学方程式正确的是( )
A.2H2(g)+O2(g)═2H2O(l)△H=﹣142.9 kJmol﹣1
B.H2(g)+ ![]() O2(g)═H2O(l)△H=﹣285.8 kJmol﹣1
O2(g)═H2O(l)△H=﹣285.8 kJmol﹣1
C.2H2+O2═2H2O△H=571.6 kJmol﹣1
D.H2(g)+ ![]() O2(g)═H2O(g)△H=﹣285.8 kJmol﹣1
O2(g)═H2O(g)△H=﹣285.8 kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在1×105 Pa、298 K条件下,2 mol氢气燃烧生成水蒸气,放出484 kJ热量,下列热化学方程式正确的是( )
A. H2O(g)===H2(g)+![]() O2(g) ΔH=+242 kJ·mol-1
O2(g) ΔH=+242 kJ·mol-1
B. 2H2(g)+O2(g)===2H2O(l) ΔH=-484 kJ·mol-1
C. H2(g)+![]() O2(g)===H2O(g) ΔH=+242 kJ·mol-1
O2(g)===H2O(g) ΔH=+242 kJ·mol-1
D. 2H2(g)+O2(g)===2H2O(g) ΔH=+484 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁是应用最广泛的金属,铁的卤化物、氧化物、硫酸盐以及高价铁的含氧酸盐均为重要化合物。
(1)在实验室中,FeCl2 可用铁粉和盐酸反应制备,FeCl3可用铁粉和_____反应制备: 现有一含FeCl2和FeCl3的混合物的样品,测得样品中n(Fe):n(Cl) = 1:2.3,则该样品中FeCl3的物质的量分数为____________。
(2)高温下,Fe 与水蒸气反应的化学方程式为____________________。
(3)硫酸亚铁、氯化亚铁溶液存放在实验室均易变质,出现红褐色沉淀,且溶液变棕黄色,则此反应的离子方程式为____________________。
(4)在氯化亚铁溶液中加入等物质的量的过氧化钠,发生反应的总的离子方程式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法在一定条件下可以实现的是( )
①酸性氧化物与酸发生反应 ②没有电子转移的氧化还原反应 ③没有水生成,也没有沉淀和气体生成的复分解反应 ④两种酸溶液充分反应后的溶液体系为中性 ⑤有单质参加的非氧化还原反应
⑥通过单质化合形成FeCl2
A. ①③④⑤ B. ②④⑤
C. ①②③⑤⑥ D. ③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列方程式表达正确的是
A. 碳酸钡跟醋酸反应:CO32-+2CH3COOH=2CH3COO-+CO2↑+H2O
B. NH4Cl溶液中加入NaOH溶液加热:NH4++0H-![]() NH3↑+H2O
NH3↑+H2O
C. 硫酸溶液和氢氧化钡溶液反应:Ba2++SO42-=BaSO4↓
D. 将Na投入到CuSO4溶液中:2Na+Cu2+=2Na++Cu↓
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com