
������1785�꣬���ĵ����ڲⶨ�������ʱ����ȥ�����е�O2��N2����֪������������������һ��������������1/200��С���ݡ�?
��1892�꣬�����ڲⶨ�����ܶ�ʱ���ӿ����еõ��ĵ����ܶ�Ϊ1.257 2 g��L-1�����Ӱ��ֽ�õ��ĵ����ܶ�Ϊ1.250 8 g��L-1���������0.006 4 g��L-1��?
����������ķ����ͬ�о�����Ϊ����������ʵ���еġ�С��������ij�ֱ�Ȼ����ϵ����Ԥ������к���ij�ֽ��ص�δ֪���塣������ʵ�飬�������ڷ����˻�ѧ���ʼ������õĶ������塪��벡�?
������������⣺?
��1����������ͨ��ͼ15-1 a��dװ��ʱ�����γ�ȥ��������(����)?
A.O2��N2��H2O��CO2������ B.CO2��H2O��O2��N2?
C.H2O��CO2��N2��O2 D.N2��O2��CO2��H2O?
?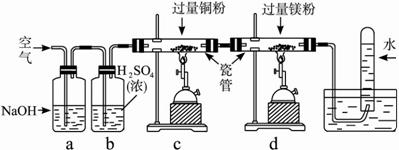
ͼ15-1
��2�����Ϣ٢��еġ�С���Բⶨ������ɺ͵����ܶȵ�ʵ������� �����Ҫ���ء���Ҫ���ء�����?
��3�����Ϣ��п�ѧ��ץס�ˡ�С��������ش���˵����������������������������������������?
 ����ѧ����ϵ�д�
����ѧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
 Fe3+��ת����A��Fe2+��
Fe3+��ת����A��Fe2+���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| �� | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| �� | �� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com