
【题目】一种生产聚苯乙烯的流程如下,下列叙述不正确的是

A.①是加成反应
B.乙苯和氢气加成后的产物的一氯代物有5种
C.鉴别乙苯与聚苯乙烯不可用Br2的四氯化碳溶液
D.乙烯和聚苯乙烯均可以和H2 发生加成反应
科目:高中化学 来源: 题型:
【题目】下列实验能达到实验目的的是______ 。
序号 | 实验内容 | 实验目的 |
A | 盛有 | 探究浓度对反应速率的影响 |
B | 用石墨电极电解 | 比较确定铜和镁的金属活动性强弱 |
C | 在容积可变的密闭容器中发生反应:2NO2(g) | 正反应速率加快,逆反应速率减慢 |
D | 向2支试管中各加入相同体积、相同浓度的 | 探究温度对反应速率的影响 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T ℃时,在0.5 L的密闭容器中,气体A与气体B反应生成气体C,反应过程中A、B、C的浓度变化如图所示。则下列结论正确的是

A. 10 s时反应生成了0.2 mol C
B. 该反应进行到10 s时,消耗了0.2 molA
C. 该反应的化学方程式为3A+B![]() 2C
2C
D. 10 s内用B表示的反应速率为0.01 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2-丁烯是一种重要的有机化工原料。回答下列问题:
(1)已知2-丁烯有顺、反两种同分异构体,可表示为顺![]() 、反
、反![]() 。一定条件下,它们分别发生加成反应的热化学方程式为:
。一定条件下,它们分别发生加成反应的热化学方程式为:
①顺![]() :
:
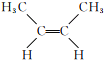
![]() 。
。
②反![]() :
:
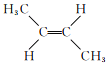
![]()
相同条件下,两种气体之间存在如下转化:
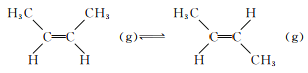
该反应的△H=________。下列叙述中,能表明该反应已达到平衡状态的是________(填序号)。
a.顺-C4H8的含量保持不变
b.混合气体的平均摩尔质量保持不变
c.混合气体中碳的质量分数保持不变
达到平衡后,若要进一步提高体系中反-C4H8的含量,可采取的措施是___________________________。
(2)2-丁烯与氯气反应时,一般用镍作催化剂。镍具有优良的物理和化学特性,是许多领域尤其是高科技产业的重要原料。
①羰基法提纯粗镍涉及的两步反应依次为:
Ⅰ.Ni(s)+4CO(g) ![]() Ni(CO)4(g) △H<0
Ni(CO)4(g) △H<0
Ⅱ.Ni(CO)4(g) ![]() Ni(s)+4CO(g)
Ni(s)+4CO(g)
则下图中能反映出羰基法提纯粗镍过程中能量变化的是________。

②一定条件下,在2L密闭容器中制备Ni(CO)4,粗镍(所含杂质不与CO反应)剩余质量和反应时间的关系如图所示。Ni(CO)4在0~10min的平均反应速率为________mol/(L·min)。
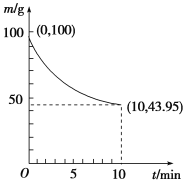
③若反应Ⅱ达到平衡后,保持其他条件不变,降低温度,重新达到平衡时________(填序号)。
a.平衡常数K增大 b.CO的浓度减小 c.v逆[Ni(CO)4]增大
④设计简单实验方案用羰基法提纯粗镍:将粗镍粉末装入玻璃管一端,抽真空后充入CO并封管,______________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种化合物的结构如图所示,其中X、Y、Z、Q、W为原子序数依次增大的五种短周期元素,Q核外最外层电子数与Y核外电子总数相同,X的原子半径是元素周期表中最小的。下列叙述正确的是
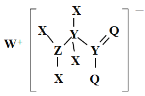
A.Z的最高价氧化物对应的水化物是一元强酸
B.WX的水溶液呈中性
C.元素非金属性的顺序为Y>Z>Q
D.该化合物中与Y单键相连的Q不满足8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一直反应:2NO2(红棕色)![]() N2O4(无色) △H<0,在100℃时,将0.40mol NO2气体充入2L密闭容器中,每隔一段时间对该容器的物质进行测量,得到的数据如下表:
N2O4(无色) △H<0,在100℃时,将0.40mol NO2气体充入2L密闭容器中,每隔一段时间对该容器的物质进行测量,得到的数据如下表:
时间/s n/mol | 0 | 20 | 40 | 60 | 80 | 100 |
n(NO2) | 0.40 | a | 0.26 | c | d | e |
n(N2O4) | 0.00 | 0.05 | b | 0.08 | 0.08 | 0.08 |
(1)a、b、c、d、e中属于平衡状态的是_____________,100s后降低反应混合物的温度,混合气体的颜色_________(填“变浅”、“变深”或“不变”)。
(2)20~40s内,v(NO2)=__________mol/(L·s),100℃时该反应的平衡常数K =_____________。
(3)将一定量的NO2充入密闭注射器中,图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是______________

A.b点的操作是压缩注射器
B.c点与a点相比,c(NO2)增大,c(N2O4)减小
C.若密闭注射器为绝热容器,则T(b)>T(c)
D.d点时v(正)>v(逆)
(4)能说明反应2NO2(红棕色)![]() N2O4(无色)达平衡的是_________
N2O4(无色)达平衡的是_________
A. 体系的颜色不变
B. 恒容条件下,气体的额密度不变
C. 2v正(NO2)=v逆(N2O4)/p>
D. 混合气体的平均摩尔质量不变
(5)100℃时,容器中物质的量的变化曲线如图,请画出80℃时物质的量的变化曲线并进行适当标注。______

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.某有机物结构如图所示,  它的结构最多有_______种
它的结构最多有_______种
II.已知:苯的同系物中,与苯环直接相连的碳原子上有氢原子,就能被酸性高锰酸钾溶液氧化,生成芳香酸,反应如下:

现有苯的同系物甲、乙、丙,分子式都是C10H14,完成以下空格:
(1)甲不能被酸性高锰酸钾溶液氧化为芳香酸,它的结构简式是 ______________________;
(2)乙能被酸性高锰酸钾溶液氧化成分子式为C9H6O6的芳香酸,则乙可能的结构有 ___种。
(3)丙苯环上的一溴代物只有一种。试写出丙可能的结构简式(写至少2种)____________________、______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图装置中:b电极用金属M制成,a、c、d为石墨电极,接通电源,金属M沉积于b极,b为阴极。同时a、d电极上产生气泡。试回答

(1)a连接电源的___极。b极的电极反应式为______。
(2)电解开始时,在B烧杯的中央,滴几滴淀粉溶液,你能观察到的现象是:___________。此时C极上的电极反应式为:_________。
(3)当d极上收集到44.8mL气体(标准状况)时停止电解,a极上的电极反应式为___________,若在b电极上沉积金属M的质量为0.432g,则此金属的摩尔质量为 ______ 。
(4)电解停止后加蒸馏水使A烧杯中的溶液体积仍为200mL。取该溶液逐滴加入到25.0mL0.1mol/L HCl溶液中,当加入25.00mL这种溶液时刚好沉淀完全。试计算电解前A烧杯中MNO3溶液的物质的量浓度为____________?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2H2O2(1)=2H2O(1)+O2(g)反应过程中的能量变化曲线如图所示,下列说法不正确的是

A. 该反应的△H<0,△S>0
B. 途径Ⅱ与途径I相比,可能是加了催化剂
C. 其他条件相同时,产生相同体积的氧气时放出的热量:途径I >途径Ⅱ
D. 其他条件相同时,产生相同体积的氧气所需的时间:途径I>途径Ⅱ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com