
【题目】某酸性废液含有H+、Fe3+、Ni2+、NO3—、F-和Cr2O72-等。下图是该废液的综合利用工艺流程:(假设: F—与金属离子的络合反应不影响其它反应和计算)
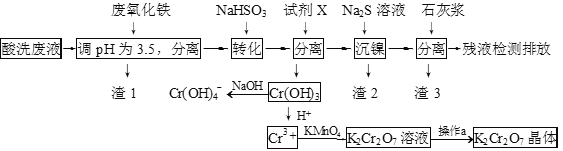
已知:金属离子开始沉淀和沉淀完全时的pH:
Fe3+ | Ni2+ | Cr3+ | |
开始沉淀 | 1.5 | 6.7 | 4.0 |
沉淀完全 | 3.4 | 9.5 | 6.9 |
Ni2+与足量氨水的反应为:Ni2++6NH3 ![]() [Ni(NH3)6]2+([Ni(NH3)6]2+为难电离的络合离子)
[Ni(NH3)6]2+([Ni(NH3)6]2+为难电离的络合离子)
(1)滤渣1的主要成分为:____________。
(2)试剂X可以是足量氨水,还可以是:____________ 。(填序号)
A.Ni(OH)2 B.Cr2O3 C.Fe2O3 D.NaOH
(3)若试剂X是足量氨水,“沉镍”的离子方程式为:____________。
(4)经检测,最后的残液中c(Ca2+)=1.0×10─5 molL-1,则残液中F-浓度____________(填 “符合”或“不符合”)排放标准[已知Ksp(CaF2)=4×10-11,国家排放标准要求氟离子浓度小于10 mgL─1]。
(5)镍(Ni)及其化合物广泛应用于生产电池、电镀和催化剂等领域。
①某蓄电池反应为NiO2+Fe+2H2O![]() Fe(OH)2+Ni(OH)2,放电时若外电路中转移0.6mol电子则正极增重____g。
Fe(OH)2+Ni(OH)2,放电时若外电路中转移0.6mol电子则正极增重____g。
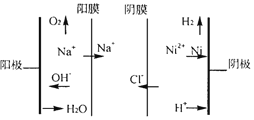
②图为双膜三室电解法处理含镍废水回收金属镍的原理示意图,阳极的电极反应式为____;电解过程中,需要控制溶液pH值为4左右,原因是_______。
【答案】Fe(OH)3 A [Ni(NH3)6]2++S2-=NiS↓+6NH3 不符合 0.6 4OH--4e-=2H2O + O2↑ pH过高时Ni2+会形成氢氧化物沉淀,pH过低时会有氢气析出,降低镍的回收率
【解析】
某酸性废液含有![]() 和
和![]() 等,在溶液中加入废氧化铁调节溶液PH=3.5,使铁离子全部沉淀,过滤得到滤渣1,滤液中加入
等,在溶液中加入废氧化铁调节溶液PH=3.5,使铁离子全部沉淀,过滤得到滤渣1,滤液中加入![]() 与
与![]() 发生反应生成铬离子,加碱沉淀铬离子形成氢氧化铬沉淀,过滤后的滤液中加入
发生反应生成铬离子,加碱沉淀铬离子形成氢氧化铬沉淀,过滤后的滤液中加入![]() 沉淀镍,过滤得到滤液中加入石灰浆沉淀得到滤渣3含有:
沉淀镍,过滤得到滤液中加入石灰浆沉淀得到滤渣3含有:![]() 和
和![]() ,氢氧化铬沉淀加酸生成铬离子,高锰酸钾将铬离子氧化为重铬酸根,结晶得到重铬酸钾晶体。
,氢氧化铬沉淀加酸生成铬离子,高锰酸钾将铬离子氧化为重铬酸根,结晶得到重铬酸钾晶体。
(1)调节溶液PH=3.5,使铁离子全部沉淀,滤渣1为![]() ,故答案为:
,故答案为:![]() ;
;
(2)据金属离子开始沉淀和沉淀完全时的pH分析,又不引入新杂质可知还可以是![]() ,故答案为:A;
,故答案为:A;
(3)若试剂X是足量氨水,![]() 与足量氨水的反应为:
与足量氨水的反应为:![]() ,加入
,加入![]() 会生成更难溶的
会生成更难溶的![]() ,“沉镍”的离子方程式为:
,“沉镍”的离子方程式为:![]() ,故答案为:
,故答案为:![]() ;
;
(4)依据溶度积常数计算F-离子浓度,![]() ,残液中
,残液中![]() ,则
,则![]()
![]() ,依据国家排放标准要求氟离子浓度小于10mgL-1分析判断,不符合国家标准,故答案为:不符合;
,依据国家排放标准要求氟离子浓度小于10mgL-1分析判断,不符合国家标准,故答案为:不符合;
(5)①![]() ,根据方程式分析正极电极反应式为:
,根据方程式分析正极电极反应式为:![]() ,转移2mol电子电极质量增加2g,故转移0.6mol电子则正极增重0.6g;故答案为:0.6;
,转移2mol电子电极质量增加2g,故转移0.6mol电子则正极增重0.6g;故答案为:0.6;
②根据图像可知,阳极氢氧根放电生成氧气,故电极反应式为:![]() ;电解过程中pH太高镍离子会沉淀,pH太低则阴极氢离子会放电生成氢气,故需要控制溶液pH值为4左右,故答案为:
;电解过程中pH太高镍离子会沉淀,pH太低则阴极氢离子会放电生成氢气,故需要控制溶液pH值为4左右,故答案为:![]() ;pH过高时
;pH过高时![]() 会形成氢氧化物沉淀,pH过低时会有氢气析出,降低镍的回收率。
会形成氢氧化物沉淀,pH过低时会有氢气析出,降低镍的回收率。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某溶液X中可能含有NO3-、Cl-、SO42-、CO32-、NH4+、Fe2+和Fe3+中的几种,且所含阴离子的物质的量相等。为确定该溶液X的成分,某学习小组做了如下实验:

则下列说法正确的是
A. 若含有Fe3+,则一定含有Cl-
B. SO42-、NH4+一定存在,Fe2+和Fe3+可能都存在
C. 该溶液中只存在上述离子中的NO3-、SO42-、NH4+、Fe2+四种离子
D. 气体甲能使湿润的蓝色石蕊试纸变红
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现代膜技术可使某种离子具有单向通过能力,常用于电解池、原电池中。电解NaB(OH)4溶液可制备H3BO3,其工作原理如图。下列叙述错误的是( )
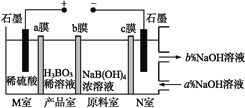
A. M室发生的电极反应式:2H2O-4e-![]() O2↑+4H+
O2↑+4H+
B. N室:a<b
C. 产品室发生的反应是B(OH)4- +H+![]() H3BO3+H2O
H3BO3+H2O
D. 理论上每生成1 mol产品,阴极室可生成标准状况下5.6 L气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LED产品的使用为城市增添色彩。下图是氢氧燃料电池驱动LED发光的一种装置示意图。下列有关叙述正确的是( )
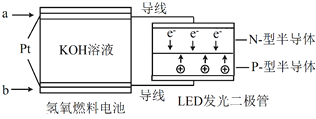
A. 电路中的电子从负极经外电路到正极,再经过KOH溶液回到负极,形成闭合回路
B. a处通入氢气, b处通氧气,该装置将化学能最终转化为电能
C. 电池放电后, OH-的物质的量浓度减小
D. 通入O2的电极发生反应:O2 + 4e- = 2O2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关晶体的结构如图所示,下列说法中不正确的是( )
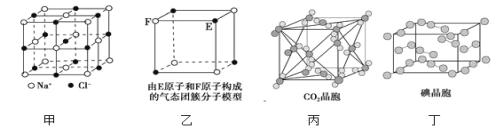
A.在NaCl晶体(图甲)中,距Na+最近的C1-围成正八面体
B.该气态团簇分子(图乙)的分子式为EF或FE
C.在CO2晶体(图丙)中,一个CO2分子周围有12个CO2分子紧邻
D.在碘晶体(图丁)中,存在的作用力有非极性共价键和范德华力
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图A所示的转化关系中(具体反应条件略),a、b、c和d分别为四种短周期元素的常见单质,其余均为它们的化合物,i的溶液为常见的酸,a的一种同素异形体的晶胞如图B所示。
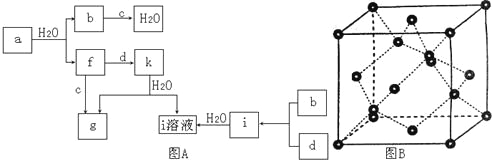
回答下列问题:
(1)图B对应的物质名称是_________,其晶胞中的原子数为______,晶体类型为_______。
(2)d中元素的原子核外电子排布式为_______。
(3)图A中由二种元素组成的物质中,沸点最高的是______,原因是______,该物质的分子构型为_________,中心原子的杂化轨道类型为_________。
(4)图A中的双原子分子中,极性最大的分子是_________。
(5)k的分子式为_________,中心原子的杂化轨道类型为_________,属于_________分子(填“极性”或“非极性”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。
(1)把与下面元素有关性质相符的曲线标号填入相应的空格中:
a. 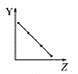 b.
b. 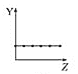 c.
c. 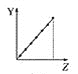 d.
d. 
①第ⅡA族元素的价电子数________。
②第三周期元素的最高化合价________。
③F-、Na+、Mg2+、Al3+的离子半径________。
(2)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3∶4;M元素原子的最外层电子数与电子层数之比为4∶3;N-、Z+、X+的半径逐渐减小;化合物XN常温下为气体。据此回答:
①X为___________(名称),Y为____________(元素符号),Z原子结构示意图为________________。
②N的最高价氧化物的水化物的化学式为________________。
③M的最高价氧化物的化学式为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式不正确的是( )
A. NO2溶于水:3NO2+H2O=2H++2NO3-+NO
B. 漂白粉溶液呈碱性的原因:ClO-+H2O![]() HClO+OH-
HClO+OH-
C. 酸性条件下用H2O2将海带灰中I-氧化:H2O2+2I-+2H+=I2+2H2O
D. 氯化铝溶液中加入过量的氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeBr2是一种黄绿色固体,某学习小组制备并探究它的还原性。
I.实验室制备FeBr2实验室用如图所示装置制取溴化亚铁。其中A为CO2发生装置,D和d中均盛有液溴,E为外套电炉丝的不锈钢管,e是两个耐高温的瓷皿,其中盛有细铁粉。
实验开始时,先将铁粉加热至600—700℃,然后将干燥、纯净的CO2气流通入D中,E管中反应开始。不断将d中液溴滴入温度为100—120℃的D中。经过几小时的连续反应,在铁管的一端沉积有黄绿色鳞片状溴化亚铁。

(1)若在A中盛固体CaCO3,a中盛6 mol/L盐酸。为使导入D中的CO2为干燥纯净的气体,则图中B、C处的装置和其中的试剂应是:B为_____________。C为________________。为防止污染空气,实验时应在F处连接盛___________的尾气吸收装置。
(2)反应过程中要不断通入CO2,其主要作用是____________________。
Ⅱ.探究FeBr2的还原性
(3)实验需要200 mL 0.1 mol/L FeBr2溶液,配制FeBr2溶液除烧杯、量筒、胶头滴管、玻璃棒外,还需要的玻璃仪器是_____________,需称量FeBr2的质量为:_________。
(4)取10 mL上述FeBr2溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:
假设1:Br一被Cl2氧化成Br2溶解在溶液中;
假设2:Fe2+被Cl2氧化成Fe3+
设计实验证明假设2是正确的:________
(5)请用一个离子方程式来证明还原性Fe2+>Br一________:
(6)若在40 mL上述FeBr2溶液中通入3×10-3mol Cl2,则反应的离子方程式为________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com