
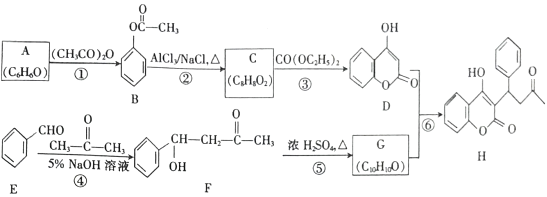
����Ŀ���б�ͪ�㶹��(H)�����ڷ���Ѫ˨˨���Լ���,��ϳ�·����ͼ��ʾ(���ַ�Ӧ������ȥ)��
��֪��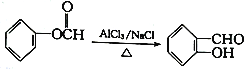
�ش���������:
��1��A��������_________,H �к��������ŵ�������_________ ��
��2����Ӧ�ٵķ�Ӧ������_________,��Ӧ���ķ�Ӧ������_________ ��
��3��C �Ľṹ��ʽΪ_________ ��
��4����Ӧ�ݵĻ�ѧ����ʽΪ_________ ��
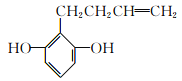
��5��F ��ͬ���칹����,����������������_____��,���к˴Ź���������7���,�ҷ����֮��Ϊ1:2:2:2:2:1:2�Ľṹ��ʽΪ__________��(��дһ��)
�ٷ��ӽṹ�г������ⲻ�����������Ҳ�����
���ܺ�FeCl3��Һ������ɫ��Ӧ
��1mol���л�������2molNaOH ǡ����ȫ��Ӧ
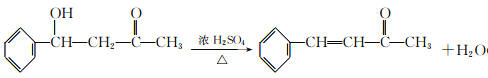
��6�������б�ͪ�㶹�صĺϳ�·�ߣ����һ����E����ȩΪԭ��(�������Լ���ѡ)�Ʊ�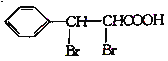 �ĺϳ�·�ߡ�_____________
�ĺϳ�·�ߡ�_____________
���𰸡� ���� �ǻ����������ʻ� ȡ����Ӧ �ӳɷ�Ӧ 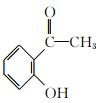
 6
6 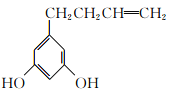 ����
���� ��
�� 
��������A�ķ���ʽΪC6H6O���������ͼ��A�к��б�������AΪ����(![]() )���������������·�Ӧ����B(
)���������������·�Ӧ����B( )��B���Ȼ������Ȼ��������·�Ӧ����C(C8H8O2)��������֪������CΪ
)��B���Ȼ������Ȼ��������·�Ӧ����C(C8H8O2)��������֪������CΪ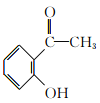 ��C��̼���������Ӧ����D(
��C��̼���������Ӧ����D(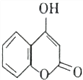 )������G�ķ���ʽ���H��D�Ľṹ��֪��GΪ
)������G�ķ���ʽ���H��D�Ľṹ��֪��GΪ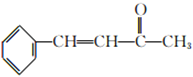 ��
��
(1)A�DZ��ӣ�H�к������������ǻ����������ʻ����ʴ�Ϊ�����ӣ��ǻ����������ʻ���
(2)����A��B�Ľṹ����Ӧ��Ϊȡ����Ӧ������E��F�Ľṹ����Ӧ��Ϊ�ӳɷ�Ӧ���ʴ�Ϊ��ȡ����Ӧ���ӳɷ�Ӧ��
(3)��������������C�Ľṹ��ʽΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
(4)��Ӧ����F�����ǻ�����ȥ��Ӧ����Ӧ�Ļ�ѧ����ʽΪ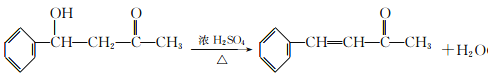 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
(5)FΪ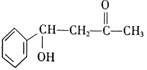 ���ٷ��ӽṹ�г������ⲻ�����������Ҳ����������ܺ�FeCl3��Һ������ɫ��Ӧ��˵�����з��ǻ�����1mol���л�������2molNaOHǡ����ȫ��Ӧ��˵������2�����ǻ������ڲ����ڼ��������IJ���ֻ��Ϊ��CH2CH2CH=CH2�������������У�2�����ǻ�������λ����2�֣�2�����ǻ����ڼ�λ����3�֣�2�����ǻ����ڶ�λ����1�֣���6�֣����к˴Ź���������7���,�ҷ����֮��Ϊ1:2:2:2:2:1:2�Ľṹ��ʽΪ
���ٷ��ӽṹ�г������ⲻ�����������Ҳ����������ܺ�FeCl3��Һ������ɫ��Ӧ��˵�����з��ǻ�����1mol���л�������2molNaOHǡ����ȫ��Ӧ��˵������2�����ǻ������ڲ����ڼ��������IJ���ֻ��Ϊ��CH2CH2CH=CH2�������������У�2�����ǻ�������λ����2�֣�2�����ǻ����ڼ�λ����3�֣�2�����ǻ����ڶ�λ����1�֣���6�֣����к˴Ź���������7���,�ҷ����֮��Ϊ1:2:2:2:2:1:2�Ľṹ��ʽΪ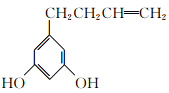 (��
(��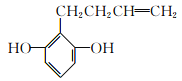 )���ʴ�Ϊ��6��
)���ʴ�Ϊ��6�� (��
(�� )��
)��
(6)��![]() ����ȩΪԭ���Ʊ�
����ȩΪԭ���Ʊ�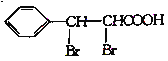 ������E����F��ԭ����������E����ȩ������������Һ�з�Ӧ����
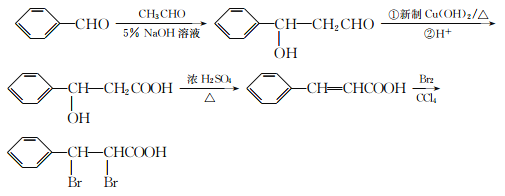
������E����F��ԭ����������E����ȩ������������Һ�з�Ӧ����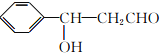 ���ٽ�ȩ������Ϊ�Ȼ�������ǻ���ȥ��������ӳɼ��ɣ��ϳ�·��Ϊ
���ٽ�ȩ������Ϊ�Ȼ�������ǻ���ȥ��������ӳɼ��ɣ��ϳ�·��Ϊ![]()
![]()
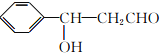
![]()
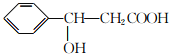
![]()
![]()
![]()
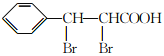 ���ʴ�Ϊ��
���ʴ�Ϊ��![]()
![]()
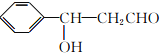
![]()
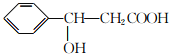
![]()
![]()
![]()
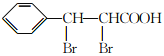 ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ѧ֪ʶ�����Ŀ��
��1��ά����C��һ��ˮ���Ե�ά���أ�ȱ��VC��ʹ�˻���������ȡһƬ����ˮ�����������ϵμӵ�����Һ�͵�ˮ�������� �� ˵������ˮ���к���VC����������VC���������������ԭ�������ʣ�
��2������ѧ�ⶨ������ƽ������65%����̼18%������10%�����Ͼ�Ϊ������������������Ԫ����ԭ����Ŀ����������Ԫ�ط��ţ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ��������Ҫ2.0mol/L��NaCl��Һ950mL�����Ƹ����ʵ���Ũ����Һʱ��Ӧѡ������ƿ�Ĺ��ͳ�ȡNaCl�������ֱ���
A.950mL��111.2gB.500mL��117.0g
C.1000mL��117.0gD.1000mL��111.2g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͬ��������������ȫȼ��ʱ�����������������ǣ�������
A.CH4
B.C2H4
C.C2H6
D.C6H6
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�ϲ������̿�(��Ҫ�ɷ�ΪMnO2)����ȡ������,������������:
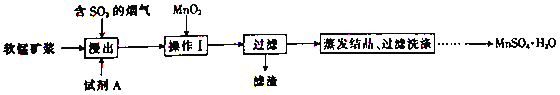
��֪:����Һ�еĽ���������Ҫ��Mn2+,������������Fe2+���ش���������:
��1��ʵ���ҽ��й��˲���ʱ�õ��IJ��������в��������ձ���______��
��2������������Ҫ��Mn2+����ʽ����,д��MnO2��SO2��Ӧ�����ӷ���ʽ:____________��
��3���������̵ĸ���Ӧ֮һ�Dz���SO2������Ϊ����,��ʹ����Һ��pH�½�,�⽫���������̿�������SO2�����������ɵ����ᣬ��ѡ�õ��Լ�A��______(����ĸ)��
A.MnCO3 B.MnO2 C.Mn(OH)2 D.MnSO4
��4������I��Ŀ����__________�͵�����Һ��pH��3��4��������˺����Һ���Ƿ���Fe3+�IJ�����_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ����˵���������ʼ��������ԣ����л�ԭ�Ե��� �� ��
A.SO3B.SC.SO2D.H2S
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڷ�Ӧ2KI+O3+H2O ==2KOH+I2+O2������˵����ȷ����
A������2 molKI������ʱ��2 mol��ԭ�ӱ���ԭ
B��O2�ǻ�ԭ����
C��������2.24 L O3����ת��0.2 mol����
D���������뻹ԭ��������ʵ���֮��Ϊ1:1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ѧ֪ʶ�����Ŀ��
��1��ij�¶�ʱ��ˮ�����ӻ�Kw=1��10��13 �� ����¶�25�棨���������������=�������ڴ��¶��£�ij��Һ����ˮ���������H+Ũ��Ϊ1��10��10 molL��1 �� �����Һ��pH����Ϊ��
��2�����¶�Ϊ25��ʱ�����ΪVa��pH=a��H2SO4�����ΪVb��pH=b��NaOH��ϣ�ǡ���кͣ�����Һ�и������ӵ�Ũ���ɴ�С������˳���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ�ģ� ��
A.SiH4�ķе����CH4 �� ���Ʋ�pH3�ķе����NH3
B.NH ![]() Ϊ�������壬���Ʋ��PH
Ϊ�������壬���Ʋ��PH ![]() ҲΪ��������ṹ
ҲΪ��������ṹ
C.CO2�����Ƿ��Ӿ��壬���Ʋ�SiO2����Ҳ�Ƿ��Ӿ���
D.C2H6��̼��Ϊֱ���͵ķǼ��Է��ӣ����Ʋ�C3H8Ҳ��̼��Ϊֱ���͵ķǼ��Է���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com