
【题目】下列推论正确的( )
A.SiH4的沸点高于CH4 , 可推测pH3的沸点高于NH3
B.NH ![]() 为正四面体,可推测出PH
为正四面体,可推测出PH ![]() 也为正四面体结构
也为正四面体结构
C.CO2晶体是分子晶体,可推测SiO2晶体也是分子晶体
D.C2H6是碳链为直线型的非极性分子,可推测C3H8也是碳链为直线型的非极性分子
【答案】B
【解析】解:A、SiH4和CH4都属于分子晶体,影响分子晶体的沸点高低的因素是分子间作用力的大小,相对分子质量越大,分子间作用力越大,NH3分子间存在氢键,沸点反常偏高大于pH3 , 故A错误;B、N、P是同主族元素,形成的离子NH4+和PH4+结构类似都是正四面体构型,故B正确;
C、CO2是分子晶体,而SiO2是原子晶体,故C错误;
D、C2H6中两个﹣CH3对称,是非极性分子,而C3H8是锯齿形结构,是极性分子,故D错误;
故选B.
【考点精析】关于本题考查的极性分子和非极性分子和氢键的存在对物质性质的影响,需要了解非极性分子中整个分子电荷分布是均匀的、对称的;极性分子中整个分子的电荷分布不均匀,不对称;氢键主要存在于HF、H2O、NH3、CH3CH2OH分子间;故HF、H2O、NH3的沸点分别与同族氢化物沸点相比反常的高才能得出正确答案.


科目:高中化学 来源: 题型:
【题目】苄丙酮香豆素(H)常用于防治血栓栓塞性疾病,其合成路线如图所示(部分反应条件略去)。
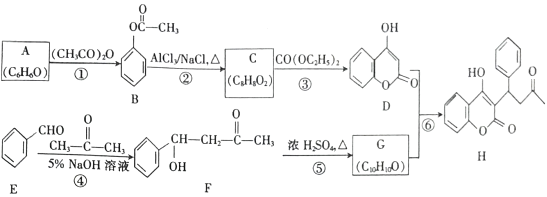
已知: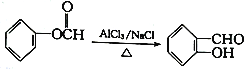
回答下列问题:
(1)A的名称是_________,H 中含氧官能团的名称是_________ 。
(2)反应①的反应类型是_________,反应④的反应类型是_________ 。
(3)C 的结构简式为_________ 。
(4)反应⑤的化学方程式为_________ 。
(5)F 的同分异构体中,满足下列条件的有_____种,其中核磁共振氢谱有7组峰,且峰面积之比为1:2:2:2:2:1:2的结构简式为__________。(任写一种)
①分子结构中除苯环外不含其他环,且不含甲基
②能和FeCl3溶液发生显色反应
③1mol该有机物能与2molNaOH 恰好完全反应
(6)参照苄丙酮香豆素的合成路线,设计一种以E和乙醛为原料(其他无机试剂任选)制备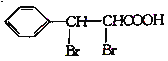 的合成路线。_____________
的合成路线。_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上由黄铜矿(主要成分 CuFeS2)制取 FeSO4·7H2O 和Cu的主要流程如下:

(1)检验酸浸过程中 Fe2+是否被氧化,应选择________(填字母编号)。
A.KMnO4 溶液 B.K3[Fe(CN)6]溶液 C.KSCN 溶液
(2)酸浸过程中主要反应的化学方程式为__________。
(3)某同学向盛有 H2O2 溶液的试管中加入几滴酸化的 FeSO4 溶液,溶液变成棕黄色,发生反应的离子方程式为___________。一段时间后.溶液中有气泡出现,并放热,随后有红褐色沉淀生成;产生气泡的原因是_________,生成沉淀的原因是___________(用平衡移动原理解释)。
(4)已知 25℃时, Ksp[Fe(OH)3]=4.0×10-38, 此温度下,若实验室中配制 2.5mol/L 100 mLFe2(SO4)3 溶液,为使配制过程中不出现浑浊,则至少需要加10mol/L的硫酸______mL(忽略加入硫酸的体积)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌锰电池(俗称干电池)在生活中的用量很大。两种锌锰电池的构造图如图(a)所示。
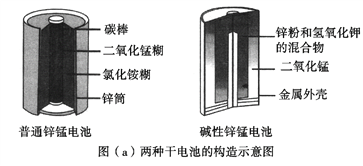
回答下列问题:
(1)普通锌锰电池放电时发生的主要反应为:Zn+2NH4Cl+2MnO2==Zn(NH3)2Cl2+2MnOOH
①该电池中,负极材料主要是________,电解质的主要成分是________,正极发生的主要反应是__________________________。
②与普通锌锰电池相比,碱性锌锰电池的优点有_____________________。(任写一条)
(2)图(b)表示回收利用废旧普通锌锰电池的一种工艺(不考虑废旧电池中实际存在的少量其他金属)。
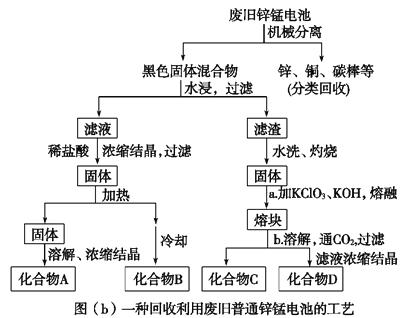
图(b)中产物的化学式分别为A_________________,B______________________。
(3)①操作a中得到熔块的主要成分是K2MnO4。操作b中,绿色的K2MnO4溶液反应后生成紫色溶液D和一种黑褐色固体C,该反应的离子方程式为_________________________。
②采用惰性电极电解K2MnO4溶液也能得到化合物D,则阴极处得到的主要物质是________。(填化学式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,将2 molSO2和1molO2充入 10 L恒容密闭容器中,发生反应:2SO2(g) +O2(g)![]() 2SO3(g) △H=-196 kJ·mol-1。5 min时达到平衡,测得反应放热166.6kJ。下列说法错误的是( )
2SO3(g) △H=-196 kJ·mol-1。5 min时达到平衡,测得反应放热166.6kJ。下列说法错误的是( )
A. 0~5min内,用O2表示的平均反应速率v(O2)=0.017 mol·L-1·min-1
B. ![]() 的值不变时,该反应达到平衡状态
的值不变时,该反应达到平衡状态
C. 若增大O2的浓度,SO2的转化率增大
D. 条件不变,若起始时充入4 molSO2和2 molO2,平衡时放出的热量小于333.2 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E、F、G7种元素,试按下述所给的条件推断:
①A、B、C是同一周期的金属元素,已知原子核外均有3个电子层,A的原子半径在所属周期中最大且原子半径A>B>C;
②D、E是非金属元素,它们跟氢化合可生成气态氢化物HD和HE,在室温时,D的单质是液体,E的单质是固体;
③F的单质在常温下是气体,性质很稳定,是除氢外最轻的气体;
④G是除氢外原子半径最小的主族元素。
(1)A的名称是____________,B位于周期表中第_________周期________族,C的原子结构示意图是________________。
(2)E的单质颜色是____________________。
(3)A元素与D元素形成的化合物的电子式是__________________。
(4)G的单质与水反应的化学方程式是______________________________。
(5)F的元素符号是_____________________。
(6)在上述七种元素中,最高价氧化物对应的水化物碱性最强的是________(填化学式,下同),酸性最强的是_______________,气态氢化物最稳定的是______________。
(7)将C的氧化物对应的水化物投入到A的氧化物对应的水化物中反应的离子方程式是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,将2.0molA(g)和2.0molB(g)充入体积为1L的密闭容器中,在一定条件发生下述反应:A(g)+B(g)![]() 2C(g)+D(s)△H<0;t时刻反应达到平衡时,C(g)为2.0mol。下列说法正确的是
2C(g)+D(s)△H<0;t时刻反应达到平衡时,C(g)为2.0mol。下列说法正确的是
A. t时刻反应达到平衡时,A(g)的体积分数为20%
B. T℃时该反应的化学平衡常数Kc=2
C. t时刻反应达到平衡后,缩小容器体积,平衡逆向移动
D. 相同条件下,若将1.0molA(g)和1.0molB(g)充入同样容器,达到平衡后,A(g)的转化率为50%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法正确的是( )
A. 1.0mol·L-1的CH3COONa溶液中所含CH3COO-的数目一定小于NA
B. 46g二氧化氮(NO2)所含的电子数为23NA
C. 标准状况下,2.24 LCCl4中所含C-Cl键的数目为0.2NA
D. 将0.1mol H2和0.2molI2充入密闭容器中充分反应后,生成HI的分子数为0.2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com