
【题目】常温下,在溶液中可发生如下反应:
①![]()
②![]()
③![]()
根据上述反应提供的信息,判断下列结论不正确的是
A.氧化性:XO4—>B2>A3+
B.X2+既有还原性,又有氧化性
C.还原性:Z—>A2+
D.溶液中可发生:![]()
【答案】C
【解析】
A. 利用氧化还原反应的规律,氧化剂的氧化性强于氧化产物的氧化性,由反应①知,氧化性B2>A3+,由反应③可知,氧化性XO4—>Z2,由反应②可知,氧化性Z2 > B2,则得到氧化性强弱关系:XO4—>Z2 >B2>A3+,A项正确;
B. 反应③中,X 的元素的化合价最高正价为+7,最低价=-(8-最高正价)=-(8-7)=-1则X2+处于中间价态,既有还原性,又有氧化性,故B正确;
C. 还原剂的还原性强于还原产物的还原性,由反应①可知,还原性A+>B-,由反应②可知,还原性B—>Z—,由反应③可知,还原性Z—>X2+,可得到还原性强弱关系:A+>B—>Z—>X2+,得不到Z—> A2+,故C错误;
D. 由①②可知,氧化性Z2 >B2>A3+,可以发生反应![]() ,故D正确;
,故D正确;
答案选C。


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】某温度下,将打磨后的镁条放入盛有![]() 蒸馏水的烧杯中,用pH传感器和浊度传感器监测溶液中的pH和浊度随时间的变化(如图所示,实线表示溶液pH随时间的变化)。下列有关描述不正确的是( )
蒸馏水的烧杯中,用pH传感器和浊度传感器监测溶液中的pH和浊度随时间的变化(如图所示,实线表示溶液pH随时间的变化)。下列有关描述不正确的是( )

A. 该实验是在加热条件下进行的
B. 该温度下![]() 的Ksp的数量级约为
的Ksp的数量级约为![]()
C. 50s时,向溶液中滴入酚酞试液,溶液仍为无色
D. 150s后溶液浊度下降是因为生成的![]() 逐渐溶解
逐渐溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究实验室制乙烯及乙烯和溴水的加成反应:甲同学设计了如图所示的实验装置,并进行了实验。当温度升至170℃左右时,有大量气体产生,产生的气体通入溴水中,溴水的颜色迅速褪去。甲同学认为达到了实验目的。乙同学仔细观察了甲同学的整个实验过程,发现当温度升到100℃左右时,无色液体开始变色,到160℃左右时,混合液全呈黑色,在170℃超过后生成气体速度明显加快,生成的气体有刺激性气味。由此他推出,产生的气体中应有杂质,可能影响乙烯的检出,必须除去。据此回答下列问题:

(1)写出甲同学实验中认为达到实验目的的两个反应的化学方程式:__________________。
(2)乙同学观察到的黑色物质是__________,刺激性气体是__________。乙同学认为刺激性气体的存在就不能认为溴水褪色是乙烯的加成反应造成的。原因是(用化学方程表示):________________________________ 。
(3)丙同学根据甲乙同学的分析,认为还可能有CO、CO2两种气体产生。为证明CO存在,他设计了如下过程(该过程可把实验中产生的有机产物除净):发现最后气体经点燃是蓝色火焰,确认有一氧化碳。
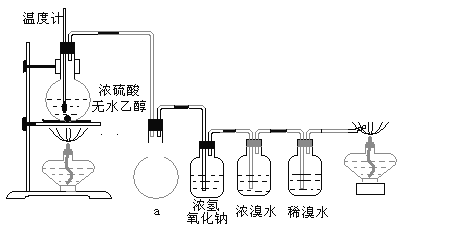
①设计装置a的作用是_____________________________________________
②浓溴水的作用是_________________________________________________,
稀溴水的作用是___________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实所对应的离子方程式正确的是
选项 | 事实 | 离子方程式 |
A | 向酸性 |
|
B | 硫代硫酸钠溶液中滴加盐酸,有淡黄色沉淀产生 |
|
C | 明矾溶液中加入 |
|
D | 碘化亚铁溶液中滴加少量溴水,溶液变为黄色 |
|
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室制取纯净、干燥的氯气,并验证氯气性质的装置。其中E瓶放有干燥红色布条;F中为红色的铜网,其右端出气管口放有脱脂棉。
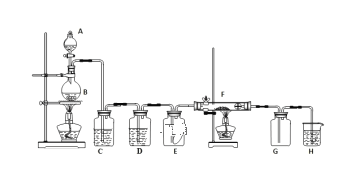
(1)装置C中盛装的溶液是___,D中试剂的作用是___。
(2)写出F中反应的化学反应方程式:__ ,其反应现象为___。
(3)H中的试剂为____,用来吸收多余氯气。该反应的离子方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验操作和现象能得出相应结论的是
选项 | 实验操作 | 现象 | 结论 |
A |
| 溶液红色褪去 |
|
B | 向1mL 2mol/L | 先生成白色沉淀,后生成红褐色沉淀 |
|
C | 将 | 溶液变为红色 | 样品已部分或全部变质 |
D | 无水乙醇中加入浓硫酸,加热,产生的气体Y通入酸性 | 溶液紫色褪去 | 气体Y中含有乙烯 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阅读下列材料后回答有关问题
一个体重50kg的健康人,体内含铁元素2g,这2g铁元素以Fe2+和Fe3+的形式存在。Fe2+易被吸收,所以给贫血者补充铁时,应补充含Fe2+的亚铁盐(如FeSO4),服用维生素C可使食物中的Fe转化成Fe2+,有利于人体对铁的吸收
(1)人体中经常进行Fe2+与Fe3+的转化,在此转化过程中,Fe2+作_______剂(填氧化或还原,下同),被__________
(2)“服用维生素C可使食物中的Fe3+转化为Fe2+这句话说明,维生素C在这个反应中作____剂(填氧化或还原,下同),具有_______性
(3)补血剂的主要成分是FeSO4请写出产物有FeSO4的符合要求的化学方程式:
①置换反应:__________________________
②复分解反应:__________________________
(4)有人在研究硫酸亚铁(FeSO4)热稳定性时,作出了两种假设
①假设它按CaCO3受热分解的方式分解,反应的化学方程式为_________________________
②假设它按KClO3受热分解的方式分解,已知产物都是氧化物,其中有两种酸性氧化物生成,则分解反应的化学方程式为____________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应实验,能达到实验目的是( )
A. 用 所示装置分离CCl4和I2的混合物
所示装置分离CCl4和I2的混合物
B. 用 所示装置获取少量SO2气体
所示装置获取少量SO2气体
C. 用 所示装置除去CO2气体中的少量SO2
所示装置除去CO2气体中的少量SO2
D. 用 所示装置蒸发NaCl溶液获得NaCl晶体
所示装置蒸发NaCl溶液获得NaCl晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组利用如图装置进行铁与水蒸气反应的实验,并检验产物的性质,请回答下列问题:
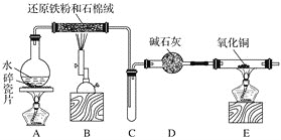
(1)A装置的作用是____________,烧瓶底部放碎瓷片的作用是_____________。
(2)装置B中发生反应的化学方程式是____________________________________,该反应中氧化剂是__________,氧化产物是_____________。
(3)D的作用是____________________________。
(4)E中的实验现象是_____________________。
(5)该同学对反应后硬质试管中固体物质的组成提出了如下假设:
假设1:只有Fe;
假设2:只有________;
假设3:既有Fe也有Fe3O4。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com