
【题目】短周期元素W、X、Y、Z的原子序数依次增加,由这些元素组成的常见物质的转化关系如下图,其中a、b、d、g为化合物,a为淡黄色固体,c是Z的单质,该单质与沸水缓慢反应,且该单质可制造照明弹;f为固体单质。下列有关说法正确的是

A. 简单离子的半径:Y>Z>X B. 元素的非金属性:W>X
C. 最高价氧化物对应水化物的碱性:Y>Z D. X、Y两种元素组成的化合物只含离子键
【答案】C
【解析】试题分析: a、b、d、g为化合物,a为淡黄色固体,则a为过氧化钠;c是Z的单质,该单质与沸水缓慢反应,且该单质可制造照明弹,则Z为镁元素;由这些元素组成的常见物质的转化关系可知,若f为固体单质,则b为二氧化碳、f为碳、e为氧气、d为碳酸钠、g为氧化镁。短周期元素W、X、Y、Z的原子序数依次增加,则其分别为C、O、Na、Mg。A. 电子层结构相同的离子,核电荷数越大的半径越小,所以简单离子的半径X>Y>Z,A不正确; B. 元素的非金属性为O >C,B不正确;C. Na的金属性强于Mg,故其最高价氧化物对应水化物的碱性较强,C正确;D. X、Y两种元素组成的化合物有氧化钠和过氧化钠,其中氧化钠只含离子键、过氧化钠既有离子键又有共价键,D不正确。本题选C。


科目:高中化学 来源: 题型:
【题目】在2L的密闭容器中,发生反应:C(s)+H2O(g)![]() CO(g)+H2(g)+131.5kJ,5min后达到平衡,固体减少了24g,则
CO(g)+H2(g)+131.5kJ,5min后达到平衡,固体减少了24g,则
A.ρ气体不变时反应达到平衡状态B.v正(CO)为2.4mol/(Lmin)
C.若容器体积缩小,平衡常数减小D.增大C的量,平衡右移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】抗癌药物乐伐替尼中间体M的合成路线如下:
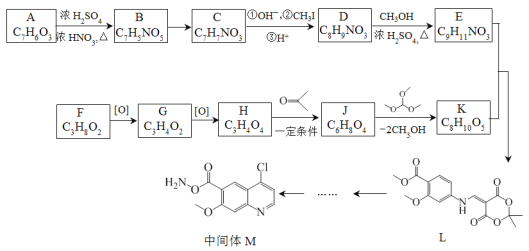
已知:
i. ![]()
![]()
![]() (R代表烃基)
(R代表烃基)
ii. 有机物结构可用键线式表示,如(CH3O)3CH的键线式为![]()
(1)A中含有苯环,两个取代基处于邻位,A中含有的官能团名称是 _______。血液中A的浓度过高能使人中毒,可静脉滴注NaHCO3溶液解毒。A与NaHCO3反应的化学方程式是_______。
(2)B生成C的过程中,B发生了_____(填“氧化”或“还原”)反应。
(3)D生成E的化学方程式是________。
(4)写出符合下列条件的D的其中一种同分异构体的结构简式________。
①分子中含有硝基且直接连在苯环上
②核磁共振氢谱图显示苯环上有两种化学环境相同的氢原子
③不能与FeCl3溶液发生显色反应
(5)F的核磁共振氢谱图中有三组峰,峰面积之比为2:1:1,F生成G的化学方程式是_____。
(6)H生成J的化学方程式是_______。
(7)已知E+K→L+CH3OH,K的结构简式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuSO4是一种重要的化工原料,其有关制备途径如图所示。下列说法正确的是

A. 途径①所用混酸中H2SO4与HNO3物质的量之比最好为2∶3
B. 利用途径③制备16g硫酸铜,消耗硫酸的物质的量为0.1mol
C. 生成等量的硫酸铜,三个途径中参加反应的硫酸的物质的量:①=②=③
D. 与途径①、③相比,途径②更好地体现了绿色化学思想
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卡托普利(E)是一种血管紧张素转化酶抑制剂,被应用于治疗高血压和某些类型的充血性心力衰竭。合成路线如下:
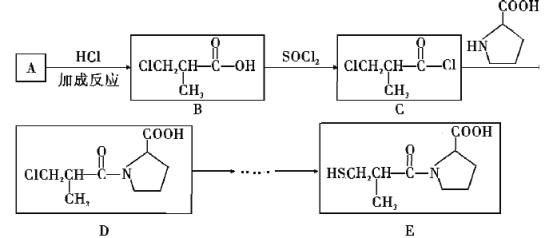
(1) A中官能团的名称是______________,A→B反应方程式为_______________。C→D的反应类型是_________________。
(2)1molD与NaOH溶液反应,最多消耗__________NaOH
(3)卡托普利E的分子中有_____个手性碳原子,下列关于E说法不正确的是______。
a.卡托普利的水溶液呈酸性 b.在氧气中充分燃烧的产物中含有SO2
c.E的分子式为C9H16NO3S d.E存在属于芳香族化合物的同分异构体
(4)A与浓硫酸、甲醇反应生成M,M的同分异构体在核磁共振氢谱图中出现两种信号峰、且只有一种官能团,该同分异构体可能结构为_________、_________。M加聚反应生成高分子化合物N的方程式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组在实验室中利用如图装置(夹持装置略去)测定某铁硫化物(FexSy)的组成,并探究反应后D装置所得溶液中含硫化合物的组成。
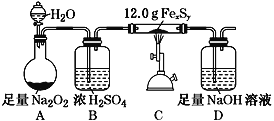
实验步骤:
步骤Ⅰ如图连接装置,检查装置气密性,装入试剂;
步骤Ⅱ旋开分液漏斗活塞与旋塞,并点燃酒精喷灯;
步骤Ⅲ足够长时间后,D中产生气泡速率变快时,停止加热,继续向烧瓶中滴水一段时间
步骤Ⅳ实验结束后,将D中所得溶液加水配制成250mL溶液;
……
请回答:
(1)步骤Ⅲ中,停止加热后还需继续向烧瓶中滴水一段时间,其目的为___。
(2)在C、D装置之间不需要防倒吸装置的理由是___。
(3)步骤Ⅳ中配制溶液时所需的玻璃仪器除玻璃棒和烧杯外,还有___。
(4)取25.00mL步骤Ⅳ中所配溶液,加入足量的双氧水,再加入足量盐酸酸化的BaCl2溶液,将所得沉淀过滤、洗涤、干燥,称其质量为4.66g。则FexSy的化学式为___。
(5)有同学认为可将装置D改为装有足量碱石灰的干燥管,通过测定反应前后干燥管的增重来计算硫元素的含量。你认为此方案是否合理:__(填“是”或“否”),原因为__。
(6)反应后D装置所得溶液中除含有Na2SO4外,还可能含有Na2SO3。现用滴定法测定溶液中Na2SO3的含量。可供选择的试剂:0.1000mol·L-1 KMnO4酸性溶液;0.1000mol·L-1 H2O2溶液;0.1000mol·L-1KI淀粉溶液;0.1000mol·L-1BaCl2溶液;0.1000mol·L-1HCl溶液。
①所选试剂应装在___(填“酸式”或“碱式”)滴定管中。
②所利用的反应原理为___(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从玉米穗轴、棉桃外皮中可提取出一种烃的含氧衍生物A,纯净的A为白色固体,易溶于水。为了研究A的组成和结构,进行了如下实验:
Ⅰ.将15gA在足量纯氧中充分燃烧,并使产物依次通过无水氯化钙、无水硫酸铜和碱石灰。实验后硫酸铜粉末没有变蓝,无水氯化钙增重9g,碱石灰增重22g。
Ⅱ.用一种现代分析技术测得其相对分子质量为150。
Ⅲ.取适量A配成水溶液,与银氨溶液共热,产生光亮如镜的银。
Ⅳ.控制一定条件,使A与足量乙酸发生酯化反应,测得产物的相对分子质量为318。
已知:A分子中无支链含![]() 结构的分子不稳定。
结构的分子不稳定。
请回答下列问题:
(1)A分子中C、H、O的原子个数比为___,A的分子式为___。
(2)步骤Ⅱ中采用的技术为(______)
A.元素分析 B.红外光谱 C.核磁共振谱 D.质谱法
(3)A中所含官能团的名称为___。
(4)步骤Ⅳ中发生反应的化学方程式为___。
(5)A加氢变成一种更有实用价值的化合物B,B可作为糖尿病人的甜味剂,其结构简式为___,根据系统命名法,B的名称为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁二酮肟镍是丁二酮肟在氨性溶液(pH=8~9)中与Ni2+发生反应生成的沉淀,该反应常用作实验室中检验镍离子。其结构如图所示,下列对该物质的分析与判断中,正确的是
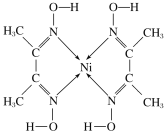
A.该物质中Ni原子具有空轨道,是配合物的配体
B.该物质中C、N、O原子存在孤电子对
C.该物质的分子中含有的化学键有共价键和配位键
D.该物质中碳原子的杂化类型均为sp2杂化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com