
【题目】摩尔是( )
A.物质的质量单位B.物质的量C.6.02×1023个微粒D.物质的量的单位
 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:
【题目】粗盐除含NaCl外,还含Mg2+、Ca2+、SO42-以及泥沙等杂质。以下是制备精盐的各步操作流程:
(1)过滤和蒸发操作中所使用的共同玻璃仪器是______,他们的作用分别是________、_______。
(2)过滤操作中要点可概括为“一贴、二低、三靠”,其中“二低”的含义是_______;_________。
(3)蒸发食盐水时,何时停止加热?__________________________。
(4)第②步操作的目的是除去粗盐中的__________(填化学式), 所涉及的化学方程式是________,判断BaCl2已过量的方法是__________。
(5)第③步操作中,除杂试剂不能用KOH的理由是______。
(6)第④步操作中加入的除杂试剂是__________(填化学式)。
(7)写出第⑥步操作中涉及的化学方程式:__________。
(8)实验室进行NaCl溶液蒸发结晶时,一般有以下操作过程,其正确的操作顺序为_______
①固定铁圈位置;②放置酒精灯;③放上石棉网;④放上蒸发皿;⑤加热搅拌;⑥停止加热,余热蒸干
A.①②③④⑤⑥ B.②①③④⑤⑥ C.②①④⑤⑥ D.②①③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、有4种化合物W(通常状况下是气态)、X(通常状况下是液态)、Y、Z(通常状况下是固态),它们共由5种短周期元素A、B、C、D、E组成。已知:①原子序数A<B<C<D<E,且A与D同族;C与E同族;B与C同周期。②W由A和B组成,且W分子中,A与B的原子个数比为4∶1;X由A和C组成,且X分子中A与C的原子个数比为1∶1;Y由C和D组成,属离子化合物,且测得Y固体中C与D的原子个数比为1∶1。③Z由D和E组成,属离子化合物,且其阳离子比阴离子少1个电子层,阳离子数与阴离子数之比为2∶1。试推断写出:
(1)W的化学式是________,W属于________化合物。
(2)X的电子式是________,X属于________化合物。
(3)1 mol Y在干燥的空气中质量会______(填“增大”或“减小”),其变化量(Δm)为________。
(4)用电子式表示化合物Z的形成过程________。
II.已知Si—Cl键、H—H键、H—Cl键、Si—Si键的键能分别为a kJ·mol-1、b kJ·mol-1、c kJ·mol-1、d kJ·mol-1,1 mol硅晶体含2 mol Si—Si键。工业上,提纯硅的化学方程式是SiCl4(g)+2H2(g)===Si(s)+4HCl(g) 则该反应的反应热是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种短周期主族元素,原子序数由A到E逐渐增大。①A元素最外层电子数是次外层电子数的2倍。 ②B的阴离子和C的阳离子与氖原子的电子层结构相同。③在通常状况下,B的单质是气体,0.1molB的气体与足量的氢气完全反应共有0.4mol电子转移。④C的单质在点燃时与B的单质充分反应,生成淡黄色的固体,此淡黄色固体能与AB2反应可生成B的单质。⑤D的气态氢化物与其最高价含氧酸间能发生氧化还原反应。请写出:
(1)A元素的最高价氧化物的电子式_____________。
(2)B元素在周期表中的位置_____________。
(3)B单质与C单质在点燃时反应的生成物中所含化学键类型有 ______________ 。
(4)D元素的低价氧化物与E的单质的水溶液反应的化学方程式为______________。
(5)C与D能形成2:1的化合物,用电子式表示该化合物的形成过程的______________。
(6)元素D与元素E相比,能证明这两种元素非金属性谁更强的事实是___________(填选项序号)。
a.常温下D的单质和E的单质状态不同
b.E的氢化物比D的氢化物稳定
c.一定条件下D和E的单质都能与钠反应
d.D的最高价含氧酸酸性弱于E的最高价含氧酸
e.D的单质能与E的氢化物反应生成E单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学根据苯和四氯化碳互溶,苯的密度比水小,四氯化碳的密度比水大的性质制作了如图所示的“液体积木”在试管中注入CCl4,再加少量水,然后再小心加入少量苯,溶液可出现分三层的现象,再用漏斗向水层中加入少量胆矾溶液及少量碘水(如图所示),静置一段时间,下列说法正确的是( )

A. 上中下三层的颜色分别为无色、蓝色、紫色
B. 上中下三层的颜色分别为紫色、蓝色、紫色
C. 振荡再静置后溶液分为两层,水在下层
D. 振荡再静置后溶液仍分为三层
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)一定温度下,有摩尔质量为M g·mol-1的某物质溶于适量的水中,得到物质的量浓度为c mol·L-1、密度为ρ g·cm-3的饱和溶液。则该温度下此物质的溶解度为__________。
(2)相同条件下,有X、Y两种气体,相对分子质量分别为A、B。
①若它们的质量相等,则两种气体的分子数之比N(X)∶N(Y)= _________;
②若它们的体积相等,则两种气体的质量之比m(X)∶m(Y)= _________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近些年,地表水和地下水域 中的高氯酸盐污染及其降解受到环境工作者的关注。某科研小组研究了一定条件 下温度、酸碱性对其降解的影响(初始质量浓度均为100mg/L),测得数据如图所示,下列说法不正确的是
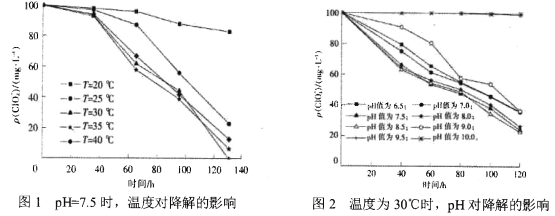
A. 在pH=7.5、温度为35℃时,0~60 h内高氯酸盐的降解平均速率为1mg/(L· h)
B. 当pH=7.5时,高氯酸盐降解最适宜温度为30℃
C. 当温度一定时,随pH的减小,高氯酸盐的降解速率不一定增大
D. 当降解时间为100h时 ,pH=7.5、温度为28℃与pH=7.3、温度为30℃两种条件下高氯酸盐的降解率可能相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com