
【题目】下列过程中△H>0的是
A. 碳酸钙受热分解 B. 乙醇燃烧
C. 铝粉与氧化铁粉末反应 D. 氧化钙溶于水
科目:高中化学 来源: 题型:
【题目】一定温度下,在3个体积均为1.0L的恒容密闭容器中反应2SO2(g)+O2(g)![]() 2SO3(g)达到平衡。下列说法正确的是
2SO3(g)达到平衡。下列说法正确的是
容器 | 温度/K | 物质的起始浓度/mol/L | 物质的平衡浓度/mol/L | SO2或SO3平衡转化率 | ||
c(SO2) | c(O2) | c(SO3) | c(SO3) | |||
I | 723 | 0.2 | 0.1 | 0 | 0.16 | a1 |
II | 723 | 0.4 | 0.2 | 0 | a2 | |
III | 823 | 0 | 0 | 0.2 | a3 | |
A. 达到平衡时,a1+a3>1
B. 达到平衡时,容器中的压强: PII>PI>PIII
C. 达到平衡时,容器III中的逆反应速率比容器I中的大
D. 若起始时,向容器I中充入0.16molSO2、0.04molO2和0.16molSO3,则此时反应向逆反应方向进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是某科研小组利用废铁屑还原浸出软锰矿(主要成分为MnO2)制备硫酸锰及电解其溶液制锰的工艺流程图:

已知:①浸出液中主要含有Fe3+、Fe2+、Co2+、Ni2+等杂质金属离子;
②生成氢氧化物的pH见下表:
物质 | Fe(OH)2 | Fe(OH)3 | Ni(OH)2 | Co(OH)2 | Mn(OH)2 |
开始沉淀pH | 7.5 | 2.7 | 7.7 | 7.6 | 8.3 |
完全沉淀pH | 9.7 | 3.7 | 8.4 | 8.2 | 9.8 |
请回答下列问题:
(1)“酸浸”前将原料粉碎的目的是______________。
(2)流程图中“①加入MnO2”的作用是将浸出液中的Fe2+氧化为Fe3+,同时自身被还原为Mn2+。该反应的离子方程式是_________,其中的MnO2可以用试剂_____(填化学式)代替。
(3)流程图中“②调节pH”可以除去某种金属离子,应将溶液pH调节控制的范围是_________下列可用于流程中调节pH的试剂是__________(填试剂对应的字母编号)。
a.MnCO3 b.Na2CO3 C.NaOH d.氨水
(4)向滤液I中加人MnS的作用是除去Co2+、Ni2+等离子,发生反应为MnS+Ni2+=NiS+Mn2+等。当该反应完全后,滤液2中的Mn2+与Ni2+离子的物质的量浓度之比是_______[已知Ksp(MnS)=2.8×10-10,Ksp(NiS)=2.0×10-21]。
(5)上述流程中,能循环使用的一种物质是___________(填化学式)。
(6)上述流程中在电解前需对电解液中Mn2+的含量进行测定。方法是:取出一定体积的电解液,加入一定质量的NaBiO3(不溶于水),使二者发生反应,反应的氧化产物和还原产物分别是MnO4-、Bi3+。该反应的离子方程式是_______________。
(7)在适当条件下,在MnSO4=H2SO4+H2O为体系的电解液中电解也可获得MnO2,其阳极电极反应式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】类比pH的定义,对于稀溶液可以定义pC=-lgC,pKa=-lgKa。常温下,某浓度H2A溶液在不同pH值下,测得pC(H2A)、pC(HA-)、pC(A2-)变化如图所示。下列说法正确的是
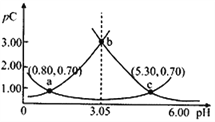
A. pH=3.50时,c(H2A)>c(HA-)>c(A2-)
B. 常温下,pKa1(H2A)=5.30,pKa2(H2A)=0.80
C. b点时,![]() =104.50
=104.50
D. pH=3.00~5.30时,c(H2A)+c(HA-)+c(A2-)先增大后减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期金属元素甲~戊在元素周期表中的相对位置如下表所示。下列判断正确的是( )

A. 原子半径:丙<丁<戊 B. 金属性:甲>丙
C. 氢氧化物碱性:丙>丁>戊 D. 最外层电子数:甲>乙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种短周期主族元素,它们的原子序数依次增大,其中A元素原子核外电子仅有一种原子轨道,也是宇宙中最丰富的元素,B元素原子的核外p电子数比s电子数少1,C为金属元素且原子核外p电子数和s电子数相等,D元素的原子核外所有p轨道全满或半满。
(1)写出四种元素的元素符号。
A:________,B:________,C:________,D:________。
(2)写出C、D两种元素基态原子核外电子排布的电子排布图。
C:___________________________,D:_____________________________。
(3)写出B、C两种元素单质在一定条件下反应的化学方程式:____________。
(4)写出B元素单质和氢化物的电子式。单质:________,氢化物:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钨有“光明使者”的美誉,在自然界中主要以钨(+6价)酸盐的形式存在,黑钨矿的主要成分是铁和锰的钨酸盐,化学式常写成(Fe、Mn)WO4,钨酸(B)酸性很弱,难溶于水,黑钨矿传统冶炼工艺的第一阶段是碱熔法,第二阶段则是用还原剂还原出金属钨。化合物A、B、C含有同一元素。请回答下列问题:

(1)为提高水浸速率,采取的措施为___________________(写两种)。
(2)用还原剂还原出金属钨。
①碳和氢气均可还原化合物C得钨,用氢气比用碳更具有优点,其理由是___________。
②如果用金属铝与化合物C反应,还原出1mol钨至少需要铝的质量为___________。
(3)利用“化学蒸气转移法”提纯金属钨的反应原理为:W(s)+I2(g)![]() WI2(g) △H<0。
WI2(g) △H<0。
①一定温度下,向某恒容密闭容器中加入2molI2(g)和足量W(s)达平衡后,I2(g)的转化率为20%,则平衡时c[I2(g)]∶c[WI2(g)]=___________;相同条件下,若开始加入I2(g)的物质的量变为原来2倍,则下列数值是原来2倍的有___________(填标号)。
A.平衡常数 B.达到平衡的时间
C.I2(g)的物质的量浓度 D.平衡时WI2(g)的体积分数
②工业上利用上述反应原理提纯金属钨的示意图如右:

反应在真空石英管中进行,先在温度为T1端放入不纯W粉末和少量I2(g),一段时间后,在温度为T2的一端得到纯净的晶体,则温度T1___________T2(填:“>”、“<”或“=”)。
(4)写出黑钨矿中FeWO4在步骤Ⅰ中反应的化学方程式__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A.沸水中滴入FeCl3饱和溶液:Fe3++3H2O![]() Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
B.一小块钠投入水中:Na+2H2O===Na++2OH-+H2↑
C.用氢氧化钠溶液吸收过量二氧化碳:OH-+CO2===HCO![]()
D.Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-===2Fe2++I2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com