
【题目】氮、碳都是重要的非金属元素,合理应用和处理碳和氮的化合物,在生产生活中有重要意义。
I.研究含氮污染物的治理是环保的一项重要工作。
T℃时,发生如下反应,3NO(g)+O3(g)![]() 3NO2(g),将0.6molNO和0.2molO3气体充入到2L固定容积的恒温密闭容器中,NO的浓度随反应时间的变化如图1所示。
3NO2(g),将0.6molNO和0.2molO3气体充入到2L固定容积的恒温密闭容器中,NO的浓度随反应时间的变化如图1所示。
①T℃时,反应3NO(g)+O3(g)![]() 3NO2(g)的平衡常数K=_____。
3NO2(g)的平衡常数K=_____。
②不能说明反应达到平衡状态的是______________。
A.气体颜色不再改变 B.气体的平均摩尔质量不再改变
C.气体的密度不再改变 D.单位时间内生成O3和NO2物质的量之比为1∶3

II.NO2的二聚体N2O4是火箭中常用氧化剂。完成下列问题。如图2所示,A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的透明气囊.关闭K2,将各1molNO2通过K1、K3分别充入真空A、B中,反应起始时A、B的体积相同均为aL(忽略导管中的气体体积)。
①若容器A中到达平衡所需时间ts,达到平衡后容器内压强为起始压强的0.8倍,则平均化学反应速率v(NO2)=_______。
②若打开K2,平衡后B容器的体积缩至0.4aL,则打开K2之前,气球B体积为__________L。
③若平衡后在A容器中再充入0.5molN2O4,则重新到达平衡后,平衡混合气中NO2的体积分数____(填“变大”“变小”或“不变”)。
Ⅲ.氮有不同价态的氧化物,如NO、N2O3、NO2等,它们在一定条件下可以相互转化。
(1)某温度下,在一体积可变的密闭容器中充入1mol N2O3,发生反应N2O3![]() NO2(g)+NO(g),达到平衡后,于t1时刻改变某一条件后,速率与时间的变化图像如图所示,有关说法正确的是__________
NO2(g)+NO(g),达到平衡后,于t1时刻改变某一条件后,速率与时间的变化图像如图所示,有关说法正确的是__________

A.t1时刻改变的条件是增大N2O3的浓度,同时减小NO2或NO的浓度
B.t1时刻改变条件后,平衡向正反应方向移动,N2O3的转化率增大
C.在t2时刻达到新的平衡后,NO2的百分含量不变
D.若t1时刻将容器的体积缩小至原容积的一半,则速率~时间图像与上图相同
(2)在1000K下,在某恒容容器中发生下列反应:2NO2(g)![]() 2NO(g)+O2(g),将一定量的NO2放入恒容密闭容器中,测得其平衡转化率α(NO2)随温度变化如图所示。图中a点对应温度下.己知NO2的起始压强P0为120kPa,列式计算该温度下反应的平衡常数Kp= __________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
2NO(g)+O2(g),将一定量的NO2放入恒容密闭容器中,测得其平衡转化率α(NO2)随温度变化如图所示。图中a点对应温度下.己知NO2的起始压强P0为120kPa,列式计算该温度下反应的平衡常数Kp= __________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。


(3)对于反应N2O4(g)![]() 2NO2(g),在一定条件下N2O4与NO2的消耗速率与自身压强间存在关系:v(N2O4)=k1·p(N2O4),v(NO2)=k2·p2(NO2)。其中,k1、2是与反应及温度有关的常数。相应的速率-压强关系如图所示:一定温度下,k1、k2与平衡常数Kp间的关系是k1=____________;在上图标出点中,指出能表示反应达到平衡状态的两个点__________,理由是__________________________。
2NO2(g),在一定条件下N2O4与NO2的消耗速率与自身压强间存在关系:v(N2O4)=k1·p(N2O4),v(NO2)=k2·p2(NO2)。其中,k1、2是与反应及温度有关的常数。相应的速率-压强关系如图所示:一定温度下,k1、k2与平衡常数Kp间的关系是k1=____________;在上图标出点中,指出能表示反应达到平衡状态的两个点__________,理由是__________________________。
【答案】 240L/mol C 0.4/(at)mol·L-1·S-1 0.7a 变小 C Kp= 81 kPa 1/2K2KP BD 达到平衡时,N2O4与NO2的消耗速率满足条件v(NO2) = 2v(N2O4)
【解析】I.①T℃时,将0.6molNO和0.2molO3气体充入到2L固定容积的恒温密闭容器中,根据图象分析可知平衡状态NO浓度为0.1mol/L,10min达到平衡,
3NO(g)+O3(g)3NO2(g)
起始量(mol/L) 0.3 0.1 0
变化量(mol/L) 0.2 ![]() 0.2
0.2
平衡量(mol/L) 0.1 ![]() 0.2
0.2
K= =240,故答案为:240;
=240,故答案为:240;
②反应3NO(g)+O3(g)3NO2(g)反应是气体体积减小反应。A.气体颜色不再改变,说明二氧化氮浓度不变,说明反应达到平衡状态,故A不符合;B.反应前后气体质量不变,物质的量变化,当气体的平均摩尔质量不再改变,说明反应达到平衡状态,故B不符合;C.气体质量和体积不变,气体的密度始终不改变,不能说明反应达到平衡状态,故C符合;D.反应速率之比等于化学方程式计量数之比为正反应速率之比,当单位时间内生成O3和NO2物质的量之比为1:3,表明正逆反应速率相同,反应达到平衡状态,故D不符合;故答案为:C;
Ⅱ.①关闭K2,将各1molNO2通过K1、K3分别充入真空A、B中,反应起始时A、B的体积相同均为aL,若容器A中到达平衡所需时间ts,达到平衡后容器内压强为起始压强的0.8倍,设生成四氧化二氮为x
2NO2(g)N2O4(g)
起始量 1 0
变化量 2x x
平衡量 1-2x x
1-2x+x=0.8×1,x=0.2mol,则平均化学反应速率v(NO2)=  =
=![]() mol/(Ls),故答案为:
mol/(Ls),故答案为: ![]() mol/(Ls);
mol/(Ls);
②打开K2,则相当于是在等温等压时的平衡,因此平衡时等效的.由于此时反应物的物质的量是B中的二倍,所以打开K2之前,气球B体积为(aL+0.4aL)÷2=0.7aL,故答案为:0.7a;
③若平衡后在A容器中再充入0.5molN2O4,相当于中等压强,平衡正向进行,则重新到达平衡后,平衡混合气中NO2的体积分数变小,故答案为:变小;
Ⅲ.(1)A.该反应为体积可变的反应,所以根据图象中最后达到平衡的速率和之前速率相同,可知改变的条件应该是恒压条件下充入反应物,故A错误;B.改变的条件应该是恒压条件下充入反应物,属于等效平衡,故平衡时反应物转化率不变,故B错误;C.改变的条件应该是恒压条件下充入反应物,等效平衡,故平衡时二氧化氮体积分数不变,故C正确;D.若t1时刻将容器的体积缩小至原容器的一半,则压强增大,正逆反应速率都增大,所以速率~时间图象与上图不同,故D错误;故选C;
(2)图中a点对应温度下,NO2的转化率是0.6,设原来NO2的物质的量为xmol,转化的物质的量为0.6xmol,
2NO2(g)2NO(g) + O2
开始 x 0 0
转化0.6xmol 0.6xmol 0.3xmol
平衡0.4xmol 0.6xmol 0.3xmol
则混合气体的物质的量=0.4xmol+0.6xmol+0.3xmol=1.3xmol,相同条件下,气体的压强之比等于其物质的量之比,所以反应后压强=![]() ×1.3xmol=156kPa,NO2的分压=156kPa×
×1.3xmol=156kPa,NO2的分压=156kPa×![]() =48kPa,NO的分压=156kPa×
=48kPa,NO的分压=156kPa×![]() =72kPa,O2的分压=156kPa×
=72kPa,O2的分压=156kPa×![]() =36kPa,化学平衡常数Kp=
=36kPa,化学平衡常数Kp= =
=![]() =81 kPa,故答案为:81 kPa;
=81 kPa,故答案为:81 kPa;
(3)反应N2O4(g)2NO2(g),则化学平衡常数Kp= ,二者的反应速率之比等于其计量数之比,则υ(NO2):υ(N2O4)=k2p2(NO2):k1p(N2O4)=2:1,又化学平衡常数Kp=
,二者的反应速率之比等于其计量数之比,则υ(NO2):υ(N2O4)=k2p2(NO2):k1p(N2O4)=2:1,又化学平衡常数Kp= ,所以K1=
,所以K1=![]() K2Kp,满足平衡条件υ(NO2)=2υ(N2O4)即为平衡点,B、D点的压强之比等于其反应速率之比为1:2,所以B、D为平衡点,故答案为:
K2Kp,满足平衡条件υ(NO2)=2υ(N2O4)即为平衡点,B、D点的压强之比等于其反应速率之比为1:2,所以B、D为平衡点,故答案为: ![]() K2Kp;BD;达到平衡时,N2O4与NO2的消耗速率满足条件v(NO2) = 2v(N2O4)。
K2Kp;BD;达到平衡时,N2O4与NO2的消耗速率满足条件v(NO2) = 2v(N2O4)。


 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案科目:高中化学 来源: 题型:
【题目】KMnO4是一种用途广泛的氧化剂,可由软锰矿制备。
(1)KMnO4稀溶液是一种常用的消毒剂,其消毒机理与下列物质相似的是_______(填字母)。
a.75%酒精 b.双氧水 c.“84”消毒液(NaClO溶液)
(2)取制得的KMnO4产品2.0000g,溶于水配成250mL 溶液,取出25.00mL 于碘量瓶中,加入稀硫酸和足量碘化钾并放于暗处5 min 左右,然后加入数滴淀粉溶液作指示剂,用0.2500 mol·L-1标准Na2S2O3 溶液进行滴定,滴定至终点消耗Na2S2O3 溶液20.00 mL。
已知:I2+2S2O3-=2I-+ S4O62-,杂质不参加反应。
①滴定终点的现象是________________________________;
②已知KMnO4在酸性条件下能被KI还原为Mn2+,写出该反应的离子方程式___________;
③计算KMnO4产品的纯度_______。(写出计算过程)
④若盛装标准Na2S2O3溶液的滴定管未润洗,则会使KMnO4产品的纯度___________(填“偏高”、 “偏低”、“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】符合如图所示的转化关系,且当X、Y、Z的物质的量相等时,存在焓变△H=△H1+△H2。满足上述条件的X、Y可能是

①C、CO ②S、SO2 ③Na、Na2O ④AlCl3、Al(OH)3 ⑤Fe、Fe(NO3)2 ⑥NaOH、Na2CO3
A. ①④⑤ B. ①②③ C. ①③④ D. ①③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:pKa=-lgKa,25℃时,H2A的pKal=1.85,pKa2=7.19。常温下,用0.1 mol·L-1NaOH溶液滴定20 mL 0.1 mol·L-1H2A溶液的滴定曲线如图所示。下列说法正确的是

A. a点所得溶液中:V0=10 mL
B. b点所得溶液中:c(H2A)+c(H+)=c(HA-)+c(OH-)
C. A2-水解平衡常数Kh(A2-)=10-7.19
D. c点所得溶液中:c(A2-)=c(HA-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X,Y,Z,W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法正确的是( ) 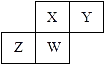
A.原子半径:W>Z>Y>X
B.最高价氧化物对应水化物的酸性:Z>W>X
C.最简单气态氢化物的热稳定性:Y>X>W>Z
D.元素Y,Z形成的化合物是制造光电池的主要材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 硅酸可由二氧化硅与水反应制得
B. Na2SiO3是硅酸盐,但不能溶于水
C. 硅是非金属元素,它的单质是灰黑色有金属光泽的固体
D. 硅是制造光导纤维的材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用湿法炼锌产生的铜镉渣生产金属镉的流程如下:

已知:铜镉渣主要含锌、铜、铁、镉(Cd)、钴(Co)等单质。
下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为0.1 mol·L-1计算):
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cd(OH)2 | Mn(OH)2 |
开始沉淀的pH | 1.5 | 6.5 | 7.2 | 8.2 |
沉淀完全的pH | 3.3 | 9.9 | 9.5 | 10.6 |
(1)为了提高铜镉渣浸出的速率,可采取的措施有:①适当升高温度;②搅拌;③______等。已知浸出的金属离子均为二价,写出浸出钴的化学方程式__________________。
(2)除钴的过程中,需要加入活化剂Sb2O3,锌粉会与Sb2O3、Co2+的溶液形成微电池并产生合金CoSb。该微电池的正极反应式为________________________________。
(3)除铁的过程分两步进行:
①先加入适量KMnO4,发生反应的离子方程式为______________________________,
②再加入ZnO控制反应液的pH范围为_____________。
(4)除铁过程第①步,若加入KMnO4时条件控制不当,MnO2会继续反应,造成的结果是______________,若加入的KMnO4不足量,则待电解溶液中有Fe元素残余。请设计实验方案加以验证_________________。
(5)净化后的溶液用惰性电极电解可获得镉单质。电解废液中可循环利用的溶质是____。
(6)处理含镉废水常用化学沉淀法,以下是几种镉的难溶化合物的溶度积常数(25℃):
Ksp(CdCO3)=5.210-12, Ksp(CdS)=3.610-29,Ksp(Cd(OH)2)=2.010-16,根据上述信息:
沉淀Cd2+效果最佳的试剂是____________。
a.Na2CO3 b.Na2S c.CaO
若采用生石灰处理含镉废水最佳pH为11,此时溶液中c(Cd2+)=_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对Fe(OH)3胶体和MgCl2溶液的描述正确的是
A. 两者都有丁达尔效应
B. Fe(OH)3胶体是带电的,MgCl2溶液是电中性的
C. 分散质的粒子都能透过滤纸
D. 逐滴加入稀硫酸,现象都是先沉淀,后溶解
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com