
【题目】A与NaOH溶液反应,有如下转化关系如下,(若产物中有水生成则省略表示出来)。
![]()
(1)若A为金属,C为气体,写出向B溶液中通入过量CO2反应的离子方程式________;
(2)若A为空气的成分之一,能造成温室效应,当向100mL1mol/LNaOH溶液中通入1.344L气体(标准状况)充分反应后,生成B和C的物质的量之比为_____(B的摩尔质量大于C);
(3)若A为AlCl3写出A与NaOH按物质的量比3:10混合时反应的离子方程式______。
【答案】 AlO2-+CO2+2H2O=HCO3-+Al(OH)3↓ 2:1 3Al3++10OH-=2Al(OH)3↓+AlO2-+2H2O
【解析】本题考查无机推断,(1)能与氢氧化钠反应的金属,产生气体,此金属为Al,C为H2,B为NaAlO2,利用碳酸的酸性强于偏铝酸,因此通入过量的CO2,发生的离子反应方程式为AlO2-+CO2+2H2O=HCO3-+Al(OH)3↓;(2)A是空气成分之一,且引起温室效应,因此A为CO2,与氢氧化钠反应产物可能是Na2CO3、NaHCO3、NaHCO3和Na2CO3的混合物,根据元素守恒,n(Na2CO3)+n(NaHCO3)=1.344/22.4,2n(Na2CO3)+n(NaHCO3)=100×10-3×1mol,解得n(NaHCO3)=0.02mol,n(Na2CO3)=0.04mol,B的摩尔质量大于C,则B为Na2CO3,C为NaHCO3,因此有B和C物质的量之比为0.4:0.02=2:1;(3)可能发生的反应是Al3++3OH-=Al(OH)3↓、Al(OH)3+OH-=AlO2-+2H2O,3molAl3+全部转变成Al(OH)3时,消耗9molOH-,生成3mol氢氧化铝,根据量,还剩1molOH-,1molOH-消耗1molAl(OH)3,生成1molAlO2-,n(Al3+):n(OH-):n(Al(OH)3):n(AlO2-)=3:10:2:1,反应的离子方程式为3Al3++10OH-=2Al(OH)3↓+AlO2-+2H2O。


科目:高中化学 来源: 题型:
【题目】
A. 少量金属钠保存在煤油中
B. FeSO4溶液存放在加有少量铁粉的试剂瓶中
C. 浓硝酸保存在棕色试剂瓶中
D. 氢氧化钠溶液保存在配有玻璃塞的细口瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色透明溶液,可能含有下列离子:Mg2+、A13+、Fe3+、Ba2+、H+、NH4+、SO42-、HCO3-、Cl-。取该溶液进行如下实验:①取溶液少许,滴入AgNO3溶液产生白色沉淀;②取溶液少许,滴入BaCl2溶液产生白色沉淀,加入足量稀硝酸沉淀不溶解;③取一定量的原溶液,加入一种淡黄色粉末状的固体X,产生气体的物质的量(n气体)、沉淀的物质的量(n沉淀)与加入淡黄色粉末的量(nx)的关系如下图所示(假设生成的气体全部逸出)。

根据实验现象和数据分析正确的是
A. 溶液中肯定大量存在的阳离子只有Mg2+、A13+、NH4+
B. 溶液中肯定没有的离子只有Fe3+、Ba2+
C. 当加入0.6mol淡黄色粉末时,生成两种气体分别为NH3和O2,其对应的体积比为2:3
D. 溶液中可能存在Cl-、HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的性质和应用都正确的是
A.氢氟酸具有强酸性,可用于雕刻玻璃
B.氨气显碱性,可用碱石灰或无水CaCl2干燥
C.MgO、A12O3熔点高,它们都可用于制作耐火材料
D.铜的活动性比铁弱,可在海轮外壳装铜块减缓海轮腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸是植物(特别是草本植物)常具有的成分,具有广泛的用途。草酸晶体(H2C2O4·2H2O)无色,熔点为101℃,易溶于水,受热易脱水、升华,170℃以上分解。常温下它的电离常数K1=5.4×10-2,K2=5.4×10-5。回答下列问题:
(1)拟用下列装置分解草酸制备少量纯净的CO,其合理的连接顺序为___________(填字母序号)。


![]()


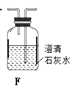
(2)相同温度条件下,分别用3支试管按下列要求完成实验:
试管 | A | B | C |
加入试剂 | 4mL 0.01mol/L KMnO4 1ml 0.1moL/L H2SO4 2mL 0.1mol/L H2C2O4 | 4mL 0.02mol/L KMnO4 1ml 0.1moL/L H2SO4 2mL 0.1mol/L H2C2O4 | 4mL 0.03mol/L KMnO4 1ml 0.1moL/L H2SO4 2mL 0.1mol/L H2C2O4 |
褪色时间 | 28秒 | 30秒 | 不褪色 |
写出试管B的离子方程式_____________________________________;上述实验能否说明“相同条件下,反应物浓度越大,反应速率越快”?____________(选填“能”或“不能”);简述你的理由:__________________________________。
(3)设计实验证明草酸为弱酸的方案及其现象均正确的有_____________(填序号)。
A.室温下,取0.010mol/L的H2C2O4溶液,测其pH=2;
B.室温下,取0.010mol/L的NaHC2O4溶液,测其pH >7;
C.室温下,取pH=a(a<3)的H2C2O4溶液稀释100倍后,测其pH< a+2;
D.标况下,取0.10mol/L的H2C2O4溶液100mL与足量锌粉反应,收集到H2体积为224mL;
(4)为测定某H2C2O4溶液的浓度,取20.00mL H2C2O4溶液于锥形瓶中,滴入2-3滴指示剂,用0.1000mol/L的NaOH溶液进行滴定,并进行3次平行实验,所用NaOH溶液体积分别为19.98mL、20.02mL和22.00mL。
①所用指示剂为_______________;滴定终点时的现象为_________________________;
②H2C2O4溶液物质的量浓度为_______________;
③下列操作会引起测定结果偏高的是__________(填序号)。
A. 滴定管在盛装NaOH溶液前未润洗
B. 滴定过程中,锥形瓶震荡的太剧烈,以致部分液体溅出
C. 滴定前读数正确,滴定终点时俯视读数
D. 滴定前读数正确,滴定终点时仰视读数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于元素周期表的说法正确的是( )
A. 18个纵行代表18个族,7个主族、8个副族
B. 短周期共有32种元素
C. 元素周期表共有7个横行代表7个周期
D. 第ⅠA族全部是金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能用离子方程式H++OH-→H2O表示的反应是( )
A. 稀硫酸和氢氧化钾 B. 稀硫酸和氢氧化钡溶液
C. 氢硫酸和氢氧化钠溶液 D. 稀硝酸和氨水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com