
【题目】【加试题】甲醇又称“木醇”或“木精”,沸点64.7℃,是无色有酒精气味易挥发的液体.甲醇有毒,误饮5~10mL能双目失明,大量饮用会导致死亡.甲醇是重要的化学工业基础原料和液体燃料,可用于制造甲醛和农药,并常用作有机物的萃取剂和酒精的变性剂等。
(1)工业上可利用CO2和H2生产甲醇,方程式如下:
CO2(g)+3H2(g)![]() CH3OH(l)+H2O(g) △H=Q1kJmol﹣1
CH3OH(l)+H2O(g) △H=Q1kJmol﹣1
又查资料得知:①CH3OH(l)+1/2O2(g)![]() CO2(g)+2H2(g) △H=Q2kJmol﹣1
CO2(g)+2H2(g) △H=Q2kJmol﹣1
②H2O(g)=H2O(l)△H=Q3kJmol﹣1,则表示甲醇的燃烧热的热化学方程式为 。
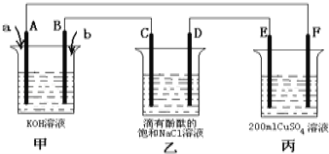
(2)甲醇燃料电池是符合绿色化学理念的新型燃料电池,下图是以甲醇燃料电池(甲池)为电源的电解装置.已知:A、B、C、D、E、F都是惰性电极,丙中为0.1mol/L CuSO4溶液 (假设反应前后溶液体积不变),当向甲池通入气体a和b时,D极附近呈红色.回答下列问题:
①a物质是 ,A电极的电极反应式为 。
②乙装置中的总化学反应方程式为 。
③当乙装置中C电极收集到224mL(标况下)气体时,丙中溶液的pH= 。
【答案】(1)CH3OH(l)+3/2O2(g)![]() CO2(g)+2H2O(l) △H=(2 Q1+3 Q2+2 Q3)kJmol﹣1;
CO2(g)+2H2O(l) △H=(2 Q1+3 Q2+2 Q3)kJmol﹣1;
(2)①甲醇,CH3OH-6e-+8OH- = CO32-+6H2O;②2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑;③1.
2NaOH+H2↑+Cl2↑;③1.
【解析】
试题分析:(1)已知A.CO2(g)+3H2(g)![]() CH3OH(l)+H2O(g) △H=Q1kJmol﹣1;①CH3OH(l)+1/2O2(g)
CH3OH(l)+H2O(g) △H=Q1kJmol﹣1;①CH3OH(l)+1/2O2(g)![]() CO2(g)+2H2(g) △H=Q2kJmol﹣1;②H2O(g)=H2O(l)△H=Q3kJmol﹣1,由2a+3①+2②得:CH3OH(l)+3/2O2(g)
CO2(g)+2H2(g) △H=Q2kJmol﹣1;②H2O(g)=H2O(l)△H=Q3kJmol﹣1,由2a+3①+2②得:CH3OH(l)+3/2O2(g)![]() CO2(g)+2H2O(l) △H=(2 Q1+3 Q2+2 Q3)kJmol﹣1,答案为:CH3OH(l)+3/2O2(g)
CO2(g)+2H2O(l) △H=(2 Q1+3 Q2+2 Q3)kJmol﹣1,答案为:CH3OH(l)+3/2O2(g)![]() CO2(g)+2H2O(l) △H=(2 Q1+3 Q2+2 Q3)kJmol﹣1;(2)A、B、C、D、E、F都是惰性电极,乙中装的是滴有酚酞的饱和NaCl溶液,D极附近呈红色,那么D极发生的反应为2H2O+2e-=H2↑+2OH-,可以推出A为燃料电池的正极,B为燃料电池的负极,①a物质是甲醇,发生的电极反应为:CH3OH+6e-+8OH- = CO32-+6H2O,答案为:甲醇,CH3OH-6e-+8OH- = CO32-+6H2O;②乙装置中是电解饱和食盐水,反应方程式为:2NaCl+2H2O
CO2(g)+2H2O(l) △H=(2 Q1+3 Q2+2 Q3)kJmol﹣1;(2)A、B、C、D、E、F都是惰性电极,乙中装的是滴有酚酞的饱和NaCl溶液,D极附近呈红色,那么D极发生的反应为2H2O+2e-=H2↑+2OH-,可以推出A为燃料电池的正极,B为燃料电池的负极,①a物质是甲醇,发生的电极反应为:CH3OH+6e-+8OH- = CO32-+6H2O,答案为:甲醇,CH3OH-6e-+8OH- = CO32-+6H2O;②乙装置中是电解饱和食盐水,反应方程式为:2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑,答案为:2NaCl+2H2O
2NaOH+H2↑+Cl2↑,答案为:2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑;③当乙装置中C电极的反应为:—2e- = Cl2↑, 生成224mL(标况下)气体时,转移的电子数为0.02mol,丙中E电极的电极反应式为: 2H2O-4e-=O2↑+4H+,转移0.002mol电子,产生的H+的物质的量为0.002mol,物质的量浓度为:0.02mol/0.2=0.1mol/L,pH为1,答案为1.
2NaOH+H2↑+Cl2↑;③当乙装置中C电极的反应为:—2e- = Cl2↑, 生成224mL(标况下)气体时,转移的电子数为0.02mol,丙中E电极的电极反应式为: 2H2O-4e-=O2↑+4H+,转移0.002mol电子,产生的H+的物质的量为0.002mol,物质的量浓度为:0.02mol/0.2=0.1mol/L,pH为1,答案为1.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】(1)苯、四氯化碳、乙醇都是常见的有机溶剂。能与水互溶的是 ;难溶于水,且密度比水小的是 。
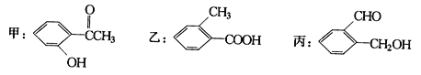
(2)现有化合物:
①请写出丙中含氧官能团的名称: 。
②请判别上述哪些化合物互为同分异构体: (填代号)。
(3)同温同压下,相同体积某烷烃的蒸气质量是氢气质量的36倍,该烃的分子式为____________,写出该烃的所有同分异构体的结构简式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳、氮广泛的分布在自然界中,碳、氮的化合物性能优良,在工业生产和科技领域有重要用途。
(1)氮化硅(Si3N4)是一种新型陶瓷材料,它可由SiO2与过量焦炭在1300~1700oC的氮气流中反应制得:3SiO2(s)+6C(s)+2N2(g) ![]() Si3N4(s)+6CO(g)。⊿H =-1591.2 kJ/mol,则该反应每转移1mole—,可放出的热量为 。
Si3N4(s)+6CO(g)。⊿H =-1591.2 kJ/mol,则该反应每转移1mole—,可放出的热量为 。
(2)某研究小组现将三组CO(g)与H2O(g)的混合气体分别通入体积为2L的恒容密闭容器中,一定条件下发生反应:CO(g)+H2O(g)![]() CO2(g)+H2(g),得到如下数据:
CO2(g)+H2(g),得到如下数据:
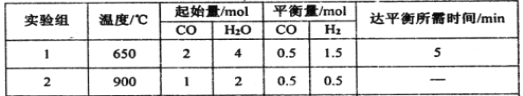
① 实验1中,前5min的反应速率v(CO2)= 。
②下列能判断实验2已经达到平衡状态的是 。
a.容器内CO、H2O、CO2、H2的浓度不再变化 b.容器内压强不再变化
c.混合气体的密度保持不变 d.v正(CO) =v逆(CO2)
e.容器中气体的平均相对分子质量不随时间而变化
③若实验2的容器是绝热的密闭容器,实验测得H2O(g)的转化率H2O%随时间变化的示意图如下图所示, b点v正 v逆(填“<”、“=”或“>”),t3~t4时刻,H2O(g)的转化率H2O%降低的原因是 。

(3)利用CO与H2可直接合成甲醇,下图是由“甲醇-空气”形成的绿色燃料电池的工作原理示意图,写出以石墨为电极的电池工作时负极的电极反应式 ,利用该电池电解1L 0.5mol/L的CuSO4溶液,当消耗560mLO2(标准状况下)时,电解后溶液的pH= (溶液电解前后体积的变化忽略不计)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸盐在能源环保领域有广泛用途。用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示。下列推断合理的是
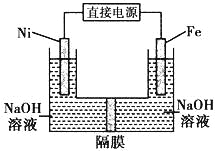
A. 镍是阳极,电极反应为4OH--4e一= O2↑+ 2 H2O
B. 电解时电流的方向为:负极→Ni电极→溶液→Fe电极→正极
C. 若隔膜为阴离子交换膜,则OH-自右向左移动
D. 电解时阳极区pH降低、阴极区pH升高,撤去隔膜混合后,与原溶液比较pH降低(假设电解前后体积变化忽略不计)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I. “立方烷”是一种人工合成的烃,其分子为正方体结构,其碳架结构如图所示:
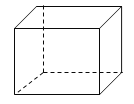
(1)“立方烷”有多种同分异构体,其中一种属于芳香烃的同分异构体的结构简式是 。
(2)立方烷”的三氯代物具有同分异构体的数目是 。
II.有机化学中的反应类型较多,将下列反应归类(填序号)。
①乙烷在空气中燃烧 ②由乙炔制氯乙烯
③甲烷与氯气在光照的条件下反应 ④乙烯使酸性高锰酸钾溶液褪色
⑤乙烯使溴的四氯化碳溶液褪色 ⑥实验室制乙烯
⑦由甲苯制取TNT ⑧溴乙烷和氢氧化钠的乙醇溶液共热
⑨乙苯的制备:![]()
(1)其中属于取代反应的是__________;属于氧化反应的是_______;
(2)写出⑦和⑧的化学方程式:
⑦_______________________ _____________________________
⑧_______________________ _____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【加试题】硝酸铝[Al(NO3)3]是一种常用媒染剂。工业上用铝灰(主要含Al、Al2O3、Fe2O3等)制取硝酸铝晶体[Al(NO3)3·9H2O]的流程如下:

(1)写出反应Ⅰ的离子方程式: (任写一个)。
(2)若在实验室中完成反应Ⅱ,为避免铝的损失,需要解决的问题是 ,可采取的措施为 。
(3)温度高于200℃时,硝酸铝完全分解成氧化铝和两种气体(其体积比为4:1),该反应的化学方程式是 。
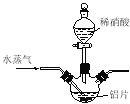
(4)若用右图所示实验装置制取Al(NO3)3,通入水蒸气的作用是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】3,5-二甲氧基苯酚是重要的有机合成中间体,可用于天然物质白柠檬素的合成。一种以间苯三酚为原料的合成反应如下:

甲醇、乙醚和3,5-二甲氧基苯酚的部分物理性质见下表:
物质 | 沸点/℃ | 熔点/℃ | 密度(20℃) / g·cm-3 | 溶解性 |
甲醇 | 64. 7 |
| 0. 7915 | 易溶于水 |
乙醚 | 34. 5 |
| 0. 7138 | 微溶于水 |
3,5-二甲氧基苯酚 |
| 33-36 |
| 易溶于甲醇、乙醚,微溶于水 |
反应结束后,先分离出甲醇,再加入乙醚进行萃取。
(1)①分离出甲醇的操作是的 。
②萃取用到的分液漏斗使用前需 并洗净,分液时有机层在分液漏斗的 填(“上”或“下”)层。
(2)分离得到的有机层依次用饱和NaHCO3溶液、饱和食盐水、少量蒸馏水进行洗涤。用饱和NaHCO3 溶液洗涤的目的是 ;用饱和食盐水洗涤的目的是 。
(3)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是 (填字母)。
a.蒸馏除去乙醚 b.重结晶 c.过滤除去干燥剂 d.加入无水CaCl2干燥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】邻苯二甲酸丁基月桂酯是一种淡黄色透明油状液体,密度约0.97g/cm3,常用作聚氯乙烯等树脂的增塑剂。工业上生产原理和工艺流程如下:
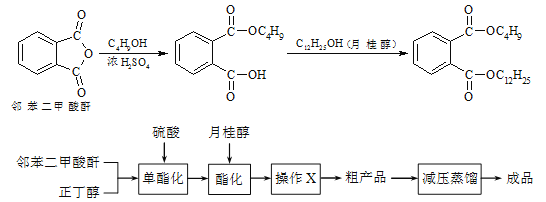
有关物质的物理性质见下表:
化合物 | 溶解性 | 熔点 | 沸点 |
邻苯二甲酸酐 | 微溶于冷水、乙醚,易溶于热苯、乙醇、乙酸 | 131.6℃ | 295℃ |
正丁醇 | 微溶于水,溶于乙醇、醚、多数有机溶剂 | -88.9℃ | 117.5℃ |
月桂醇 | 不溶于水,溶于醇、醚 | 24 | 259℃ |
邻苯二甲酸丁基月桂酯 | 不溶于水,溶于多数有机溶剂 | 不祥 | 202~210℃ |
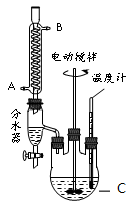
某实验小组的同学模拟工业生产的工艺流程,用右图所示装置制取少量邻苯二甲酸丁基月桂酯,图中夹持和加热装置已略去。主要操作步骤如下:
①向三颈烧瓶内加入30 g 邻苯二甲酸酐、16 g 正丁醇以及少量浓硫酸。
②搅拌,升温至105 ℃,持续搅拌反应1小时。
③冷却至室温,加入40 g 月桂醇,升温至160 ℃,搅拌、保温至反应结束。
④冷却至室温,将反应混合物倒出。
⑤通过工艺流程中的操作X,得到粗产品。
请回答下列问题:
(1)仪器C的名称___________。冷凝管中冷水应从___________进。
(2)步骤③中判断反应已结束的方法是___________。
(3)步骤⑤中操作X可除去少量未反应的邻苯二甲酸酐及正丁醇,操作X包括___________。
(4)工艺流程中减压蒸馏的目的是___________。
(5)实验结果表明步骤②、③产率都比较高,原因是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学——选修3:物质结构与性质】A、B、C、D、E、F为元素周期表前四周期的元素,原子序数依次增大。A元素的单质是空气的主要成分,B原子核外p轨道上有1对成对电子,D元素的价电子数是其余电子数的一半,C与B同主族,A与F同主族,D与E同族。回答下列问题:
(1)A、B、C第一电离能由大到小的顺序为: (用元素符号表示)。
(2)B与C形成的二元化合物中,属于非极性分子的是: (填化学式);该分子中心原子的杂化类型为: 。
(3)A、C元素形成的常见含氧酸中,分子的中心原子的价层电子对数为4的酸是 ;(填化学式,下同)酸根呈平面三角形的酸是 。
(4)E和F形成的一种化合物的晶体结构如图所示,则该化合物的化学式为 ;F的配位数为 。
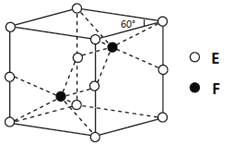
(5)D的离子可以形成多种配合物,由Dn+、Br-、C的
最高价含氧酸根和A的简单氢化物形成的1:1:1:5的某
配合物,向该配合物的溶液中滴加AgNO3溶液产生
淡黄色沉淀,滴加BaCl2溶液无现象,则该配合物的化学式为: ;n值为 ;Dn+的基态电子排布式为: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com