
【题目】短周期元素X、Y、W的原子序数依次增大,元素X的一种单质有杀菌俏毒的作用,Y与X的某种化合物A可以作潜水艇的供氧剂。 W质子数为偶数,室温下W单质为黄色固体。生活中常见元素M的一种氧化物有磁性,回答下列问题:
(1) W元素位于周期表中的第________周期、_________族。
(2)写出化合物A的电子式____________
用电子式表示W元素气态氢化物的形成过程____________。
(3)X的简单氢化物与M的单质在高温下反应的化学方程式为__________
(4)X的氢化物沸点高于W的氢化物沸点,原因是___________
【答案】 三 ⅥA ![]()
![]() 3Fe+4H2O
3Fe+4H2O![]() Fe2O3+4H2(反应条件写加热也给分) 水分子间存在氢键
Fe2O3+4H2(反应条件写加热也给分) 水分子间存在氢键
【解析】元素X的一种单质有杀菌俏毒的作用,说明X为氧元素,Y与X的某种化合物A可以作潜水艇的供氧剂,则Y为Na元素; W质子数为偶数,室温下W单质为黄色固体,可知W为硫元素,生活中常见元素M的一种氧化物有磁性,则M为Fe元素;
(1) 硫元素的核电荷数为16,位于周期表中的第三周期、ⅥA 族;
(2)Na2O2是离子化合物,其电子式为![]() ;H2S是共价化合物,其电子式形成过程为
;H2S是共价化合物,其电子式形成过程为![]() ;
;
(3)Fe在高温下与H2O反应生成四氧化三铁和氢气的化学方程式为3Fe+4H2O![]() Fe2O3+4H2;
Fe2O3+4H2;
(4)水分子间存在氢键,故H2O的沸点比H2S高。


 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:高中化学 来源: 题型:
【题目】已知二氧化硫可使酸性高锰酸钾溶液褪色,化学反应方程式为:
5SO2 + 2KMnO4 + 2H2O = K2SO4 + 2MnSO4 + 2H2SO4
用下图装置来验证浓硫酸与木炭在加热条件下反应的产物中含有SO2和CO2。试用如图所列各装置设计一个实验,来验证上述反应所产生的各种产物。
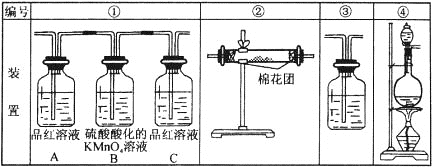
(1)这些装置的连接顺序是(按产物气流从左至右的方向,填写装置的编号):______→____→____→____。
(2)实验时可观察到装置①中A瓶的溶液褪色。A瓶溶液的作用是_________,B瓶溶液的作用是_______, C瓶溶液的作用是________________。
(3)装置②中所加的固体药品是____________,可验证的产物是____________。
(4)装置③中所盛溶液是_____________,可验证的产物是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含有HCO3-、CO32-、SO32-、Na+、NO3-五种离子,若向其中加入Na2O2粉末,则充分反应后溶液中离子浓度保持不变的是(溶液体积变化忽略不计)
A. CO32- NO3- Na+ B. CO32- NO3- C. SO32- NO3- D. NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液中可能含有下列几种离子中的某几种:Ca2+、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、Cu2+。为确认溶液组成进行如下实验:(1)200mL上述溶液,加入足量
、Cu2+。为确认溶液组成进行如下实验:(1)200mL上述溶液,加入足量![]() 溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30g,向沉淀中加入过量的盐酸,有2.33g沉淀不溶。(2)向(1)的滤液中加入足量的
溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30g,向沉淀中加入过量的盐酸,有2.33g沉淀不溶。(2)向(1)的滤液中加入足量的![]() 溶液,加热,产生能促使湿润红色石蕊试纸变蓝的气体1.12L(已换算成标准状况,假定产生的气体全部逸出)。由此可以得出关于原溶液组成的正确结论是
溶液,加热,产生能促使湿润红色石蕊试纸变蓝的气体1.12L(已换算成标准状况,假定产生的气体全部逸出)。由此可以得出关于原溶液组成的正确结论是
(1)溶液中一定不存在的离子是__,不能确定是否存在的离子是__.为确定该离子,应当补充的实验名称是______________
(2)溶液中肯定存在的阴离子有哪些?通过计算求出它们的物质的量浓度(或范围)。______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. 6.8g固体KHSO4与3.9g固体Na2O2中阴离子数目相同
B. 常温下铁、铜均不溶于浓硫酸,说明常温下铁、铜与浓硫酸均不反应
C. 离子化合物中只含离子键
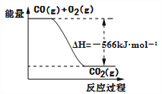
D. 已知:2CO(g)+O2(g)=2CO2(g);ΔH=-566kJ·mol-1,下图可表示由CO生成CO2的反应过程和能量关系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:N2(g)+3H2(g)![]() 2NH3(g)(正反应为放热反应),673 K、30 MPa下,n(NH3)和n(H2)随时间t变化的关系示意图如图所示。下列叙述中正确的是( )
2NH3(g)(正反应为放热反应),673 K、30 MPa下,n(NH3)和n(H2)随时间t变化的关系示意图如图所示。下列叙述中正确的是( )
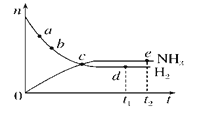
A. c点处正反应速率和逆反应速率相等
B. a点处正反应速率比b点处的大
C. d点(t1时刻)和e点(t2时刻)处n(N2)不同
D. t2时刻,正反应速率大于逆反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组微粒中,在一定条件下均可以作氧化剂的是
A. F-、Br-、S2- B. Fe3+、MnO4-、NO3-
C. Cl2、HClO、Mg D. ClO-、Cl-、Ag+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式书写正确的是( )
A.2SO2+O2![]() 2SO3 △H=-196.6kJ/mol
2SO3 △H=-196.6kJ/mol
B.C(s)+O2(g)=CO2(g) △H=+393.5kJ/mol
C.在500℃、30MPa下,将0.5molN2和1.5molH2置于密闭容器中充分反应生成NH3(g),放出热量19.3kJ,其热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) △H=-38.6kJ/mol
2NH3(g) △H=-38.6kJ/mol
D.2.00gC2H2气体完全燃烧生成液态水和二氧化碳气体,放出99.6kJ的热量,该反应的热化学方程式为:2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H=-2589.6kJ/moL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com