
【题目】某溶液中含有HCO3-、CO32-、SO32-、Na+、NO3-五种离子,若向其中加入Na2O2粉末,则充分反应后溶液中离子浓度保持不变的是(溶液体积变化忽略不计)
A. CO32- NO3- Na+ B. CO32- NO3- C. SO32- NO3- D. NO3-
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:
【题目】液氨和水类似,也能电离:NH3+NH3![]() NH4++NH2﹣,25℃时,其离子积K=1.0×10﹣30mol2L﹣2.现将2.3g金属钠投入1.0L液氨中,钠完全反应,有NaNH2和H2产生,则所得溶液中粒子关系不正确的是(设温度保持不变,溶液体积为1L)
NH4++NH2﹣,25℃时,其离子积K=1.0×10﹣30mol2L﹣2.现将2.3g金属钠投入1.0L液氨中,钠完全反应,有NaNH2和H2产生,则所得溶液中粒子关系不正确的是(设温度保持不变,溶液体积为1L)
A.c(Na+)=c(NH2﹣) B.c(NH4+)=1.0×10﹣29molL﹣1
C.c(NH2﹣)>c(NH4+) D.c(NH4+) c(NH2﹣)=1.0×10﹣30 mol2L﹣2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黑火药是我国古代的四大发明之一,距今已有1000多年的历史,其成分是木炭(C)、硫粉(S)和硝酸钾(KNO3)。回答下列有关问题:
(1)黑火药爆炸生成无毒的气体和K2S,该反应的化学方程式为________________。
(2)Se与S同主族,则Se原子的核外电子排布式为〔Ar〕________,有____对成对电子。
(3)C、N、O、K的电负性由大到小的顺序是_________________。
(4) 黑火药爆炸除生成K2S外,还生成少量K2S2,其结构类似于Na2O2。则K2S2中含有的化学键类型为_______________。
(5) K2S遇酸生成H2S,H2S分子中,S原子的杂化轨道类型是_________;KNO3可电离出NO3-,NO3-的空间构型是______________。
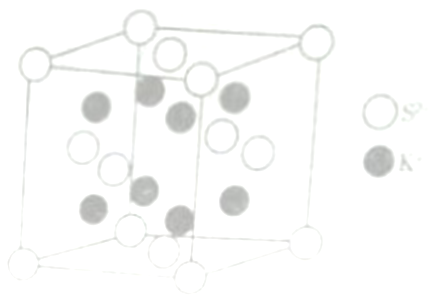
(6) K2S的晶胞结构如右图所示。其中K+的配位数为_______,若K2S晶体的密度为ρg·cm-3,则晶胞中距离最近的两个S2-核间距为_________cm(用NA表示阿伏伽德罗常数的值)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请回答下列问题:
(1)纯水在T ℃时pH=6,该温度下1 mol/L的NaOH溶液中,由水电离出的c(OH-)= mol/L。
(2)某一元弱酸溶液(A)与二元强酸(B)的pH相等。若将两溶液稀释相同的倍数后,pH(A) pH(B) (填“>”、“=”或“<”);现用上述稀释溶液中和等浓度等体积的NaOH溶液,则需稀释溶液的体积V(A) V(B)(填“>”、“=”或“<”)。
(3)已知:二元酸H2R 的电离方程式是:H2R=H++HR﹣,HR﹣![]() R2﹣+H+,若0.1molL﹣1NaHR溶液的c(H+)=a molL﹣1,则0.1molL﹣1H2R溶液中c(H+) (0.1+a) molL﹣1(填“<”、“>”或“=”),理由是 。
R2﹣+H+,若0.1molL﹣1NaHR溶液的c(H+)=a molL﹣1,则0.1molL﹣1H2R溶液中c(H+) (0.1+a) molL﹣1(填“<”、“>”或“=”),理由是 。
(4)电离平衡常数是衡量弱电解质电离程度的物理量。已知:
化学式 | 电离常数(25 ℃) |
HCN | K=4.9×10-10 |
CH3COOH[] | K=1.8×10-5 |
H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
①25 ℃时,有等浓度的HCN溶液、H2CO3溶液和CH3COOH溶液,三溶液的pH由大到小的顺序为________(用化学式表示)。
②向NaCN溶液中通入少量的CO2,发生反应的化学方程式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸亚铁(FeCO3)是菱镁矿的主要成分,将FeCO3加热到200℃开始分解为FeO和CO2,若在空气中高温煅烧FeCO3生成Fe2O3。
I.已知25℃,101kPa时:4Fe(s)+3O2(g)=2Fe2O3(s) △H=-1648kJ/mol
C(s)+ O2(g)=CO2(g) △H=-393 kJ/mol 2FeCO3(s)=2Fe(s)+ 3O2(g) △H=+148OkJ/mol
(1)请写出FeCO3在空气中煅烧生成Fe2O3的热化学方程式_______。
Ⅱ.生成的FeO和Fe2O3在一定条件下被还原为金属铁。
(2)据报道一定条件下Fe2O3可被甲烷还原为“纳米级”的金属铁。其反应为:
Fe2O3(s)+3CH4(g)=2Fe(s)+3CO(g)+6H2(g) △H>0
① 原子序数为26的铁元素位于元素周期表的第_______周期。
②反应在5L的密闭容器中进行,2min后达到平衡,测得Fe2O3在反应中质量消耗4.8g。则该段时间内用H2表达的平均反应速率为____________。
③将一定量的Fe2O3(s)和一定量的CH4(g)置于恒温恒压容器中,在一定条件下反应,能表明该反应达到平衡状态的是___________。
a.CH4的转化率等于CO的产率 b.混合气体的平均相对分子质量不变
c.v正(CO):v逆(H2)=1:2 d.固体的总质量不变
(3)FeO可用CO进行还原,已知:t℃时,FeO(s)+CO(g)![]() Fe(s)+CO2(g),K=0.5,若在1L密闭容器中加入0.04mol FeO(s),并通入xmolCO,t℃时反应达到平衡。此时FeO(s)的转化率为50%,则x=_______。
Fe(s)+CO2(g),K=0.5,若在1L密闭容器中加入0.04mol FeO(s),并通入xmolCO,t℃时反应达到平衡。此时FeO(s)的转化率为50%,则x=_______。
Ⅲ. Fe2O3还可用来制备FeCl3,FeCl3在水溶液中的水解分三步:
Fe3++H2O![]() Fe(OH)2++H+ K1
Fe(OH)2++H+ K1
Fe(OH)2++ H2O![]() Fe(OH)2++H+ K2
Fe(OH)2++H+ K2
Fe(OH)2++ H2O![]() Fe (OH)3+H+ K3
Fe (OH)3+H+ K3
(4)以上水解反应的平衡常效K1、K2、K3由大到小的顺序是_______。通过控制条件,以上水解产物聚合生成聚合物的离子方程式为:xFe3++yH2O===Fex(OH)y(3x-y)++yH+
欲使平衡正向移动可采用的方法是__________(填字母)
a.加水稀释 b.加入少量NaCl固体 c.升温 d.加入少量Na2CO3固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、W的原子序数依次增大,元素X的一种单质有杀菌俏毒的作用,Y与X的某种化合物A可以作潜水艇的供氧剂。 W质子数为偶数,室温下W单质为黄色固体。生活中常见元素M的一种氧化物有磁性,回答下列问题:
(1) W元素位于周期表中的第________周期、_________族。
(2)写出化合物A的电子式____________
用电子式表示W元素气态氢化物的形成过程____________。
(3)X的简单氢化物与M的单质在高温下反应的化学方程式为__________
(4)X的氢化物沸点高于W的氢化物沸点,原因是___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据事实,写出下列反应的热化学方程式。
(1)在25℃、101kPa下,1g液态甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为: 。
(2)若适量的N2和O2完全反应,每生成23克NO2需要吸收16.95kJ热量。写出1mol N2和O2完全反应的热化学方程式为: 。
(3)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com