
【题目】一定条件下,CH4与H2O(g)发生反应:CH4(g)+H2O(g) ![]() CO(g)+3H2(g)。 设起始
CO(g)+3H2(g)。 设起始![]() ,在恒压下,平衡时CH4的体积分数
,在恒压下,平衡时CH4的体积分数![]() 与Z和T(温度)的关系如图所示,下列说法错误的是
与Z和T(温度)的关系如图所示,下列说法错误的是
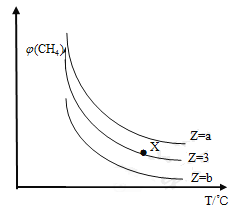
A. 该反应的焓变△H>0
B. 图中Z的大小为b>3>a
C. 图中X点对应的平衡混合物中![]()
D. 温度不变时,加压,平衡逆向移动,甲烷的体积分数增大
 名校通行证有效作业系列答案
名校通行证有效作业系列答案科目:高中化学 来源: 题型:
【题目】下列关于“有效碰撞”的说法不正确的是( )
A.分子间的碰撞均为有效碰撞
B.能发生化学反应的碰撞叫做有效碰撞
C.发生有效碰撞时,化学键才能断裂
D.其他条件相同时,反应物浓度越大,单位时间内的有效碰撞次数越多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.同温同压下,相同体积的气体,其气体分子物质的量也相等
B.任何条件下,等物质的量的甲烷和一氧化碳所含的分子数可能不相等
C.不同的气体,若体积不同,则它们所含的分子数也不同
D.同温同压下,若体积不相等,则一氧化碳气体和氮气质量可能相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中的一定量混合气体发生反应:xA(g) + yB(g)![]() zC(g)平衡时测得A的浓度为0.50 mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30mol/L。下列有关判断正确的是 ( )
zC(g)平衡时测得A的浓度为0.50 mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30mol/L。下列有关判断正确的是 ( )
A. x + y < z B. 平衡向正反应方向移动
C. B的转化率降低 D. C的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在酸性溶液中,下列各组离子能大量共存的是( )
A.K+、Fe3+、SO ![]() 、NO3﹣
、NO3﹣
B.Cu2+、Mg2+、SO ![]() 、Cl﹣
、Cl﹣
C.Ag+、Na+、NO3﹣、Cl﹣
D.K+、Na+、CO ![]() 、OH﹣
、OH﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题: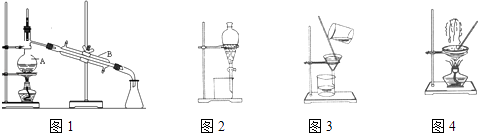
(1)装置图1中A的名称是 . A 中加入碎瓷片的作用是 .
(2)为了从海带中提取碘,某研究性学习小组设计并进行了以下实验: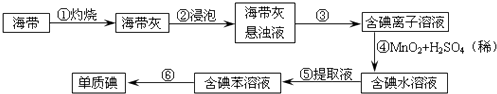
①灼烧海带时,除需要酒精灯与三脚架外,还需要用到的实验仪器是(从下列仪器中选出所需仪器,用标号字母填写在空白处);
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.铁架台 F.干燥器
②步骤③的实验选择上述装置图(填图的序号).步骤⑤的实验操作名称是 . 步骤⑥的目的是从含碘苯溶液中分离出单质碘,同时回收苯,该步骤的实验操作名称是 , 选择上述装置图(填图的序号)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“电解质的溶液中所有阳离子所带的正电荷数与所有阴离子所带的负电荷数相等,故显电中性,常称电荷守恒”.某盐的溶液中含有Na+、Mg2+、Cl﹣、SO ![]() 四种离子,若Na+为0.2mol,Mg2+为0.4mol,Cl﹣ 为0.4mol,则SO
四种离子,若Na+为0.2mol,Mg2+为0.4mol,Cl﹣ 为0.4mol,则SO ![]() 物质的量为( )
物质的量为( )
A.0.1mol
B.0.3mol
C.0.5mol
D.0.15mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究铁和硫反应产物中铁的化合价为+2价或+3价或既有+2也有+3价,某同学设计了如下图所示的实验过程:(已知硫会溶于热碱溶液)
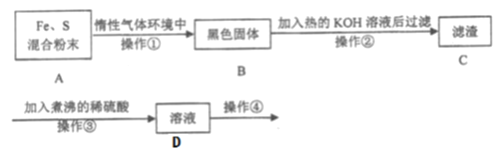
请回答以下问题:
(1)混合粉末A中S粉必须要过量,其原因是为了保证铁粉完全反应,从而避免_____。
(2)反应在“惰性气体环境中”进行的原因是______________________。
(3)操作①是用烧热的玻璃棒点触混合粉末,反应即可持续进行,这说明了_______。
(4)操作②的作用是________________________________________。
(5)操作③中稀硫酸煮沸的目的是____________________________________。
(6)为探究产物中铁的价态,需要继续对D溶液进行实验,请写出操作④的具体操作、现象及结论:__________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com