
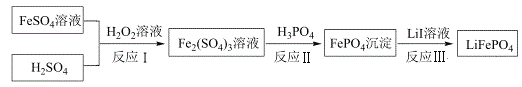
【题目】2019年诺贝尔化学奖颁给锂离子电池领域,获奖科学家的重要贡献之一是研发出了电极材料——磷酸亚铁锂(LiFePO4)。LiFePO4的一种制备方法如图。
已知:H3PO4能电离出PO![]() 。
。
(1)LiFePO4中,铁元素的化合价为_____。
(2)反应I中H2O2的作用是_____。
(3)检测反应II中铁离子是否完全反应的操作是_____。(离子检验常用的表达方式为:取xx试剂,向其中滴加xx,若出现xx现象,则说明xx结论。)
(4)反应Ⅲ的化学方程式是_____。
【答案】+2 氧化剂,将Fe2+氧化为Fe3+ 取少量反应Ⅱ中的滤液,向其中滴加KSCN溶液,若溶液不变红(或无现象),则说明反应Ⅱ中铁离子完全反应 2FePO4+2LiI=2LiFePO4+I2
【解析】
由工艺流程分析可知,FeSO4被H2O2在酸性条件下氧化生成Fe2(SO4)3,Fe2(SO4)3与H3PO4反应生成FePO4沉淀,FePO4与LiI溶液发生氧化还原反应2FePO4+2LiI=2LiFePO4+I2得到LiFePO4,据此分析解答问题。
(1)根据化合物元素化合价代数和为0可知,LiFePO4中Li为+1价,![]() 为-3价,则铁元素的化合价为+2价,故答案为:+2;
为-3价,则铁元素的化合价为+2价,故答案为:+2;
(2)根据分析,反应Ⅰ中H2O2在酸性条件下将Fe2+氧化为Fe3+,故答案为:作氧化剂,将Fe2+氧化为Fe3+;
(3)一般用KSCN溶液检验Fe3+,因此检测反应II中铁离子是否完全反应,可取少量反应Ⅱ中的滤液,向其中滴加KSCN溶液,若溶液不变红(或无现象),则说明反应Ⅱ中铁离子完全反应,故答案为:取少量反应Ⅱ中的滤液,向其中滴加KSCN溶液,若溶液不变红(或无现象),则说明反应Ⅱ中铁离子完全反应;
(4)反应Ⅲ为FePO4与LiI溶液发生氧化还原反应生成LiFePO4,反应的化学方程式为2FePO4+2LiI=2LiFePO4+I2,故答案为:2FePO4+2LiI=2LiFePO4+I2。


 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案科目:高中化学 来源: 题型:
【题目】配制100 mL 1.0 mol/LNa2CO3溶液,下列操作正确的是
A. 称取10.6 g无水碳酸钠,加入100 mL容量瓶中,加水溶解、定容
B. 称取10.6 g无水碳酸钠,加入100 mL蒸馏水,搅拌、溶解
C. 转移Na2CO3溶液时,未用玻璃棒引流,直接倒入容量瓶中
D. 定容后,塞好瓶塞,反复倒转、摇匀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,可逆反应X(g)+3Y(g)![]() 2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(单位mol/L),当达平衡时X、Y、Z的浓度分别为0.1mol/L,0.3mol/L,0.08mol/L,则下列判断不合理的是( )
2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(单位mol/L),当达平衡时X、Y、Z的浓度分别为0.1mol/L,0.3mol/L,0.08mol/L,则下列判断不合理的是( )
A.c1:c2=1:3B.0≤c2≤0.42
C.X、Y的转化率相等D.当反应达到平衡时,反应就停止了
查看答案和解析>>
科目:高中化学 来源: 题型:
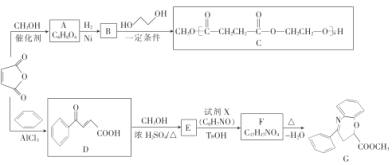
【题目】丁烯二酸酐(![]() )是一种重要的化工原料,可用于合成有机高分子及某些药物,相关合成路线如图:
)是一种重要的化工原料,可用于合成有机高分子及某些药物,相关合成路线如图:
已知:①![]() +2ROH
+2ROH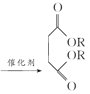 +H2O
+H2O
②R1OH+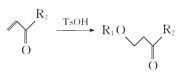 。
。
回答下列问题:
(1)![]() 的化学名称为__;X中含有的官能团为__。
的化学名称为__;X中含有的官能团为__。
(2)A的核磁共振氢谱有__组峰;D→E的反应类型是__。
(3)写出F的结构简式并用星号(*)标出手性碳:__。
(4)B→C的化学方程式为__。
(5)W是D的同分异构体,写出符合下列条件的W的结构简式:__。
a.属于芳香族化合物,且为间位的三元取代物
b.能与NaHCO3溶液反应
c.能发生银镜反应
(6)丁烯二酸酐(![]() )可由
)可由![]() 制备得到,写出合成路线流程图(无机试剂任选)___。
制备得到,写出合成路线流程图(无机试剂任选)___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素a--f在周期表中的位置如表所示,下列有关说法正确的是
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
二 | c | d | |||||
三 | a | b | e | f |
A. c、d、e的氢化物中,e的氢化物沸点最高
B. a、b、d三种元素的离子半径:a >b >d
C. 六种元素中,a元素的金属性最强
D. e、f的氧化物对应的水化物的酸性依次增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微生物燃料电池(MFC)为可再生能源的开发和难降解废弃物的处理提供了一条新途径。某微生物燃料电池示意图如图所示(假设废弃物为乙酸盐)。下列说法错误的是( )

A.甲室菌为好氧菌,乙室菌为厌氧菌
B.甲室的电极反应式为![]()
C.该微生物燃料电池(MFC)电流的流向:由b经导线到a
D.电池总反应式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A. Ag2SO4固体与饱和NaCl溶液反应:Ag2SO4+2Cl-=2AgCl+SO42-
B. 用惰性电极电解饱和NH4Cl溶液:2Cl-+2H2O![]() H2↑+Cl2↑+2OH-
H2↑+Cl2↑+2OH-
C. NaAlO2溶液中通入过量的CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
D. KMnO4酸性溶液与FeSO4溶液反应:MnO4-+Fe2++8H+=Mn2++Fe3++4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】应用铝热反应焊接铁轨时发生的主要反应为Fe2O3+2Al![]() 2Fe+Al2O3。
2Fe+Al2O3。
(1)作还原剂的物质是_____,铁元素的化合价_____(填“升高”或“降低”)。
(2)在该反应中,若消耗了1molAl则生成_____molFe,转移电子的物质的量为______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将下列物质进行分类:
①![]() H与
H与![]() H;②O2与O3;③乙醇(C2H5OH)与甲醚(CH3—O—CH3);④正戊烷(CH3CH2CH2CH2CH3)与异丁烷(
H;②O2与O3;③乙醇(C2H5OH)与甲醚(CH3—O—CH3);④正戊烷(CH3CH2CH2CH2CH3)与异丁烷(![]() )
)
(1)互为同位素的是_____(填序号、下同);
(2)互为同系物的是_____;
(3)互为同分异构体的是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com