
【题目】无机化合物可根据其组成和性质进行分类。
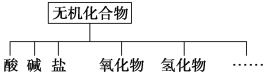
(1)如图所示的物质分类方法的名称是______________。
(2)
物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
化学式 | ①HCl ②______ | ③________ ④Ba(OH)2 | ⑤Na2CO3 ⑥_______ | ⑦CO2 ⑧Na2O | ⑨NH3 ⑩H2O2 |
以Na、K、H、O、C、S、N中任两种或三种元素组成合适的物质,分别填在上表中②③⑥后面。
(3)写出⑦转化为⑤的化学方程式_______。
【答案】树状分类法 H2SO4(或HNO3或H2CO3) NaOH(或KOH) Na2SO4(或K2CO3或Na2SO3或NaNO3) 2NaOH+CO2(少量)===Na2CO3+H2O
【解析】
(1)树状分类法是一种很形象的分类法,按照层次,一层一层来分,就像一棵大树;(2)酸电离出的阳离子全部是氢离子的化合物;碱电离出的阴离子全部为氢氧根离子;盐电离出得阳离子为金属离子,阴离子为酸根离子;(3)CO2与NaOH反应转化为Na2CO3;据此分析解答。
(1)树状分类法是一种很形象的分类法,按照层次,一层一层来分,就像一棵大树,有叶、枝、杆、根,图示方法就是树状图,故答案为:树状分类法;
(2)电离出的阳离子全部是氢离子的化合物为酸,如H2SO4(或HNO3或H2CO3);电离出的阴离子全部为氢氧根离子的化合物为碱,如NaOH(或KOH);电离出得阳离子为金属离子,阴离子为酸根离子的化合物为盐,如Na2SO4(或K2CO3或Na2SO3或NaNO3),故答案为:H2SO4;NaOH;Na2SO4;
(3)CO2与NaOH反应转化为Na2CO3,反应的化学方程式为:CO2+2NaOH═Na2CO3+H2O,故答案为:CO2+2NaOH═Na2CO3+H2O。


科目:高中化学 来源: 题型:
【题目】实验室用下图装置完成表中的四个实验,不能达到实验目的的是
实验装置 | 实验目的 | 试剂X | 试剂Y | |
| A. | 检验C2H5Br消去反应后的气体产物 | 水 | 酸性KMnO4溶液 |
B. | 检验C2H5OH消去反应后的气体产物 | NaOH溶液 | Br2的CCl4溶液 | |
C. | 比较醋酸、碳酸、苯酚酸性强弱 | NaOH溶液 | 苯酚钠溶液 | |
D. | 检验制取乙炔时的气体产物 | CuSO4溶液 | 酸性KMnO4溶液 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在铜-锌-稀硫酸构成的原电池中,当导线中有1mol电子通过时,下列说法正确的是
①锌片溶解了32.5g ②溶液中![]() 向铜片电极移动 ③正极上发生氧化反应产生了H2 ④铜片上逸出0.5molH2
向铜片电极移动 ③正极上发生氧化反应产生了H2 ④铜片上逸出0.5molH2
A.①③B.①④C.②③D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D、E、F六种短周期主族元素,其原子序数依次增大。A能分别与B、C、D三种元素形成电子数相同的分子,且B的最外层电子数是次外层电子数的2倍。E的阳离子、D的阴离子均与氖原子的电子层结构相同,且E的单质与D的单质反应能生成E2D和E2D2两种化合物。F所在主族序数与所在周期序数之差为4。(答题时,请用具体的化学用语表示)
(1)元素B在周期表中的位置__________周期________族;C元素的原子结构示意图_________________。
(2)写出由E、F两种元素形成的离子化合物的电子式________________,C2A4的结构式为:_______________,用电子式表示E2D的形成过程:_____________________。
(3)C、D、E形成的简单离子的半径由大到小的顺序为:_____________________。(用离子符号表示)
(4)E的最高价氧化物对应的水化物与F的最高价氧化物对应的水化物之间发生的化学反应方程式为:______________________________________________________________。
(5)向KI溶液中通入适量的F单质后,再滴加一定量的CCl4,振荡静置后的现象为_____________________________________,继续通入F单质并充分振荡,混合溶液逐渐褪为无色,若1mol还原剂转移10NA电子,上述反应的化学方程式为:___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】部分氧化的Fe-Cu合金样品(氧化产物为Fe2O3、CuO)共2.88g,经如下处理:

下列说法正确的是
A.滤液A中的阳离子为Fe2+、Fe3+、H+B.V=224
C.样品中CuO的质量为2.0gD.样品中铁元素的质量为0.56g
查看答案和解析>>
科目:高中化学 来源: 题型:
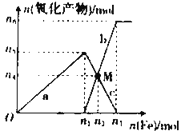
【题目】在1 L 2 mol·L-1稀硝酸溶液中逐渐加入铁粉,反应中氧化产物的物质的量与加入铁粉的物质的量的关系如图所示:
回答下列问题:
(1)与曲线a对应的离子方程式为_____。
(2)曲线b代表的微粒为_____________,n2的值为__________。
(3)若M点时再加入V L 2 mol·L-1的稀硝酸,恰好反应完全,则V为_____________。
(4)研究表明硝酸的浓度越小,反应后氮的化合价越低。在极稀的硝酸溶液中加入少量铁粉,生成NH4+的离子方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏伽德罗常数,下列叙述错误的是( )
A. 18g H2O中含的质子数为10NA
B. 1mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子
C. 46g NO2和N2O4混合气体中含有原子总数为3NA
D. 12g金刚石含有的共价键数为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列所示的物质间的转化均能实现的是( )
A.HCl(浓)![]() Cl2
Cl2![]() FeCl3(aq)
FeCl3(aq)
B.Al![]() Al2O3
Al2O3![]() Al(OH)3
Al(OH)3
C.NaCl(熔融)![]() Na
Na![]() NaOH
NaOH
D.N2![]() NO2
NO2![]() HNO3
HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物J是我国自主成功研发的一种新药。合成J的一种路线如图:
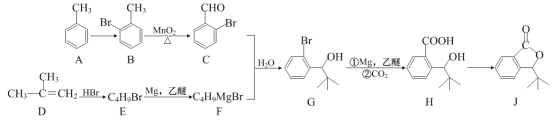
(1)由A生成B的反应所需的试剂及反应条件为___。
(2)由B生成C的反应类型为___。
(3)D___(填写“存在”或“不存在”)顺反异构现象。
(4)C与新制氢氧化铜反应的化学方程式为___(该条件下苯环上的溴不参与反应)。
(5)写出同时满足下列条件的J的一种同分异构体的结构简式___。
①分子中除苯环外不含其它环状结构;
②能发生银镜反应;
③分子中只含有有2种不同化学环境的氢。
(6)写出以乙醇和乙酸为原料制备![]() 的合成路线图___(无机试剂和乙醚任用,合成路线图示例见本题题干)。
的合成路线图___(无机试剂和乙醚任用,合成路线图示例见本题题干)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com