
【题目】某金属与氯气反应生成的化合物中,其质量比为1∶1.9,原子个数比为1∶3,则金属的相对原子质量为
A. 27 B. 56 C. 23 D. 64
科目:高中化学 来源: 题型:
【题目】下列可以大量共存的离子组是( )
A. 无色透明溶液中:NH4+、Cu2+、Cl﹣、NO3﹣
B. 碱性溶液中:K+、Na+、SO42﹣、Cl﹣
C. 酸性溶液中:K+、Na+、HCO3﹣、Ca2+
D. 酸性溶液中:Na+、Fe2+、SO42﹣、ClO﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F是六种短周期主族元素,它们的原子序数依次增大,其中C是地壳中含量最多的元素,A、F两元素的原子核中质子数之和比C、D两元素原子核中质子数之和少2,F元素的最外层电子数是次外层电子数的0.75倍.又知B元素的最外层电子数是内层电子数的2倍,E元素的最外层电子数等于其电子层数.
请回答:
(1)由E、F二种元素组成的化合物跟由A、C、D三种元素组成的化合物的水溶液充分反应的化学方程式为____________。
(2)单质B与A2C在一定条件下发生反应,工业上用于制水煤气、利用水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g) ![]() CH3OH(g) ΔH=-90.8 kJ·mol-1
CH3OH(g) ΔH=-90.8 kJ·mol-1
②2CH3OH(g) ![]() CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ·mol-1
CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ·mol-1
③CO(g)+H2O(g) ![]() CO2(g)+H2(g) ΔH=-41.3 kJ·mol-1
CO2(g)+H2(g) ΔH=-41.3 kJ·mol-1
请写出由水煤气合成二甲醚的总反应的热化学方程式:__________ 。
(3)用B元素的单质与E元素的单质可以制成电极浸入由A、C、D三种元素组成的化合物的溶液中构成电池,则电池负极的电极反应式_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计实验证明铜与浓硫酸能发生反应,并检验生成气体的性质,如图所示,在试管里加入2mL浓硫酸,用带导管和一个小孔的胶管塞紧,从孔中插入一根铜丝,加热,把放出的气体依次通入品红溶液和石蕊溶液中. 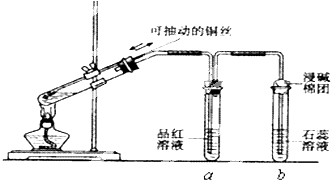
请回答下列问题:
(1)写出铜与浓硫酸反应的化学方程式: .
(2)试管a、b分别检验生成气体的性质,写出观察到的现象及其作用.试管a中的现象是 , 作用是 . 试管b中的现象是 , 作用是 .
(3)装置中浸碱面团的作用是 .
(4)如图将铜丝改为可抽动的铜丝符合化学实验“绿色化”的原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,有关零排放车载燃料电池叙述正确的是( ) 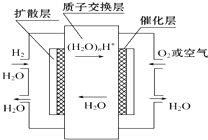
A.正极通入H2 , 发生还原反应
B.负极通入H2 , 发生还原反应
C.总反应式为2H2+O2=2H2O
D.导电离子为质子,且在电池内部由正极定向移向负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列依据热化学方程式得出的结论正确的是( )
A. 常温常压下,1 g H2在足量Cl2中燃烧生成HCl,放出92.3 kJ的热量,则热化学方程式可表示为H2(g)+Cl2(g)2HCl(g) ΔH=+184.6 kJ·mol-1
B. 甲烷的标准燃烧热为ΔH=-890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1
C. 已知NaOH(aq)+HCl(aq)NaCl(aq)+H2O(l) ΔH=-57.4 kJ·mol-1,则含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量
D. 相同条件下,2 mol氢原子所具有的能量小于1 mol氢分子所具有的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组同学展开对漂白剂亚氯酸钠(NaClO2)的研究。

已知:①NaClO2饱和溶液在温度低于38℃时析出晶体是NaClO23H2O,高于38℃时析出晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl;
②二氧化氯极易溶于水。
(1)装置A中NaClO3和Na2SO3制备ClO2气体,其物质的量的理论比值为____________;该装置中采用浓硫酸而不用稀硫酸的原因是___________。
(2)装置B的作用是 _____________;装置C中反应为放热反应,在不改变反应物浓度和体积的条件下,为了使反应在低温下进行,实验中可采取的措施是________________。
(3)写出装置C发生的离子方程式______________。
(4)从装置C反应后的溶液获得干燥的NaClO2晶体的操作步骤为:将装置C中的液体取出在减压和55℃条件下蒸发,至出现大量晶体后,___________________(填实验步骤)。(已知:NaClO2晶体易溶于水,难溶解于乙醇等有机溶剂。)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车、飞机等交通工具排放的尾气中含有的大量CO、NO 等大气污染物,是造成雾霾天气的主要原因,研究CO、NO 的转化对于环境的改善有重大意义。
(1)有人设想将CO按下列反应除去:2CO(g)=2C(s) +O2(g) △H>0。你认为该设想能否实现并说明理由:__________________________。
(2)用活性炭还原法可以处理汽车尾气中的氮氧化物。某研究小组在2 L的恒容密闭容器中加人0.100 mL NO 和2.030 mol固体活性炭,发生反应:C(s)+2NO(g) ![]() N2(g)+CO2(g)。在不同温度下测得平衡体系中各物质的物质的量如下表:
N2(g)+CO2(g)。在不同温度下测得平衡体系中各物质的物质的量如下表:
T/℃ | n(固体活性炭)/mol | n(NO)/mol | n(N2)/mol | n(CO2)/mol |
200 | 2.000 | 0.040 | 0.030 | 0.030 |
350 | 2.005 | 0.050 | 0.025 | 0.025 |
①该反应的正反应为___________(填“吸热”或“放热”)反应。
②200℃时,反应达到平衡后向恒容容器中再充入0.100 mol NO,再次达到平衡后,混合气中NO的百分含量将__________(填“增大”“减小”或“不变”)。
③上述反应在350℃时的平衡常数K=_______________。
(3)在密闭容器中发生上述反,,达到平衡时,下列措施能提高NO转化率的是___________(填字母)。
A.选用更高效的催化剂 B.增加C(s)的量
C.降低反应体系的温度 D.缩小容器的体积
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com