
【题目】水中的溶解氧的含量是衡量水质的一个重要指标,某实验兴趣小组通过如下步骤来测量水中溶解氧的含量:
步骤一:向溶解氧测量瓶中注入20.00 mL水样,再分别加入1 mL 0.1 mol L-1MnSO4溶液和3mL NaOH和KI的混合溶液,充分反应。此时发生反应的化学方程式为: Mn2++2OH-=Mn(OH)2↓ 2Mn(OH)2+ O2 =2MnO(OH)2
步骤二:向上述混合物中加入1.5 mL浓硫酸,充分反应后制沉淀完全溶解,此时溶液呈黄色。
步骤三:将溶液全部转移到容量瓶中,向其中滴加23滴淀粉溶液,溶液呈蓝色。用 0.005 mol L-1的Na2S2O3标准溶液滴定至蓝色恰好消失,共消耗Na2S2O3标准溶液3.60 mL。此时发生反应为:
I2+2Na2S2O3= 2NaI + Na2S4O6
(1)25 ℃时,步骤一中当加入NaOH使溶液的pH = 12时,此时溶液中的c(Mn2+)=_________mol L-1 。 (已知 KspMn(OH)2 =2.06×10-13)
(2)写出步骤二中所发生反应的化学方程式:______________________________。
(3)计算该水样中溶解氧的含量。(单位:mg L-1,请写出计算过程)______________________________
【答案】 2.06×10-9 MnO(OH)2+2H2SO4+2KI=MnSO4+K2SO4+I2+3H2O 由化学方程式可知:O24Na2S2O3
n(O2)=![]() ×0.005mol L-1×3.60×10-3L=4.5×10-6mol
×0.005mol L-1×3.60×10-3L=4.5×10-6mol
溶解氧的含量=![]() =7.2 mg L-1
=7.2 mg L-1
【解析】本题考查溶度积的计算、氧化还原反应方程式的书写、化学计算等知识,(1)根据溶度积的表达式,Ksp=c(Mn2+)×c2(OH-),此时溶液的pH=12,即溶液中c(OH-)=10-2mol·L-1,c(Mn2+)=Ksp/c2(OH-)=2.06×10-13/10-4=2.06×10-9mol·L-1;(2)根据步骤二现象加入浓硫酸后,沉淀溶解,且溶液显黄色,说明I-转化成I2,MnO(OH)2作氧化剂,被还原成Mn2+,化合价降低2价,I-转化成I2,化合价由-1价→0价,化合价共升高1价,最小公倍数为2,根据化合价的升降以及原子守恒,电荷守恒进行配平;因此化学反应方程式为MnO(OH)2+2H2SO4+2KI=MnSO4+K2SO4+I2+3H2O;(3)根据化学反应方程式,建立关系式:O2~4Na2S2O3,n(O2)=n(Na2S2O3)/4=3.6×10-3×0.005/4mol=4.5×10-6mol,即溶解氧的含量是4.5×10-6×32×10-3/20×10-3mg·L-1=7.2mg·L-1。


科目:高中化学 来源: 题型:
【题目】处理燃烧产生的烟道气CO和SO2,方法之一是在一定条件下将其催化转化为CO2和S。
已知:①2CO(g)+O2(g)![]() 2CO2(g) H=-566.0kJ/mol
2CO2(g) H=-566.0kJ/mol
②S(g)+O2(g)![]() SO2(g) H=-296.0kJ/mol
SO2(g) H=-296.0kJ/mol
下列说法中正确的是
A. 转化①有利于碳参与自然界的元素循环
B. 转化②中S和O2属于不同的核素
C. 可用澄清的石灰水鉴别CO2与SO2
D. 转化的热化学方程式是:2CO(g)+ SO2(g) ![]() S(s)+ 2CO2 (g) H =+270kJ/mol
S(s)+ 2CO2 (g) H =+270kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种重要的可再生资源。
(1)已知:2CH4(g)+O2(g) =2CO(g)+4H2(g) △H=akJmol-1
CO(g) +2H2(g)=CH3OH(g) △H=bkJmol-1
写出由CH4和O2制取CH3OH(g)的热化学方程式:____________________________。
(2)反应:CO(g)+2H2(g)![]() CH3OH(g)的平衡常数K的表达式为________________;甲图是反应时CO和CH3OH(g)的物质的量浓度随时间(t)的变化曲线。从反应开始至达到平衡时,用H2表示的反应速率υ(H2)=________________。
CH3OH(g)的平衡常数K的表达式为________________;甲图是反应时CO和CH3OH(g)的物质的量浓度随时间(t)的变化曲线。从反应开始至达到平衡时,用H2表示的反应速率υ(H2)=________________。
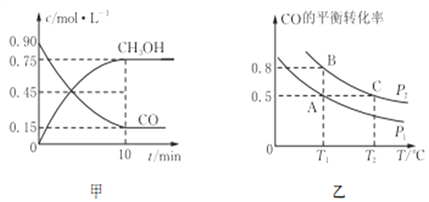
(3)在一容积可变的密闭容器中充入10 mol CO和20 mol H2,发生反应并达到平衡,CO的平衡转化率随温度(T)、压强(P)的变化曲线如图乙所示。
①能判断该反应达到化学平衡状态的是_______(填选项字母)。
A.H2的消耗速率等于CH3OH的生成速率的2倍
B.H2的体积分数不再改变
C.H2的转化率和CO的转化率相等
D.混合气体的平均相对分子质量不再改变
②比较A、B两点压强大小P(A)________P(B)(填“>、<、=”)。
③比较KA、KB、KC的大小:________________。
(4)以甲醇为燃料,O2为氧化剂,KOH溶液为电解质溶液,可制成燃料电池(电极材料为惰性电极)。若KOH溶液足量,写出燃料电池负极的电极反应式:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】12mL浓度为0.05mol/L 的Na2SO3溶液恰好与VmL浓度为0.02mol/L的K2X2O7溶液完全反应。已知X元素在产物中的化合价为+3。则V为( )
A. 5 B. 10 C. 15 D. 20
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于有机物的性质,下列说法不正确的是
A. CH4气体能与Cl2在光照条件下发生取代反应生成CCl4
B. CH2=CH2能使酸性高锰酸钾溶液褪色是因为发生了氧化反应
C. 通常情况下,苯是无色气体,能在催化剂条件下与Br2发生单取代反应
D. 乙醇和乙酯发生酯化反应生成乙酸乙酯是可逆反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前有四个实验方案,可行的是
A. 除去混在Cu粉中的少量Mg粉和Al粉,加稀盐酸后过滤
B. 分离汽油和煤油,可用萃取的方法
C. 分离硝酸钾和氯化钠固体的混合物,可用溶解、过滤的方法
D. 将氧气和氢气的混合气体通过灼热的氧化铜,以除去其中的氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴及其化合物可应用与催化剂、电池、颜料与染料等。
(1)CoO是一种油漆添加剂,可通过反应①②制备。
①2Co(s)+O2(g)=2CoO(s) ΔH1=akJ·mol-1
②2CoCO3(s) =CoO(s) + CO2 (g) ΔH2=akJ·mol-1
则反应2Co(s)+O2(g)+2CO2(g)=2CoO3(s) 的ΔH=_________。
(2)某锂电池的电解质可传导Li+,电池反应式为:LiC6+CoO2![]() C6+LiCoO2
C6+LiCoO2
①电池放电时,负极的电极反应式为_________,Li+向______移动(填“正极”或“负极“)。
②一种回收电极中Co元素的方法是:将LiCoO2与H2O2、H2SO4反应生成CoSO4。该反应的化学方程式为___________________。
(3)BASF高压法制备醋酸采用钴碘催化循环过程如图-1所示,该循环的总反应方程式为_________________(反应条件无需列出)

(4)某含钴催化剂可同时催化去除柴油车尾气中的碳烟(C)和NOx。不同温度下,将10mol模拟尾气(成分如下表所示)以相同的流速通过该催化剂,测得所有产物(CO2、N2、N2O)与NO的相关数据结果如图-2所示.
模拟尾气 | 气体 | 碳烟 | ||
NO | O2 | He | ||
物质的量分数或物质的量 | 0.25% | 5% | 94.75% | a mol |

①380℃时,测得排出的气体中含0.45 mol O2和0.0525 mol CO2,则Y的化学式为__________________。
②实验过程中采用NO模拟NOx,,而不采用NO2的原因是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的水溶液中,加入Ba(OH)2溶液后,原溶液中阴、阳离子都减少的是( )
A.CuSO4
B.Ca(NO3)2
C.Na2CO3
D.FeCl3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com