

分析 (1)二氧化硫是酸性氧化物,可以和强碱反应生成盐和水,根据二氧化硫的量多少来书写化学方程式;
(2)实现固体和液体的分离可以采用过滤的方法;硫酸钡和盐酸不反应,但是亚硫酸钡可以和盐酸反应;
(3)硫酸钡是白色不溶于强酸的沉淀,亚硫酸根离子还原性强,容易被氧化为硫酸根离子.
解答 解:(1)二氧化硫是酸性氧化物,可以和强碱反应,少量SO2通入到Ba(OH)2溶液中的离子反应方程式为SO2+Ba2++2OH-═BaSO3↓+H2O,过量的SO2通入到Ba(OH)2溶液中,因为二氧化硫会和亚硫酸钡之间反应生成亚硫酸氢钡,所以过量的SO2通入到Ba(OH)2溶液中的离子反应方程式为SO2+OH-═HSO3-,
故答案为:SO2+Ba2++2OH-═BaSO3↓+H2O;SO2+OH-═HSO3-;
(2)实现固体和液体的分离可以采用过滤的方法,将SO2通入到BaCl2溶液中,出现的白色浑浊可能是硫酸钡还可能是亚硫酸钡,硫酸钡和盐酸不反应,但是亚硫酸钡可以和盐酸反应,溶解,可以用盐酸来鉴别沉淀成分,故答案为:过滤;HCl;
(3)硫酸钡和盐酸不反应,但是亚硫酸钡可以和盐酸反应,所以白色不溶于盐酸的沉淀物是硫酸钡,硫酸钡沉淀的生成和亚硫酸根离子的不稳定性有关,
即2SO2+2Ba2++O2+2H2O═2BaSO4↓+4H+,
故答案为:BaSO4;2SO2+2Ba2++O2+2H2O═2BaSO4↓+4H+.
点评 本题考查学生二氧化硫的以及含硫元素的盐的性质知识,侧重考查元素及其化合物知识,可以根据所学知识来回答,难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 一定含有SO42- | B. | 一定含有Ag+ | ||
| C. | 可能含有SO42-或Ag+ | D. | 可能含有SO42-或Ag+或CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 根据水溶液能否导电将化合物分为电解质和非电解质 | |
| B. | 根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应 | |
| C. | 根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液 | |
| D. | 根据能否与碱溶液反应,可将氧化物分为酸性氧化物和碱性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
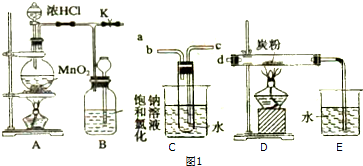
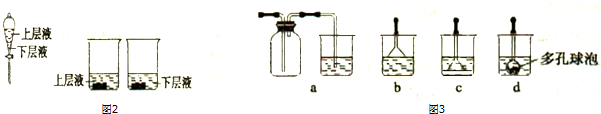
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Q1+Q2<2Q3 | B. | Q1+Q2>Q3 | C. | Q1+Q2<Q3 | D. | Q1+Q2>2Q3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
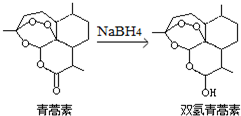 我国科学家屠呦呦获得2015年诺贝尔生理学或医学奖.她研究的青蒿素、双氢青蒿素在寄生虫疾病治疗方面取得了伟大成就.下列有关说法正确的是( )
我国科学家屠呦呦获得2015年诺贝尔生理学或医学奖.她研究的青蒿素、双氢青蒿素在寄生虫疾病治疗方面取得了伟大成就.下列有关说法正确的是( )| A. | 青蒿素易溶于水 | |
| B. | 青蒿素可与NaOH溶液反应 | |
| C. | 青蒿素转化为双氢青蒿素是氧化反应 | |
| D. | 青蒿素有11种一氯代物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com