
| 选项 | 实验操作、现象 | 结论 |
| A | 某溶液加入稀盐酸产生能使澄清石灰水变浑浊的无色无味气体;另取原溶液少许,向其中滴加CaCl2溶液,有白色沉淀生成 | 确定该溶液存在CO32- |
| B | 氯水中存在多种分子和离子,向新制氯水中加入有色布条,片刻后有色布条褪色 | 说明氯水中有HClO存在 |
| C | 将淀粉与KCl混合液装于半透膜内,浸泡在盛蒸馏水的烧杯中,5min后取烧杯中液体,加碘水变蓝色 | 证明半透膜有破损 |
| D | 将气体通入盛饱和碳酸钠溶液的洗气瓶 | 可用于除去中CO2的HCl |
| A. | A | B. | B | C. | C | D. | D |
分析 A.该无色无味气体是二氧化碳,溶液中可能含有碳酸根离子或碳酸氢根离子,且能与氯化钙反应生成白色沉淀的只能为碳酸根离子;
B.氯气不具有漂白性,能够使有色布条褪色的为次氯酸;
C.根据胶体不会通过半透膜分析;
D.二氧化碳能够与碳酸钠溶液反应生成碳酸氢钠,违反了除杂原则.
解答 解:A.某溶液加入稀盐酸产生能使澄清石灰水变浑浊的无色无味气体,该气体只能为二氧化碳,说明原溶液中可能含有碳酸根离子或碳酸氢根离子;另取原溶液少许,向其中滴加CaCl2溶液,有白色沉淀生成,由于碳酸氢根离子不与氯化钙溶液反应,则该溶液中一定含有CO32-,故A正确;
B.向新制氯水中加入有色布条,片刻后有色布条退色,由于氯气不具有漂白性,则说明氯水中一定含有能够使有色布条褪色的HClO,故B正确;
C.5min后取烧杯中液体,加碘水变蓝色,说明烧杯中含有淀粉,由于淀粉胶体不会透过半透膜,则说明半透膜有破损,故C正确;
D.二氧化碳和HCl都与碳酸钠反应,应该用饱和碳酸氢钠溶液,故D错误;
故选D.
点评 本题考查了化学实验方案的评价,题目难度不大,涉及物质除杂、离子检验、胶体性质、物质漂白性等知识,明确常见元素及其化合物性质为解答关键,注意掌握物质分离与提纯的原则,试题培养了学生的分析能力及化学实验能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
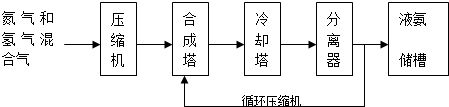
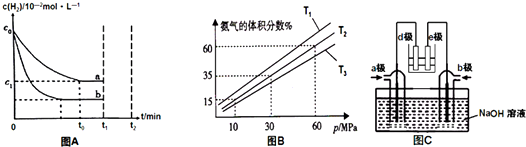
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
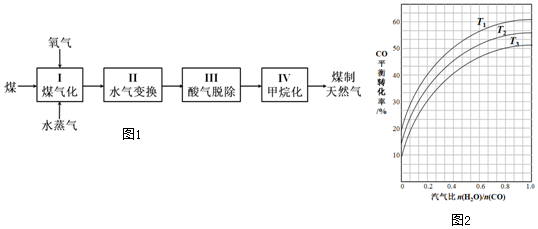 ②
②查看答案和解析>>
科目:高中化学 来源: 题型:选择题
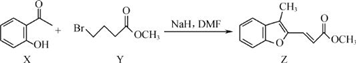
| A. | 物质 X在空气中不易被氧化 | |
| B. | 物质 Y中只含一个手性碳原子 | |
| C. | 物质 Z中所有碳原子不可能在同一平面内 | |
| D. | 等物质的量的 X、Y分别与 NaOH反应,最多消耗 NaOH的物质的量之比为 1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.3mol | B. | 0.15mol | ||
| C. | 小于0.15mol | D. | 大于0.15mol,小于0.3mol |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 体积②>③>①>④ | B. | 密度②>④>③>① | ||
| C. | 氢原子个数②>①>③>④ | D. | 质量②>③>①>④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
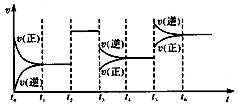 某密闭容器中发生反应:X(g)+3Y(g)?2Z(g)△H<0.如图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是( )
某密闭容器中发生反应:X(g)+3Y(g)?2Z(g)△H<0.如图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是( )| A. | t2时加入了催化剂 | |
| B. | t3时平衡的移动可使化学平衡常数减小 | |
| C. | t5时增大了压强 | |
| D. | t6时达到平衡后反应物的转化率最大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com