
����Ŀ����ͼ�DZ������ȡ����Ӧ��ʵ��װ��ͼ������ A Ϊ����֧�ܵ��Թܸ��Ƴɵķ�Ӧ�����������¶˿���һ��С�ף�����ʯ���ޣ��ټ�����������м�ۡ���д���пհף�

��1����Ӧ����A ����μ�����ͱ��Ļ��Һ���������ھͷ�����Ӧ��д��A �з�����Ӧ�Ļ�ѧ����ʽ(�л���д�ṹ��ʽ)____��
��2����֤��A �з�������ȡ����Ӧ�������Ǽӳɷ�Ӧ���Թ�C �б���������__________����Ӧ��ʼ�۲�D ��E ��֧�Թܣ�����������ֱ���___________��________��
��3����Ӧ 2 min��3 min ���� B �е�����������Һ��ɹ۲쵽��������______��_____��
��4������һ����Ҫ�Ļ���ԭ�ϣ��������ñ���Ϊԭ���Ʊ�ijЩ�������ת����ϵͼ��

��֪��a��RNO2 ![]() RNH2
RNH2
b��������ԭ�е�ȡ�������µ����ȡ�������뱽����λ��������Ӱ�졣
c��![]() +H2SO4(Ũ)
+H2SO4(Ũ)![]()
 +H2O
+H2O
��A ת��Ϊ B �Ļ�ѧ����ʽ��________��
��E �Ľṹ��ʽΪ__________
���𰸡�![]() �����廯�������л��е�Br2���� D������Һ��� E���в���dz��ɫ���� ���ɫ���� �ײ������״Һ��
�����廯�������л��е�Br2���� D������Һ��� E���в���dz��ɫ���� ���ɫ���� �ײ������״Һ�� 
![]()
��������
��1����Ӧ����A �б���Һ������м�����������·���ȡ����Ӧ�����屽���廯�⣻
��2����֤��A �з�������ȡ����Ӧ�������Ǽӳɷ�Ӧ��˵��������Ϊ�屽���廯�⣬�������ӷ����廯�������л�����������
��3���廯��������������Һ��Ӧ���ɺ��ɫ�����������������屽������������Һ�����ܣ����屽���ܶȴ���ˮ���ܶȣ�
��4�������л���ת����ϵ��֪����Ũ���������£�����Ũ���Ṳ�ȷ���������Ӧ������������
���ɱ����� ��ת����ϵ��֪�����������������������µ����ȡ��������뱽���ļ�λ���ɱ�����
��ת����ϵ��֪�����������������������µ����ȡ��������뱽���ļ�λ���ɱ�����![]() ��ת����ϵ��֪������������������ԭ�ӣ��µ����ȡ��������뱽���Ķ�λ��
��ת����ϵ��֪������������������ԭ�ӣ��µ����ȡ��������뱽���Ķ�λ��
��1����Ӧ����A �б���Һ������м�����������·���ȡ����Ӧ�����屽���廯�⣬��Ӧ�Ļ�ѧ����ʽΪ![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
��2����֤��A �з�������ȡ����Ӧ�������Ǽӳɷ�Ӧ��˵��������Ϊ�屽���廯�⣬�������ӷ����廯�������л�����������������������ԭ��֪�������������Ȼ�̼������C�б��������������廯�������е�����������ֹ�����������廯��ļ��飻�廯������ˮ�õ������ᣬ���������������ʣ���ʹʯ����Һ���ɫ���������ܺ���������Ӧ���ɵ���ɫ�����廯������۲�D��E���Թܣ�������������D���б�죬E���в���dz��ɫ�������ʴ�Ϊ�������廯�������л��е�Br2������D������Һ��죬E���в���dz��ɫ������
��3����������Ӧ�����廯�����廯������Ӧ�Ĵ������廯��������������Һ��Ӧ���ɺ��ɫ�����������������屽������������Һ�����ܣ����屽���ܶȴ���ˮ���ܶȣ�����B�е�����������Һ��ɹ۲쵽�������ǵײ������״Һ�壬�ʴ�Ϊ�����ɫ�������ײ������״Һ�壻
��4�������л���ת����ϵ��֪����Ũ���������£�����Ũ���Ṳ�ȷ���������Ӧ��������������AΪ����������������CH3Cl�ڴ��������·���ȡ����Ӧ����![]() ����BΪ
����BΪ![]() ����A ת��ΪB�Ļ�ѧ����ʽΪ
����A ת��ΪB�Ļ�ѧ����ʽΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
���ɱ����� ��ת����ϵ��֪�����������������������µ����ȡ��������뱽���ļ�λ���ɱ�����
��ת����ϵ��֪�����������������������µ����ȡ��������뱽���ļ�λ���ɱ�����![]() ��ת����ϵ��֪������������������ԭ�ӣ��µ����ȡ��������뱽���Ķ�λ����Eһ��Ϊ
��ת����ϵ��֪������������������ԭ�ӣ��µ����ȡ��������뱽���Ķ�λ����Eһ��Ϊ![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ��ˮ�ۺ����õĹ�ҵ����ͼ���ж�����˵����ȷ���ǣ� ��
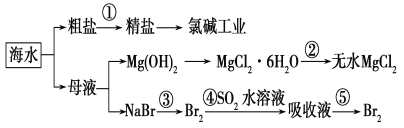
��֪��MgCl2��6H2O��������Mg(OH)Cl��HCl����ȡ�
A. ��ȥ���������ʣ�Mg2+��SO42����Ca2+���������ҩƷ˳��Ϊ��NaOH��Һ��Na2CO3��Һ��BaCl2��Һ�����˺������
B. �ڹ��̢��н�MgCl2��6H2O���ռ����Ƶ���ˮMgCl2
C. �������Ƕ��������ȼҵ�еĵ�ⱥ��ʳ��ˮ��һ������ѧ��ת��Ϊ���ܵĹ���
D. �ӵڢ۲����ڢݲ���Ŀ����Ϊ��Ũ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��X��Y��Z��W��Q��Ԫ�����ڱ��е����λ����ͼ��ʾ����ش���������

I. (1)����˵����ȷ����________ .
a.XY2��WY2��������ˮ���ɶ�Ӧ����
b.Q�ĺ���������Ա�X�ĺ����������ǿ
c.X�������̬�⻯����ȶ��Դ���W�������̬�⻯����ȶ���
d.���ݽ�NaOH��Һ�ֱ����MgO2��ZQ3��Һ�еķ�Ӧ����ɱȽ�Mg��Z�����Ե�ǿ��
��. QY2�ǹ����Ϲ��ϵĸ�Ч�����������
(2)ʵ����������KQY3����������������������Ʊ�QY2��д����Ӧ�Ļ�ѧ����ʽ�����õ����ű�������ת�Ƶķ������Ŀ______________________��
(3)����ˮ������QY2������ˮ�����������������ˮ��Ҫ��QY2��Ũ����0.10��0.80mg��L-1֮�䡣���������Լ��ˮ��QY2��Ũ�ȣ��������£�
����I ��ȡһ�������ˮ��������һ�����ĵ⻯�أ�����NaOH��Һ�������ԣ������������Һ����Һ������
���������ټ���һ������Na2S2O3��Һ������֪��2S2O32-+I2 = S4O62-+2I-)��
��������Ȼ���ټ��������ˮ��pH��1��3��
����ʱ����ͬpH������QԪ���������༰���ϼ���ͼ��ʾ��

�ٲ���I�з�Ӧ�����ӷ���ʽ��_______________________��
��ȷ������II��ȫ��Ӧ��������___________________________��
���ڲ����������У���Һ�ֳ���ɫ����Ӧ�����ӷ���ʽ��_________________��
����ˮ�������Ϊ1.0L���ڲ���II��������1.0��10-3mol��L-1��Na2S2O3��Һ10mL����ˮ����QY2��Ũ����__________mol��L-1(��ȷ��0.01)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ���ܴﵽԤ��Ŀ�ĵ���
A.  ���屽
���屽
B.  �� a ���Ƶ� b �����۲쵽ͭ˿�ɺڱ��
�� a ���Ƶ� b �����۲쵽ͭ˿�ɺڱ��
C.  ������ˮ�Ҵ����Ƿ���ˮ
������ˮ�Ҵ����Ƿ���ˮ
D.  ���뺬������Ȼ�̼Һ�壬��������ƿ�пɻ�õ�
���뺬������Ȼ�̼Һ�壬��������ƿ�пɻ�õ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ij����FeCl2��FeCl3��CuCl2�Ĺ�ҵ��Һ�л���ͭ���Ʊ��Ȼ���������������£�
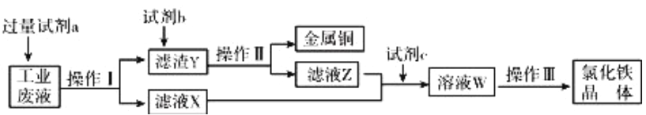
������˵����ȷ���ǣ� ��
A. �Լ�a�������Լ�b��ϡ����
B. ������������������������ͬ
C. �Լ�c����������Ӧ�ķ�ӦΪ:2Fe2++Cl2=2Cl-+2Fe3+
D. ������KMn04��Һ�ɼ�����ҺW���Ƿ���Fe2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����12�֣�������̼����;�dz��㷺�Ļ�������ԭ�ϣ��ش��������⣺
��1����ҵ�Ͽ�����CO2������ȼ�ϼ״���
��֪��CO2��g��+3H2��g��![]() CH3OH��l��+H2O(l) ��H=-130kJ��mol-1
CH3OH��l��+H2O(l) ��H=-130kJ��mol-1
2H2(g)+O2(g)=2H2O(l) ��H=-572kJ��mol-1
CH3OH(l)��ȼ������H=___________��
��2���ڴ��������£�CO2��CH4��ֱ��ת��Ϊ���CO2(g)+CH4(g)=CH3COOH(g) ��H��0�ڲ�ͬ�¶���������������ʱ仯��ͼ��ʾ��
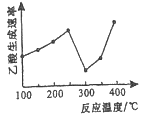
�ٵ��¶���250�桪300�淶Χʱ��������������ʼ�������Ҫԭ����_________��
����ʹ�����ƽ�������ߣ�Ӧ��ȡ�Ĵ�ʩ��_____________����дһ����ʩ���ɣ���
��3��һ�������£����ܱ������з�����Ӧ��2CO��g��![]() C��s��+CO2��g����
C��s��+CO2��g����
��������˵���÷�Ӧ�ﵽƽ�����___________��
A.�����ڻ�������������
B.CO��CO2�����ʵ���֮�Ȳ��ٱ仯
C.��������ƽ��Ħ���������ٱ仯
D.�γ�amolC=O����ͬʱ����amolC![]() O��
O��
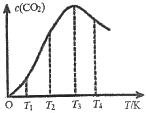
����ij����������ͨ��һ������CO����������Ӧ���ڲ�ͬ�¶���CO2�����ʵ���Ũ��c��CO2�����¶ȵı仯����ͼ��ʾ����÷�ӦΪ________������ȡ������ȡ�����Ӧ��
�����ݻ��ɱ��ij��ѹ������ͨ��amolCO��TCʱ��Ӧ����10min��ƽ�⣬CO���������Ϊ75%��CO��ƽ��ת����Ϊ_______�����ݻ��ı�������£���Ӧ���ʿ��õ�λʱ���ڷ�Ӧ�������������ʵ����仯����ʾ����0-10min��ƽ����Ӧ����v��CO2��=__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ĵ��볣�����±���

�����й�˵����ȷ���ǣ� ��
A. ǡ���к͵��������pH��HCOOH��HCN����NaOH����ǰ�ߴ��ں���
B. ���������Ũ�ȵ�HCOONa��NaCN����Һ��������������ĿHCOONa����NaCN
C. NaHS��Һ�м������� KOH��c��Na+��=c��H2S��+c��HS-��+2c��S2-��
D. HCOO-��CN-��HS-����Һ�в����Դ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���α��������֪����Ѫ�����ŵĽ�Ѫѹҩ��ϳ��м���I�Ǻϳ��α��������Ҫ���裬�����Ǻϳ��м���I����֪��ҵ����:
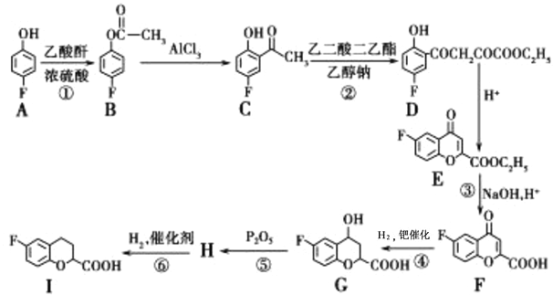
��֪���������Ľṹ��ʽ![]()
��ش��������⣺
��1��I�����еĺ��������ŵ�������____________________________��
��2����Ӧ�ٵĻ�ѧ����ʽΪ__________________����Ӧ�ݵĻ�ѧ����ʽΪ______________������ţ�
��3�������٢�������ȡ����Ӧ����____________________________��������ţ�
��4��д����������������C��ͬ���칹��Ľṹ��ʽ��____________________________��
��.������ֻ������ȡ����
��.�����к˴Ź���������4���
��.����NaHCO3��Ӧ����CO2
��5����������֪ʶ����������Ϣ��д����![]() ��������Ϊԭ���Ʊ�
��������Ϊԭ���Ʊ� �ĺϳ�·������ͼ�����Լ���ѡ��__________���ϳ�·������ͼʾ�����£�
�ĺϳ�·������ͼ�����Լ���ѡ��__________���ϳ�·������ͼʾ�����£�
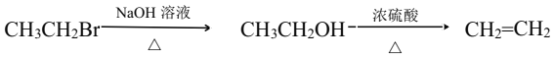
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com