
【题目】某学习小组探究氨的还原性及检验产物的性质,按下图装置进行实验(图中夹持装置已略去)。将B处的三氧化二铬加热至红热,再鼓入空气,已知:无水氯化钙可吸收氨气和水。回答下列问题:
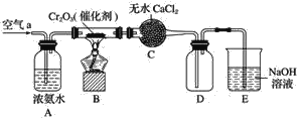
(1)B中发生反应的化学方程式是________________________________。
(2)证明氨气发生了催化氧化的现象是____________________________。
(3)写出(2)中反应的化学方程式______________________。
(4)装置E作用是________________________________________。
【答案】4NH3+5O2![]() 4NO+6H2O D中广口瓶中有红棕色气体 2NO+O2=== 2NO2 氢氧化钠溶液吸收有毒气体氮的氧化物,防止污染空气
4NO+6H2O D中广口瓶中有红棕色气体 2NO+O2=== 2NO2 氢氧化钠溶液吸收有毒气体氮的氧化物,防止污染空气
【解析】
在A中空气将氨水中的部分氨气带出,在B中NH3在Cr2O3催化下与O2反应产生NO和H2O,未反应的NH3及反应产生的H2O被C中CaCl2的吸收,NO与D中O2反应产生NO2,NO、NO2会被E中NaOH反应消耗掉,防止污染大气。
(1)装置B中发生的反应是氨的催化氧化反应,反应方程式为:4NH3+5O2![]() 4NO+6H2O;
4NO+6H2O;
(2)NH3发生氧化反应,其产物之一NO极易与O2反应生成NO2,该气体是红棕色气体,所以装置B中反应后的气体经C中CaCl2后,未反应的NH3及反应产生的H2O被无水CaCl2吸收,进入装置D中,发生反应:2NO+O2=2NO2,所以证明氨气发生了催化氧化的现象是装置D中广口瓶内有红棕色气体产生;
(3)在上述(2)中反应的化学方程式是2NO+O2=2NO2;
(4)装置E的作用是氢氧化钠溶液吸收有毒气体氮的氧化物,防止污染空气。


科目:高中化学 来源: 题型:
【题目】某一元弱酸(用HA表示)在水中的电离方程式是HA![]() H++A-,回答下列问题:
H++A-,回答下列问题:
(1)向纯水中加入适量HA,水的电离平衡将向___(填“正”、“逆”)反应方向移动,理由是____。
(2)在25℃下,将a mol·L-1的氨水与0.01mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-),则溶液显__性(填“酸”、“碱”或“中”),a___0.01(填“大于”、“小于”或“等于”);用含a的代数式表示NH3·H2O的电离常数Kb=__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组的同学,在实验室做锌与浓硫酸反应的实验中,甲同学认为产生的气体是二氧化硫,而乙同学认为除二氧化硫气体外,还可能产生氢气。为了验证甲、乙两位同学的判断是否正确,丙同学设计了如图所示实验装置(锌与浓硫酸共热时产生的气体为X,且该装置略去),试回答下列问题:
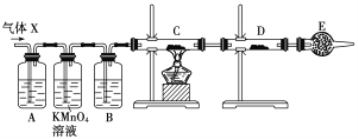
(1)上述反应中生成二氧化硫的化学方程式为______________________________。
(2)乙同学认为还可能产生氢气的理由是__________________________________。
(3)丙同学在安装好装置后,必不可少的一步操作是________________________。
(4)A中加入的试剂可能是_____,作用是__________________________________;B中加入的试剂可能是_____,作用是__________________________________;E中加入的试剂可能是_____,作用是__________________________________。
(5)可以证明气体X中含有氢气的实验现象是:C中:_________________________,D中:_________________________ 。如果去掉装置B,还能否根据D中的现象判断气体X中有氢气?_____ (填“能”或“不能”),原因是______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某温度时,水的离子积为KW=1×10-13,则该温度___25℃(填“>”、“<”或“=”)。在此温度下,某溶液中由水电离出来的H+浓度为1×10-10mol/L,则该溶液的pH可能为_____。
(2)若温度为25℃时,体积为Va、pH=a的H2SO4与体积为Vb、pH=b的NaOH混合,恰好中和。已知Va>Vb,且a=0.5b,此溶液中各种离子的浓度由大到小的排列顺序是:____,a的取值范围____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组实验测得某硅酸盐所含氧化物的质量分数如下表:
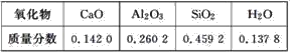
根据表中的数据请写出
(1)该硅酸盐的普通化学式是______________。
(2)用氧化物的形式表示该硅酸盐的组成是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在50 mL 4 mol·L-1的氢氧化钠溶液中,通入一定量的硫化氢,反应完毕,在常温减压条件下,用氮气把溶液吹干,得到白色固体7.92 g,通过计算确定白色固体的组成及各组分的质量。_________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生课外活动小组利用下图所示装置分别做如下实验:
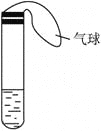
(1)在试管中注入某红色溶液,加热试管,溶液颜色逐渐变浅,冷却后恢复红色,则原溶液可能是________溶液;加热时溶液由红色逐渐变浅的原因是________________。
(2)在试管中注入某无色溶液,加热试管,溶液变为红色,冷却后恢复无色,则此溶液可能是________溶液;加热时溶液由无色变为红色的原因是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】HCHO与O2在HAP表面催化氧化的历程示意图如图:(HAP仅为部分结构)
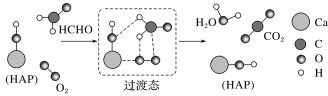
下列说法正确的是( )
A.HAP能提高HCHO的平衡转化率
B.HCHO在反应过程中有C-H键的断裂
C.产物CO2分子中的氧原子全部来自O2
D.该反应可表示为2HCHO+O2![]() CO2+2H2O
CO2+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】奥司他韦是一种高效、高选择性神经氨酸酶抑制剂,是目前治疗流感的最常用药物之一,是公认的抗禽流感、甲型H1N1等病毒最有效的药物之一。其合成路线如图所示:
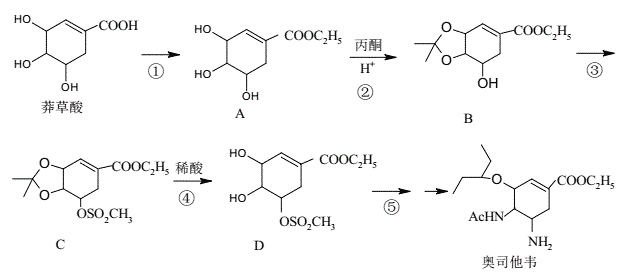
回答下列问题:
(1)莽草酸的含氧官能团名称有__;反应③的反应类型__。
(2)反应①的反应试剂和反应条件__。
(3)1molB最多可以消耗___molNaOH溶液。
(4)请写出反应②的化学方程式__。
(5)芳香化合物X是B的同分异构体,则符合官能团只含酚羟基的X有___种。
(6)设计由对甲基苯甲醛制备对醛基苯甲酸![]() 的合成路线__。
的合成路线__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com