
【题目】根据问题填空:
(1)钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢铁占世界钢铁年产量的四分之一. 
①钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的正极反应式为 .
②为了降低某水库的铁闸门被腐蚀的速率,可以采用如图甲所示的方案,其中焊接在铁闸门上的固体材料 R 可以采用 .
A.铜B.锡C.锌D.石墨
③如图乙方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的极上.
(2)根据反应 Fe+Fe2(SO4)3═3FeSO4设计的双液原电池如图丙所示.
①电极Ⅰ的材料为金属铁,则烧杯 A 中的电解质溶液为(填化学式)
②电极Ⅱ发生的电极反应式为 .
(3)某同学组装了如图丁所示的电化学装置.电极Ⅰ为 Al,其他电极均为 Cu. ①电极Ⅰ为极(填“正”“负”或“阴”“阳”),发生反应(填“氧化”或“还 原”),电极反应式为;电极Ⅲ为极(填“正”“负”或“阴”“阳”).
②盐桥中盛有含 KNO3 溶液的琼脂,盐桥中的 K+向极(填“Ⅰ”或“Ⅱ”)移动.
【答案】
(1)O2+4e﹣+2H2O=4OH﹣; C;负
(2)FeSO4; Fe3++e﹣=Fe2+
(3)负;氧化; Al﹣3e﹣=Al3+;阳; II
【解析】解:(1)①钢铁发生吸氧腐蚀时,铁作负极,发生失电子的氧化反应,即Fe=Fe2++2e﹣,碳作正极,正极上氧气得电子发生还原反应,电极反应式为:2H2O+O2+4e﹣=4OH﹣,所以答案是:2H2O+O2+4e﹣=4OH﹣;
②为了降低某水库的铁闸门被腐蚀的速率,可以让金属铁做原电池的正极,其中焊接在铁闸门上的固体材料R可以是比金属铁的活泼性强的金属,
所以答案是:C;
③电解池的阴极上的金属被保护,为降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的负极,
所以答案是:负;(2)①电解Ⅰ的材料为金属铁,则烧杯A中的电解质溶液为含有亚铁离子的可溶性的盐溶液,可以是硫酸亚铁,所以答案是:FeSO4;
②B烧杯是硫酸铁溶液,溶液中铁离子在电极Ⅱ上得电子,变成亚铁离子,所以Ⅱ发生的电极反应式为:Fe3++e﹣=Fe2+,所以答案是:Fe3++e﹣=Fe2+;(3)①电极Ⅰ为Al,其它均为Cu,Al易失电子作负极,所以Ⅰ是负极,负极上发生氧化反应,其电极反应为:Al﹣3e﹣=Al3+;I与IV相连,则Ⅳ是阴极,II为正极,Ⅲ是阳极;
所以答案是:负;氧化;Al﹣3e﹣=Al3+;阳;
②原电池中阳离子向正极移动,则盐桥中的K+向II极移动;
所以答案是:II.
【考点精析】通过灵活运用金属的电化学腐蚀与防护,掌握金属的保护:涂保护层;保持干燥;改变金属的内部结构,使其稳定;牺牲阳极的阴极保护法即用一种更为活泼的金属与要保护的金属构成原电池;外加电源法即可以解答此题.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】天然气可以制备大量的化工原料。请回答下列问题:
(1)由天然气制备合成气(CO和H2),进而可合成H2C2O4。
①欲加快H2C2O4溶液使5mL0.01mol/L酸性KMnO4溶液褪色,可采取的措施有__________、_______________(写两点)。
②下列可以证明H2C2O4是弱酸的是___________。
A.H2C2O4可以分解为CO、CO2和H2O
B.常温下,0.1mol/LNaHC2O4溶液中c(HC2O4-)+c(C2O42-)<0.lmol/L
C.0.1mol/LH2C2O4溶液25mL可以消耗0.1mol/LNaOH溶液50mL
D.常温下,0.05mol/L的H2C2O4溶液pH≈4
(2)已知:①CO(g)+H2(g)![]() C(s)+H2O(g) △H1=-130kJ/mol
C(s)+H2O(g) △H1=-130kJ/mol
②CH4(g)![]() C(s)+2H2(g) △H2=+76kJ/mol
C(s)+2H2(g) △H2=+76kJ/mol
③CO2(g)+H2(g)![]() CO(g)+H20(g) △H3=+41kJ/mol
CO(g)+H20(g) △H3=+41kJ/mol
则CH4(g)+CO2(g)![]() 2H2(g)+2CO(g) △H=________。
2H2(g)+2CO(g) △H=________。
(3)向2L容器中通入3molCO2、3molCH4,在不同温度下,以镍合金为催化剂,发生反应:CH4(g)+CO2(g)![]() 2H2(g)+2CO(g)。平衡体系中CH4和CO2的体积分数如下图。
2H2(g)+2CO(g)。平衡体系中CH4和CO2的体积分数如下图。

①高温下该反应能自发进行的原因是______________,930K时的平衡常数K=___________(保留两位小数)。
②请解释图中曲线随温度变化的原因______________。
③在700~1100K内,同温度下平衡转化率:CO2________CH4(填“大于”、“ 小于”或“等于”),结合(2)提供的反应分析,其原因可能是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某城市为了减少钢管因锈蚀造成的损失,拟用如图方法保护埋在酸性土壤中的钢管。下列有关说法正确的是( )

A. 在潮湿的酸性土壤中钢管主要发生化学腐蚀
B. 在潮湿的酸性土壤中金属棒M将电子通过导线流向钢管
C. 在潮湿的酸性土壤中H+向金属棒M 移动,抑制H+与铁的反应
D. 钢管与金属棒M也可用导线分别连接直流电源正、负极以使钢管表面的腐蚀电流接近于零
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z原子序数依次增大,其中W元素原子的最外层电子数是内层电子数的两倍。X与Z同主族,两原子的核外电子数之和为24。Y的原子半径是所有短周期主族元素中最大的。下列说法正确的是( )
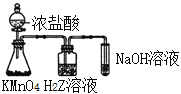
A. 简单离子半径:Z>Y>X
B. 如图所示实验可证明非金属性:Cl>Z
C. W、Y、Z的单质分别与X2反应时,X2用量不同产物均不同
D. Y分别与X、Z形成二元化合物中不可能存在共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列依据热化学方程式得出的结论正确的是( )
A.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=﹣57.3KJ/mol,则40gNaOH固体与稀盐酸完全反应,放出的热量即为57.3KJ
B.已知C(s)+O2(g)=CO2(g)△H1 C(s)+ ![]() (g)=CO(g)△H2 则△H1<△H2
(g)=CO(g)△H2 则△H1<△H2
C.已知H2(g)+Cl2(g)=2HCl,△H=﹣184.6KJ/mol,则反应物总能量小于生成物总能量
D.已知P(白磷,s)=P(红磷,s)△H<0,则白磷比红磷稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】地球的表面积为5.1亿平方公里,其中海洋的面积为3.67亿平方公里,占整个地球表面积的70.8 %。海洋是一个巨大的化学资源宝库,下面根据海水资源综合利用,请回答下列问题:
(1)淡化海水的方法有________________(写一种合理方法即可)。由海水提取的粗盐中含有Ca2+、Mg2+、SO42-等离子,为了除去这些离子,需要依次加入稍过量的NaOH、BaCl2、________(填化学式),之后________(填操作名称),再加入适量________(填试剂名称)。将所得溶液加热浓缩、冷却结晶,得到精盐。
(2)由无水MgCl2制取金属镁的常用工业方法是__________________。
(3)向苦卤中通入Cl2置换出Br2,再用空气吹出溴并用SO2吸收,转化为Br-,反复多次,以达到富集溴的目的。由海水提溴过程中的反应可得出Cl-、SO2、Br-还原性由强到弱的顺序是__________。
(4)工业上也可以用Na2CO3溶液吸收吹出的Br2,生成溴化钠和溴酸钠,同时放出CO2,写出反应的离子方程式____________。再H2SO4处理所得溶液重新得到Br2,其反应的离子方程式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是室温下,向100mL盐酸中逐渐加入NaOH溶液时,溶液的pH变化图象.根据图象所得结论正确的是( ) 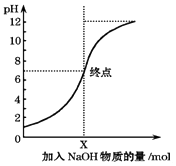
A.原来盐酸的物质的量浓度为0.1mol/L
B.NaOH溶液的浓度为0.1mol/L
C.pH=1和pH=7的点对应溶液中水的电离程度相同
D.X点NaOH溶液的体积为100mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧锰八面体纳米棒(OMS-2)是一种新型的环保催化剂。用软锰矿和黄铁矿(主要成分分别为MnO2、FeS2)合成OMS-2的工艺流程如下:
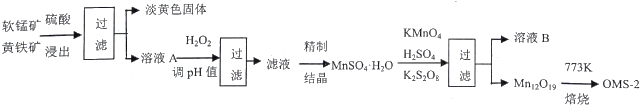
(1)FeS2中硫元素的化合价是_________。“调pH并过滤”主要除去______元素。
(2)Mn12O19中氧元素化合价均为-2价,锰元素的化合价有两种,则Mn (Ⅲ)、Mn (Ⅳ) 物质的量之比为_______________。生产过程中的原料KMnO4、K2S2O8、MnSO4·H2O按物质的量比1:1:5反应,产物中硫元素全部以SO42-的形式存在,该反应的离子方程式为__________________________。
(3)溶液B可进一步分离出两种主要化合物,一种可在该工艺中循环使用,化学式是____________;另一种为盐类,在农业生产中可用作___________________________。
(4)OMS-2是一种纳米级的分子筛。分别用OMS-2和MnOx对甲醛进行催化氧化,在相同时间内甲醛转化率和温度的关系如图:
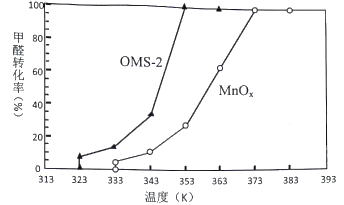
由图可知,OMS-2与MnOx相比,催化效率较高是____________________,原因是________________。
(5)甲醛(HCHO)在OMS-2催化氧化作用下生成CO2和H2O,现利用OMS-2对某密闭空间的甲醛进行催化氧化实验,实验开始时,该空间内甲醛含量为1.22mg/L,CO2含量为0.590mg/L,一段时间后测得CO2含量升高至1.25mg/L,该实验中甲醛的转化率为_______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com