
【题目】如图是室温下,向100mL盐酸中逐渐加入NaOH溶液时,溶液的pH变化图象.根据图象所得结论正确的是( ) 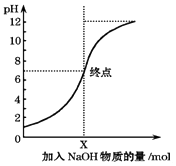
A.原来盐酸的物质的量浓度为0.1mol/L
B.NaOH溶液的浓度为0.1mol/L
C.pH=1和pH=7的点对应溶液中水的电离程度相同
D.X点NaOH溶液的体积为100mL
科目:高中化学 来源: 题型:
【题目】下列化学方程式不正确的是( )
A.CH3CO18OC2H5+H2O ![]() CH3COOH和C2H518OH
CH3COOH和C2H518OH
B.溴乙烷与氢氧化溶液共热:CH3CH2Br+NaOH ![]() CH3CH2OH+NaBr
CH3CH2OH+NaBr
C.蔗糖水解: ![]() +H2O
+H2O ![]()
![]()
D.苯酚钠中通入二氧化碳: ![]() +CO2+H2O→
+CO2+H2O→ ![]() +NaHCO3
+NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据问题填空:
(1)钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢铁占世界钢铁年产量的四分之一. 
①钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的正极反应式为 .
②为了降低某水库的铁闸门被腐蚀的速率,可以采用如图甲所示的方案,其中焊接在铁闸门上的固体材料 R 可以采用 .
A.铜B.锡C.锌D.石墨
③如图乙方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的极上.
(2)根据反应 Fe+Fe2(SO4)3═3FeSO4设计的双液原电池如图丙所示.
①电极Ⅰ的材料为金属铁,则烧杯 A 中的电解质溶液为(填化学式)
②电极Ⅱ发生的电极反应式为 .
(3)某同学组装了如图丁所示的电化学装置.电极Ⅰ为 Al,其他电极均为 Cu. ①电极Ⅰ为极(填“正”“负”或“阴”“阳”),发生反应(填“氧化”或“还 原”),电极反应式为;电极Ⅲ为极(填“正”“负”或“阴”“阳”).
②盐桥中盛有含 KNO3 溶液的琼脂,盐桥中的 K+向极(填“Ⅰ”或“Ⅱ”)移动.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2的绿色减排、捕捉、转化是人类可持续发展的重要战略之一。
(1)CO2来源之一是汽车尾气
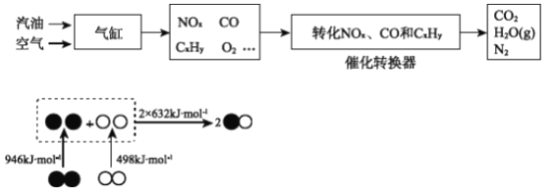

①根据上图,写出气缸内产生NO的热化学方程式________。
②写出转换器中在催化剂作用下NOx和CO反应的化学方程式________。
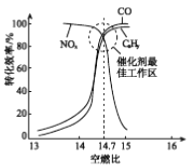
③在催化转换器中机动车尾气转化效率与空燃比(空气与燃油气的体积比)的关系如右图。若空燃比小于14.7,氧气不足,CxHy和CO不能被完全氧化,导致其转化效率降低;若空燃比大于14.7,则NOx的转化效率降低,原因是________。
(2)利用NaOH溶液可以“捕捉” CO2
已知:0.448L CO2(已折算标准状况)被NaOH溶液充分吸收,得到100mL含有Na2CO3和NaHCO3的吸收液。
①向吸收液中加入足量BaCl2溶液得到沉淀,经过滤、洗涤、干燥后,称重为1.97g,则吸收液中c(Na2CO3) = ________。(该条件下NaHCO3与BaCl2不反应)
②对该吸收液,下列判断正确的是________。
a . c (CO32- ) > c (HCO3- )
b. 2c (CO32- ) + c (HCO3- ) + c (OH- ) = c (H+ ) + c (Na+ )
c. c (H2CO3) + c (HCO3- ) + c (CO32- ) =0.2molL-1
(3)工业上可用CO2来制甲醇
①CO2 (g) + 3H2(g) ![]() CH3OH(g) + H2O(g) ΔH < 0
CH3OH(g) + H2O(g) ΔH < 0
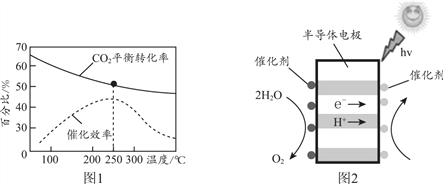
根据图1分析,实际工业生产中,反应温度选择250℃的理由________。
②利用光电催化原理,由CO2和H2O制备CH3OH的装置如图2。写出右侧的电极反应式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a.某有机物A化学式为CxHyOz,15 gA完全燃烧生成22 gCO2和9 gH2O。试确定:
(1)该有机物的最简式______________;
(2)若A的相对分子质量为60且和Na2CO3混合有气体放出,A和醇能发生酯化反应,则A的结构简式为 _______________ ;
(3)若A的相对分子质量为60且是易挥发有水果香味的液体,能发生水解反应,则其结构简式为______________;
(4)若A分子结构中含有6个碳原子,具有多元醇和醛的性质,则其结构简式为_______。
b.有机物A、B、C、D在一定条件下有如图所示的转化关系:

请回答下列有关问题:
(1)写出B的分子式:____________________。
(2)分别写出反应①的反应方程式______________和②的反应方程式________________________
(3)③的反应类型为___________________________。
(4)两分子D在浓硫酸存在的条件下加热可以发生自身的酯化反应生成E或F,且E的相对分子质量比F的小,则E和F的结构简式分别为___________________、_________________。
(5)下列关于有机物A的说法正确的有__________________(填序号)。
a.含有氢氧根离子,具有碱性
b.能发生加聚反应
c.能使溴水褪色
d.在一定条件下能与冰醋酸反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质所发生的化学反应中,由于反应物的用量不同而得到不同产物的是( )
①铁与稀硝酸②碳酸钠溶液与稀盐酸③铝和NaOH溶液④铁与氯气
A.①②B.①②③④C.①③D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用0.1032molL﹣1 HCl溶液滴定未知浓度的NaOH溶液,
(1)某同学按下列步骤进行实验:①取一锥形瓶,用待测NaOH溶液润洗两次; ②在锥形瓶中加入 25,.00 mL待测NaOH溶液;③加入几滴石蕊试剂做指示剂;④取一支酸式滴定管,洗涤干净; ⑤直接往酸式滴定管中注入标准酸溶液,进行滴定; ⑥两眼注视着滴定管内盐酸溶液液面下降,直至滴定终点.
其中所述操作有错误的序号为
(2)取用25.00 mL待测NaOH溶液应用以下(选填:“甲”、“乙”)装置,若取用NaOH溶液开始平视读数、结束时俯视读数,会导致所测氢氧化钠溶液浓度(填“偏大““偏小“或“不变“) ![]()
(3)若滴定开始前滴定管尖嘴中有一气泡,滴定结束后气泡消失, 则会导致所测氢氧化钠溶液浓度(填“偏大““偏小“或“不变“)
(4)若平行实验三次,记录的数据如下表
滴定次数 | 待测溶液的体积(/mL) | 标准HCl溶液的体积 | |
滴定前读数(/mL) | 滴定后读数(/mL) | ||
① | 25.00 | 1.02 | 21.04 |
② | 25.00 | 2.00 | 22.98 |
③ | 25.00 | 0.20 | 20.18 |
试计算待测NaOH溶液的物质的量浓度(列出计算过程).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com