
【题目】有X,Y,Z,W四种元素,它们的原子序数分别为6、10、11、17,下列判断错误的是( )
A.X,W能形成共价化合物
B.Z,W能形成离子化合物
C.Y分子中存在共价键
D.Y和Z不能形成化合物
科目:高中化学 来源: 题型:
【题目】工业纯碱中常含有NaCl、Na2SO4等杂质,可用如下图所示的装置测定工业纯碱中有效成分的含量。
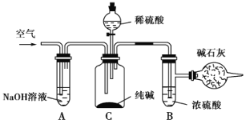
实验过程的主要步骤是:
①准确称取干燥试样x g(x>2),放入广口瓶C中。
②准确称量装有碱石灰的干燥管的质量为y g。
③从分液漏斗中缓缓注入稀硫酸,至不再产生气体为止。
④缓缓鼓入空气数分钟,然后将干燥管取下,准确称量其质量为W g。
根据以上实验,填写下列空格:
(1)装置A的作用是____________________________,如果不用装置A,会导致实验结果偏________(填“大”“小”或“不变”,下同)。
(2)装置B的作用是__________________,如果不用装置B,会导致实验结果偏________。
(3)通入空气的作用是____________________。如果不通入空气,会导致实验结果偏________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,X是主要物质,Y是少量杂质,Z是为除去杂质所要加入的试剂,其中所加试剂正确的组合是 ( )
A | B | C | D | |
X | FeCl2溶液 | FeCl3溶液 | Fe | Na2SO4溶液 |
Y | FeCl3 | CuCl2 | Al | Na2CO3 |
Z | Cu | Fe | NaOH溶液 | BaCl2溶液 |
A. A B. B C. C D. D
【答案】C
【解析】A.铜粉与氯化铁反应生成氯化亚铁和氯化铜,会引入新杂质,故A错误;B.二者均与Fe反应,不符合除杂的原则,不能除杂,故B错误;C.Al与NaOH溶液反应,而Fe不能,则加NaOH溶解后过滤可除杂,故C正确;D.二者均与BaCl2溶液反应,应加适量硫酸除杂,故D错误;故选C。
【题型】单选题
【结束】
19
【题目】某化学兴趣小组利用如图装置进行“铁与水反应”的实验,并检验产物的性质,请回答下列问题:
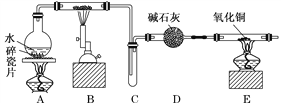
(1)A装置的作用是________________,B中反应的化学方程式为_____________。
(2)D的作用是____________________________________________________________。
(3)E中的现象是__________________________________________________________。
(4)A、B两个装置中应先点燃_______处的酒精灯,点燃E处酒精灯之前应进行的操作是_______________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组利用以下线路合成有机化合物F:
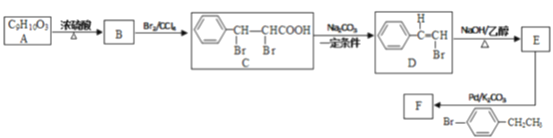
已知:R-C≡CH+R-Br![]() R-C≡C-R+HBr
R-C≡C-R+HBr
(1)B中官能团的名称是______,E的化学名称是_______;
(2)F的结构简式为____,由D生成E的反应类型是_______;
(3)试推断在核磁共振氢谱中A有多少组峰__;
A.8 组 B.9 组 C.7 组
(4)写出C与足量NaOH 溶液在加热条件下反应的化学方程式:____________;
(5)2 分子A在一定条件下反应生成一种含有3个六元环的化合物,该生成物的结构简式为_______ ;
(6) 同时满足下列条件的A 的同分异构体有___种( 不考虑立体异构)。
①属于芳香族化合物;
②能与碳酸氢钠溶液反应生成CO2;
③在一定条件下能发生催化氧化,且其产物能发生银镜反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.工业上生产水泥和玻璃都要用石灰石做原料
B.玻璃钢是一种合金材料
C.除去氨气中的水蒸气可用无水氯化钙可做干燥剂
D.溶于水可以导电的化合物一定是离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于恒容密闭容器中发生的可逆反应N2(g)+3H2(g)![]() 2NH3(g) ΔH<0,能说明反应达到化学平衡状态的为
2NH3(g) ΔH<0,能说明反应达到化学平衡状态的为
A. 断开一个N≡N键的同时有6个N—H键生成
B. 混合气体的密度不变
C. 混合气体的平均相对分子质量不变
D. N2、H2、NH3分子数比为1∶3∶2的状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锶(Sr)与镁是同主族元素.锶的单质及其化合物用途广泛,例如金属锶用于制造合金、光电管、照明灯,Sr(OH)2用于磨拉石的提纯,Sr(NO3)2用于烟火装置,SrCl2用于修补牙齿等。
(1)锶(Sr)位于周期表的第___周期___族,过氧化锶(SrO2)中锶元素的化合价为______。
(2)金属锶在常温下和水反应,有气体生成,写出该反应的化学方程式______。
(3)金属锶很活泼,在空气中易被氧化,可保存在______中(填序号)。
①水 ②酒精 ③煤油
(4)锶的性质与钙类似。已知:CaCl2 易溶于水,CaF2难溶于水,请写出硝酸锶和氟化钠反应的离子方程式______。
(5)隔绝空气高温焙烧SrSO4和C粉的混合物,若2molSrSO4完全反应,只有S被还原并转移16mol电子,同时只生成一种可燃性气体,该反应的化学方程式:______。
(6)在t℃时,某Sr(OH)2的稀溶液中c(H+)=10—amolL—1,c(OH—)=10—bmolL—1,已知a+b=12.向该溶液中逐滴加入 pH=X 的盐酸,测得混合溶液的部分pH如表所示。
Sr(OH)2溶液的体积/mL | 盐酸的体积/mL | 溶液的 pH | |
① | |||
② | 22.00 | 18.00 | 7 |
③ | 22.00 | 22.00 | 6 |
若忽略溶液混合前后的体积变化,则X为______(用数字填空)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知X、Y、Z、W为短周期主族元素,在周期表中的相对位置如下图所示,下列说法一定正确的是
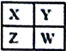
A. 若X元素在自然界中存在同素异形体,则W在同周期元素中,原子半径最小
B. 若HmXOn为强酸,则X 的氢化物溶于水一定显酸性(m、n均为正整数)
C. 若四种元素均为金属,则Z的最高价氧化物对应的水化物一定为强碱
D. 若四种元素均为非金属,则Y元素在化合物中不可能显示正化合价
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃下,现有0.1mol·L-1的H2SO4和0.1 mol·L-1一元弱酸HA两种溶液
(1)实验测得0.1 mol·L-1一元弱酸HA 的pH为4,则HA的电离平衡常数Ka= ;
(2)0.1mol·L-1的H2SO4中水电离出的C(H+)为 ;
(3)向0.1mol·L-1的硫酸中加入一定体积的pH=13的NaOH溶液,反应后溶液的pH为2,则所需NaOH溶液与硫酸的体积比为 ;
(4)向0.1 mol·L-1一元弱酸HA加入一定体积的水,在此过程中,下列数值变大的是 ;
①c(H+) ② 电离度(α) ③c(OH-) ④ Ka ⑤c(A-)/ c(HA) ⑥n(A-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com