
【题目】甲醇是未来重要的绿色能源之一。以CH4和H2O为原料,通过下列反应来制备甲醇。
Ⅰ、CH4(g)+H2O(g)═CO(g)+3H2(g) △H=+206.0KJ/mol
Ⅱ、CO(g)+2H2(g)═CH3OH(g) △H=﹣129.0KJ/mol
(1)CH4(g)与H2O(g)反应生成CH3OH(g)和H2(g)的热化学方程式为___。
(2)将1.0molCH4和2.0mol H2O(g)通入容积为2L的密闭容器中,在一定条件下发生反应I,测得在一定压强下平衡时CH4的转化率与温度的关系如图1。

①假设100℃时反应I达到平衡所需的时间为5min,则用H2表示这段时间该反应的平均反应速率为___。
②100℃时反应I的平衡常数为___。若保持温度和容器的容积不变,5min时再向容器中充入H2O(g)和CO各0.2mol,平衡将___移动(填“正向”、“逆向”或“不”)。
(3)如图2,P是可自由平行滑动的活塞,关闭K2,在相同温度下,通过K1、K3分别向A、B中各充入2mol CO和3molH2,在一定条件下发生反应Ⅱ,关闭K1、K3,反应起始时A、B的体积相同,均为aL。
①反应达到平衡后,A内压强为起始压强的![]() ,则平衡时A容器中H2的体积分数为__。
,则平衡时A容器中H2的体积分数为__。
②若在平衡后打开K2,再次达到平衡后B容器的体积缩至0.6aL,则打开K2之前,B容器的体积为___L。
【答案】CH4(g)+H2O(g)=CH3OH(g)+H2(g) △H=+77.0kJ·mol﹣1 0.12mol·L﹣1·min﹣1 0.18mol2·L﹣2 逆向 ![]() 0.8aL
0.8aL
【解析】
(1)Ⅰ、CH4(g)+H2O(g)═CO(g)+3H2(g) △H=+206.0KJ/mol
Ⅱ、CO(g)+2H2(g)═CH3OH(g) △H=﹣129.0KJ/mol
将Ⅰ+Ⅱ得:CH4(g)+H2O(g)== CH3OH(g)+ H2(g) △H=+77.0kJ·mol﹣1
(2) 利用三段式我们可以进行以下
CH4(g)+H2O(g)═CO(g)+3H2(g)
起始量 1.0mol 2.0mol 0 0
变化量 0.4mol 0.4mol 0.4mol 1.2mol
平衡量0.6mol 1.6mol 0.4mol 1.2mol
① 答案为:0.12mol·L﹣1·min﹣1
答案为:0.12mol·L﹣1·min﹣1
②![]() 答案为0.18mol2·L﹣2
答案为0.18mol2·L﹣2
若保持温度和容器的容积不变,5min时再向容器中充入H2O(g)和CO各0.2mol,则此时各物质的浓度为 c(CH4)=0.3mol/L,c(H2O)=0.9mol/L,c(CO)=0.3mol/L,c(H2)=0.6mol/L
![]() mol2·L﹣2>0.18mol2·L﹣2
mol2·L﹣2>0.18mol2·L﹣2
所以平衡应逆向移动。答案为逆向
(3)①设参加反应的CO物质的量为x
CO(g)+2H2(g)═CH3OH(g)
起始量 2mol 3mol 0
变化量 x 2x x
平衡量 2-x 3-2x x
![]() x=1mol
x=1mol
则平衡时A容器中H2的体积分数为![]() 答案为
答案为![]()
②若在平衡后打开K2,再次达到平衡后B容器的体积缩至0.6aL,则A、B 两容器内气体的总体积为1.6aL,相当于每个容器内的气体各为0.8aL。
故若打开K2之前,B容器的体积为0.8aL。
答案为0.8aL


科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数的数值,下列说法中正确的是( )
A.常温常压下,32 g氧气所含的原子数为NA
B.标准状况下,22.4 L 四氯化碳的分子数为NA
C.0℃,101 kPa下,44.8 L氮气所含有的分子数为2NA
D.常温常压下,1 mol氦气含有的分子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列示意图中,白球代表氢原子,黑球代表氦原子,方框代表容器,容器中间有一个可以左右自由滑动的隔板(其质量忽略不计).其中能表示相同温度时,等质量的氢气与氦气的是( )
A. B.
B.
C. D.
D.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:xA(g)+B(g)![]() 2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别用下表和如图表示:下列说法正确的是( )
2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别用下表和如图表示:下列说法正确的是( )
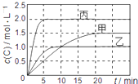
容器 | 甲 | 乙 | 丙 |
容积 | 0.5L | 0.5L | 1.0L |
温度 | T1 | T2 | T2 |
反应物起始量 | 0.5molA 1.5molB | 0.5molA 1.5molB | 2.0molA 6.0molB |
A.由图可知:T1<T2,且该反应为吸热反应
B.T2时该反应的平衡常数K=0.8
C.物质A的化学计量数x=2
D.保持甲容器体积不变,向其中通入He气体,达到新平衡后,C的百分含量减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】探究浓度对化学平衡的影响,实验如下:
I.向5mL 0.05mol/L FeCl3溶液中加入5mL 0.05mol/L KI溶液(反应a),平衡后分为两等份
Ⅱ.向一份加入饱和KSCN溶液,变红(反应b);加入CCl4,振荡、静置,下层显极浅的紫色
Ⅲ.向另一份加入CCl4,振荡、静置,下层显紫红色
结合实验,下列说法不正确的是
A. 反应a为:2Fe3++ 2I-![]() 2Fe2++I2
2Fe2++I2
B. Ⅱ中,反应a进行的程度大于反应b
C. 比较氧化性:Ⅱ中,I2>Fe3+
D. 比较水溶液中c(Fe2+):Ⅱ<Ⅲ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对CO2及氮氧化物的研究有更大意义:
(1)CO2与H2可用来合成可再生能源甲醇,已知CH3OH(l)标准燃烧热△H=-726.5kJ/mol、H2的燃烧热数值为285.8kJ/mol,则CO2(g)+3H2(g)![]() CH3OH(l)+H2O(l) △H=___。
CH3OH(l)+H2O(l) △H=___。
(2)用NH3催化还原NOx时包含以下反应。
反应I:4NH3(g)+6NO(g)![]() 5N2(g)+6H2O(l) △H1<0
5N2(g)+6H2O(l) △H1<0
反应Ⅱ:4NH3(g)+6NO2(g)![]() 5N2(g)+3O2(g) + 6H2O(l) △H2>0
5N2(g)+3O2(g) + 6H2O(l) △H2>0
反应Ⅲ:2NO(g) +O2(g)![]() 2NO2(g) △H3<0
2NO2(g) △H3<0
① 反应I在容积固定密闭容器内进行,选用不同的催化剂,反应产生N2的量随时间变化如图所示。下列说法正确的是___。
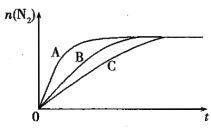
A.该反应的活化能大小顺序是:Ea(A)>Ea(B)>Ea(C)
B.增大压强能使反应速率加快,是因为增加了活化分子百分数
C.单位时间内H-O键与N-H键断裂的数目相等时,说明反应已经达到平衡
D.若在恒容绝热的密闭容器中发生反应,当K值不变时,说明反应已经达到平衡
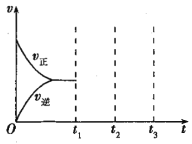
②将物质的量之比为2:1的NO、O2混合气体置于恒温密闭容器中发生反应Ⅲ,正、逆反应速率随时间变化曲线如图所示。在t1时,保持容器压强不变,充入一定量的NO2,t2时建立新的平衡,请在答题纸中画出t1~t3正、逆反应速率随时间变化曲线。___
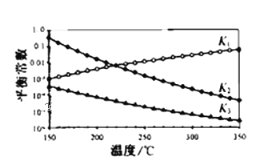
(3)一定条件下,由CO2和H2制备甲醇的过程中含有下列反应:
反应1:CO2(g)+H2(g)CO(g)+H2O(g) △H1
反应2:CO(g)+2H2(g)CH3OH(g) △H2
反应3:CO2(g)+3H2(g)CH3OH(g)+H2O(g) △H3
其对应的平衡常数分别为K1、K2、K3,它们随温度变化的曲线如图所示。则△H2__△H3(填“大于”、“小于”、“等于”),理由是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为一个五圆环,每个环中的物质依次为FeCl3、NaCl、Na2O2、CO2、I2,图中相连的两种物质可归属为同一类,用①、②、③、④表示相交部分,请回答下列问题:

(1)关于上述相交部分的说法不正确的是_____________(填序号)。
A ①表示盐类 B ②表示钠的化合物
C ③表示氧化物 D ④表示非电解质
(2)关于上述相交部分的说法正确的是_____________(填序号)。
A 海水晒盐属于物理变化 B Na2O2属于碱性氧化物
C I2易溶于CCl4 D 钠着火可用CO2灭火
(3)若NaCl固体中含有少量I2杂质,可采用的除杂方法是_____________(填序号)
A 过滤 B 升华 C 渗析
(4)上述五种物质中,有两种物质可以发生氧化还原反应,其化学方程式为___________;
(5)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入1 mol·L-1上图中某物质M的溶液,继续煮沸得到红褐色透明液体。
①物质M的化学式为__________。
②检验该红褐色透明液体是胶体的方法为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定量的Cu、Fe2O3的混合物中加入400 mL 1 mol·L-1的盐酸,恰好使混合物完全溶解,所得溶液中不含Fe3+。若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为
A. 2.4 g B. 3.2 g C. 4.8 g D. 6.4 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以NaClO为有效成分的“84”消毒液在抗击新冠疫情的消杀工作中起到了重要作用。某研究小组设计下列实验探究NaClO的性质。
(已知:电离常数:![]() :
:![]() ,
,![]() ;
;![]() )
)
实验 | 装置 | 试剂(少量) | 预测可能的现象 |
① |
| 酚酞 | 无色溶液最终呈红色 |
② |
| 无明显现象 | |
③ | 淀粉 | 无色溶液立即变蓝 | |
④ |
| 溶液略呈浅绿色 |
结合上述实验探究,预测的现象以及解释均正确的是( )
A.实验①:NaClO溶液呈碱性:![]()
B.实验②:NaClO可用于制得![]()
C.实验③:NaClO具有氧化性:![]()
D.实验④:NaClO具有还原性:![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com