
【题目】某化学兴趣小组的同学利用酸碱滴定法测定某变质烧碱样品(含Na2CO3杂质)中 NaOH 的质量分数。实验步骤如下:
(I)迅速地称取烧碱样品0.50 g,溶解后配制成100 mL溶液,备用。
(II)将0.1000 mol·L1HCl标准溶液装入酸式滴定管,调零,记录起始读数V0;用碱式滴定管取 20.00mL 样品溶液于锥形瓶中,滴加 2 滴酚酞;以HCl 标准溶液滴定至第一终点,记录酸式滴定管的读数V1;然后再向锥形瓶内滴加2滴甲基橙,继续用 HCl 标准溶液滴定至第二终点,记录酸式滴定管的读数V2。重复上述操作两次,记录数据如下:
实验序号 | 1 | 2 | 3 |
V0/ mL | 0.00 | 0.00 | 0.00 |
V1/ mL | 22.22 | 22.18 | 22.20 |
V2/ mL | 23.72 | 23.68 | 23.70 |
(1)步骤I中所需的玻璃仪器有烧杯、玻璃棒、胶头滴管和__。酸式滴定管用蒸馏水洗净后、装入标准溶液并调零之前,应进行的操作是__。
(2)溶液中的H2CO3、![]() 、
、![]() 的物质的量分数随 pH 的变化如图所示:
的物质的量分数随 pH 的变化如图所示:
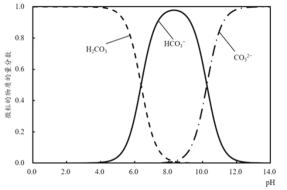
酚酞和甲基橙指示剂的变色pH范围及对应颜色见表。
酚酞 | 无色 pH < 8.0 | 粉红 pH 8.0~9.8 | 红 pH > 9.8 |
甲基橙 | 红 pH < 3.1 | 橙 pH 3.1~4.4 | 黄 pH > 4.4 |
①滴定至第一终点时,溶液中含碳微粒的主要存在形式为__。
②滴定至第一终点的过程中,发生反应的离子方程式为__。
③已知:pKa1= lgKa1,结合图像可知,H2CO3的pKa1约为__。
a.5.0 b.6.4 c.8.0 d.10.3
(3)下列有关滴定的说法正确的是__。
a.滴定至第一终点时,溶液中 c(H+)+c(Na+) = 2c(![]() ) + c(
) + c(![]() ) + c(OH)
) + c(OH)
b.滴定至第一终点时,溶液中 n(Cl) +n(![]() ) + n(
) + n(![]() ) + n(H2CO3) =n(Na+)
) + n(H2CO3) =n(Na+)
c.判断滴定至第二终点的现象是溶液由黄色变为橙色
d.记录酸式滴定管读数V1时,俯视标准液液面,会导致测得的NaOH质量分数偏低
(4)样品中NaOH的质量分数![]() (NaOH) =__%(计算结果保留小数点后 1 位)
(NaOH) =__%(计算结果保留小数点后 1 位)
【答案】100mL容量瓶(量筒) 用标准盐酸溶液润洗酸式滴定管 ![]() H++OH-═H2O H+ +
H++OH-═H2O H+ +![]() =
=![]() b bcd 84.1
b bcd 84.1
【解析】
(1)配制一定物质的量浓度溶液的步骤选择需要的仪器,用到的仪器:托盘天平、药匙、烧杯、玻璃棒、量筒、胶头滴管和容量瓶(一定要注明规格),酸式滴定管用蒸馏水洗净后,还应该进行的操作是需要用待装标准液润洗减少误差;
(2)①从图中可以看出当酚酞试液变色时,pH大致为8,此时溶液中含碳微粒主要时碳酸氢根离子;②滴定至第一终点的过程中,发生的反应是氢氧化钠和盐酸反应生成氯化钠溶液,碳酸钠和盐酸反应生成碳酸氢钠;③根据电离平衡常数表达式可知H2CO3的Ka1=![]() 结合图像便可计算;
结合图像便可计算;
(3) a.根据溶液中的电荷守恒式判断;b.根据物料守恒式可判断;c.第二反应终点是继续滴入盐酸和碳酸氢钠反应生成氯化钠溶液,甲基橙溶液由黄色变为橙色; d.记录酸式滴定管读数V1时,俯视标准液液面,记录盐酸溶液体积减小;
(4)将0.1000mol/L HCl标准溶液装入酸式滴定管,调零,记录起始读数V0;用碱式滴定管取20.00 mL样品溶液于锥形瓶中,滴加2滴酚酞;以HCl标准溶液滴定至第一终点(此时溶质为NaCl和NaHCO3),记录酸式滴定管的读数V1,发生的反应为NaOH+HCl=NaCl+H2O,Na2CO3+HCl=NaHCO3+NaCl,然后再向锥形瓶内滴加2滴甲基橙,继续用HCl标准溶液滴定至第二终点,发生的反应为:NaHCO3+HCl=NaCl+H2O+CO2↑,记录酸式滴定管的读数V2,重复上述操作两次,记录数据计算出平均值V1和V2,(V2-V1)即为碳酸氢钠消耗的盐酸,结合反应过程计算样品中碳酸钠的质量,得到样品中氢氧化钠的质量分数;
(1)配制一定物质的量浓度溶液的一般步骤为:计算、称量、溶解、移液、洗涤、定容、摇匀,用到的仪器:托盘天平、药匙、烧杯、玻璃棒、胶头滴管;还缺少的玻璃仪器:100mL容量瓶(量筒),酸式滴定管用蒸馏水洗净后、装入标准溶液前,应进行的操作是:用HCl标准溶液润洗酸式滴定管,故答案为:100 mL容量瓶;用HCl标准溶液润洗酸式滴定管;
(2) ①第一阶段滴定使用了酚酞做指示剂,故滴定到pH为8时,即为滴定终点,对照微粒分布图中可知,此时,溶液中含碳微粒的主要存在形式为![]() ,故答案为:
,故答案为:![]() ;
;
②滴定至第一终点的过程中OH-和![]() 与盐酸反应分别生成水和
与盐酸反应分别生成水和![]() ,故该过程中发生反应的离子方程式为H++OH-═H2O,H+ +
,故该过程中发生反应的离子方程式为H++OH-═H2O,H+ +![]() =
=![]() ,故答案为:H++OH-═H2O,H+ +
,故答案为:H++OH-═H2O,H+ +![]() =
=![]() ;
;
③根据电离平衡常数表达式可知H2CO3的Ka1=![]() 结合图像可知,当pH=6.4左右时,c(
结合图像可知,当pH=6.4左右时,c(![]() ) = c(
) = c(![]() ),故H2CO3的pKa1约为6.4,故答案为:b;
),故H2CO3的pKa1约为6.4,故答案为:b;
(3) a.滴定至第一终点时,溶液中电荷守恒式为c(H+)+c(Na+) = 2c(![]() ) + c(
) + c(![]() ) +c(OH)+c(Cl),故a错误;
) +c(OH)+c(Cl),故a错误;
b.滴定至第一终点时,溶液中是氯化钠和碳酸氢钠的混合溶液,故由物料守恒式:n(Cl) +n(![]() ) + n(
) + n(![]() ) +n(H2CO3) =n(Na+),故b正确;
) +n(H2CO3) =n(Na+),故b正确;
c.根据图中可知,碳酸氢根基本完全转化为碳酸时,pH大致为4,故滴定至第二终点的现象是溶液由黄色变为橙色,故c正确;
d.记录酸式滴定管读数V1时,俯视标准液液面,记录盐酸溶液体积V1减小,计算得到碳酸钠质量增大,氢氧化钠质量减小,质量分数减小,故d正确;
故答案为:bcd;
(4)将0.1000mol/L HCl标准溶液装入酸式滴定管,调零,记录起始读数V0;用碱式滴定管取20.00 mL样品溶液于锥形瓶中,滴加2滴酚酞;以HCl标准溶液滴定至第一终点(此时溶质为NaCl和NaHCO3),记录酸式滴定管的读数V1,发生的反应为NaOH+HCl=NaCl+H2O,Na2CO3+HCl=NaHCO3+NaCl,然后再向锥形瓶内滴加2滴甲基橙,继续用HCl标准溶液滴定至第二终点,发生的反应为:NaHCO3+HCl=NaCl+H2O+CO2↑,记录酸式滴定管的读数V2。重复上述操作两次,记录数据如表,
平均V1=![]() ,平均V2=
,平均V2=![]() ,发生反应NaHCO3+HCl=NaCl+H2O+CO2↑,消耗的盐酸溶液体积=23.70mL-22.20mL=1.50mL,结合反应过程计算样品中碳酸钠的质量=0.0015L×0.1mol/L×
,发生反应NaHCO3+HCl=NaCl+H2O+CO2↑,消耗的盐酸溶液体积=23.70mL-22.20mL=1.50mL,结合反应过程计算样品中碳酸钠的质量=0.0015L×0.1mol/L×![]() =0.00075mol,得到样品中氢氧化钠的质量分数=
=0.00075mol,得到样品中氢氧化钠的质量分数=
![]() ,故答案为:84.1。
,故答案为:84.1。


科目:高中化学 来源: 题型:
【题目】在一定条件下,N2O分解的部分实验数据如下( )
反应时间/min | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
c(N2O)/molL-1 | 0.100 | 0.090 | 0.080 | 0.070 | 0.060 | 0.050 | 0.040 | 0.030 | 0.020 | 0.010 | 0.000 |
下图能正确表示该反应有关物理量变化规律的是( )
(注:图中半衰期指任一浓度N2O消耗一半时所需的相应时间,c1、c2均表示N2O初始浓度且c1<c2)
A. B.
B. C.
C. D.
D.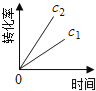
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年2月16日李克强总理到东北调研经济情况,重点走访了钢铁厂,鼓励钢铁厂提高钢铁质量和产量,铁及其化合物在日常生活中应用广泛。
(1)利用Fe2+、Fe3+的催化作用,常温下可将SO2转化为SO42-,从而实现对SO2的治理。已知含SO2的废气通入含Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2++O2+4 H+=4Fe3++2H2O,则另一反应的离子方程式为__________;
(2)氧化铁是重要工业颜料,下面是制备氧化铁的一种方法,其流程如下:

①操作Ⅰ的名称是__________;操作Ⅱ为洗涤,洗涤操作的具体方法为__________;
②滤液A中加入稍过量的NH4HCO3溶液生成沉淀同时有一种气体产生,写出其化学方程式: __________;
(3)如果煅烧不充分,产品中将有FeO存在,称取3.0 g氧化铁产品,溶解,在250 mL容量瓶中定容;量取25.00 mL待测溶液于锥形瓶中,用酸化的0.01000 mol/L KMnO4溶液滴定至终点,重复滴定2-3次,消耗KMnO4溶液体积的平均值为20.00 mL,
①该实验中的KMnO4溶液需要酸化,用于酸化的酸是__________(填字母序号)。
a.稀硝酸 b.稀盐酸 c.稀硫酸 d.浓硝酸
②计算上述产品中Fe2O3的质量分数为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学实验事实及其解释都正确的是( )
A. 过量的铜屑与稀硝酸作用,反应停止后,再加入1 mol/L稀硫酸,铜屑又逐渐溶解是因为铜 可直接与1 mol/L稀硫酸反应
B. 粗锌与稀硫酸反应制氢气比纯锌快,是因为粗锌比纯锌还原性强
C. 铁钉放在浓硝酸中浸泡后,再用蒸馏水冲洗,然后放入CuSO4溶液中不反应,说明铁钉表面 形成了一层致密稳定的氧化膜
D. 工业制玻璃的主要反应之一:Na2CO3+SiO2高温Na2SiO3+CO2↑,该反应原理可用“强酸H2CO3制弱酸H2SiO3”来解释
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于密闭容器中的反应:2SO2(g)+O2(g)![]() 2SO3(g) △H<0,450℃时,n(SO3)和n(O2)随时间的变化关系如图所示,下列说法正确的是
2SO3(g) △H<0,450℃时,n(SO3)和n(O2)随时间的变化关系如图所示,下列说法正确的是

A.点c处反应达到平衡
B.点a的正反应速率比点b的大
C.点d (t1时刻)和点e (t2时刻)处n(SO2)不一样
D.其他条件不变,600℃时反应至t1时刻,n(SO 3)比上图中的e点值要大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随Cr含量的变化三种稀酸对Fe﹣Cr合金腐蚀速率的曲线如图所示,下列有关说法正确的是( )
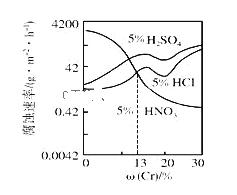
A.稀硝酸对Fe﹣Cr合金的腐蚀性比稀硫酸和稀盐酸的弱
B.随着Cr含量增加,稀硝酸对Fe﹣Cr合金的腐蚀性减弱
C.Cr含量大于13%时,因为三种酸中硫酸的氢离子浓度最大,所以对Fe﹣Cr合金的腐蚀性最强
D.酸对Fe﹣Cr合金的腐蚀与阴离子浓度无关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将2 mol SO2和2 mol SO3气体混合于某固定体积的密闭容器中,在一定条件下反应:2SO2(g)+O2(g)![]() 2SO3(g),平衡时SO3为W mol。相同温度下,分别按下列配比在相同体积的容器中反应,反应达到平衡时,SO3的物质的量大于W mol的是( )
2SO3(g),平衡时SO3为W mol。相同温度下,分别按下列配比在相同体积的容器中反应,反应达到平衡时,SO3的物质的量大于W mol的是( )
A.2 mol SO2+1 mol O2B.4 mol SO2+1 mol O2
C.2 mol SO2+1 mol O2+2 mol SO3D.3 mol SO2+1 mol SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:![]() 时
时
化学式 |
|
|
|
电离平衡常数 |
|
|
|
下列说法正确的是 ( )
A. 醋酸稀释过程中,![]() 逐渐减小
逐渐减小
B. ![]() 溶液中:
溶液中:![]()
C. 向醋酸或HCN溶液中加入![]() ,均产生
,均产生![]()
D. 物质的量浓度相同时![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】双氧水(过氧化氢的水溶液)在工业生产和日常生活中应用广泛。
(1)双氧水常用于伤口消毒,这一过程利用了过氧化氢的_________(填过氧化氢的化学性质)。
(2)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态过氧化氢。已知0.4 mol液态肼与足量的液态过氧化氢反应,生成氮气和水蒸气,并放出256.652kJ的热量。该反应的热化学方程式为__________。
(3)双氧水能将碱性废水中的CN-转化成碳酸盐和一种对环境无污染的气体,CN-的电子式为________,写出该反应的离子方程式________。
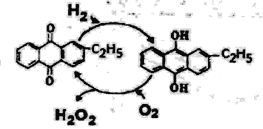
(4)下图是工业上制备过氧化氢最常见的方法,写出实际发生反应的总方程式_______。
(5)下图是一种用电解原理来制备H2O2,并用产生的H2O2处理废氨水的装置。
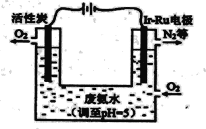
①Ir-Ru惰性电极吸附O2生成H2O2,其电极反应式是_______。
②处理废氨水中溶质(以NH3计)的质量是34g,理论上电路中转移电子数为__________mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com