
����Ŀ������ͼ�й�����ת����ϵ�У������ʾ��dz��л�ѧ���������ʣ�����AΪ��ɫ�������ʣ�B�ܲ���ֲ��Ĺ�����á�C��DΪ��ɫ��ĩ��FΪ�����ڸ������������ļGΪ���������ʣ�HΪ��������ɫ���ʣ�ͼ�в�����������ʡ�ԣ���

��1���û�ѧʽ��ʾ�� D________��G___________��
��2��д��E��F��Ӧ�Ļ�ѧ����ʽ________________________��
��3������������ɵĵ����������ڱ�������ǣ�C6H12O6������������ø�Ĵ������·�������������ͬʱ�ų�������д�������Ƿ�������������Ӧ�Ļ�ѧ����ʽ______________��
���𰸡�CBaSO4CuSO4+Ca(OH)2��Cu(OH)2��+CaSO4C6H12O6+6O2![]() 6CO2+6H2O
6CO2+6H2O
��������
���ݸ����ʾ��dz��л�ѧ���������ʣ�AΪ��ɫ�������ʣ�����A��ͭ��B�ܲ���ֲ��Ĺ�����ã�C��DΪ��ɫ��ĩ��C��D���»�����ͭ��B������B�Ƕ�����̼��C��D������ͭ��̼��C��X���ɵ�E�����Ȼ�����Ӧ������C������ͭ��D��̼��FΪ�����ڸ������������ļ����F���������ƣ�GΪ���������ʣ�HΪ��������ɫ���ʣ�����E������ͭ������ͭ���Ȼ�����Ӧ�������ᱵ�������Ȼ�ͭ������G�����ᱵ��X�����ᣬ����ͭ���������Ʒ�Ӧ��������ƺ�������ͭ����������H��������ͭ��I������ƣ�Ȼ���Ƴ������ʽ�����֤���ɡ�
�������Ϸ�����֪A��ͭ��B�Ƕ�����̼��C������ͭ��D��̼��E������ͭ��F���������ƣ�G�����ᱵ��X�����ᣬH��������ͭ��I������ƣ���
��1���������Ϸ�����֪D��G�Ļ�ѧʽ�ֱ���C��BaSO4��
��2��E��F�ķ�Ӧ���������ƺ�����ͭ��Ӧ��������ƺ�������ͭ��������ѧ����ʽΪCuSO4+Ca(OH)2��Cu(OH)2��+CaSO4��
��3����Ϊ�����Ƿ�������������Ӧ���ɶ�����̼��ˮ���ʻ�ѧ����ʽΪC6H12O6+6O2![]() 6CO2+6H2O��
6CO2+6H2O��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������������ȷ����
A. ���³�ѹ�£�20g���������е�ԭ����ĿΪ0.5NA
B. 2.8������50mL4 mol��L-1������ȫ��Ӧת�Ƶ��ӵ���ĿΪ0.1NA
C. ��״���£�22.4 LSO2��SO3������к��е���ԭ����ĿΪ0.1NA
D. 28g��C2H4��N2��������к��е�ԭ����Ϊ2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�ش��������⣺
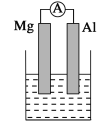
(1)���ձ�����ҺΪ����������Һ����Ϊ________(��Mg��Al)���ܷ�Ӧ����ʽΪ______��
(2)��������������ɴ���ʹ����һ������װ�ã��乹������ͼ��ʾ��A��B�����缫���ɶ��̼����ɡ��õ�ص�������ӦʽΪ��___________________________��
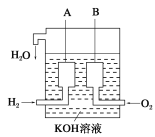
(3)���������װ����ͨ���H2�ij�CH4���壬Ҳ�������һ��ԭ���װ�ã���ص��ܷ�Ӧ����ʽΪ��CH4+2O2+2KOH=K2CO3+3H2O����õ�صĸ�����ӦʽΪ��____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йؽ����Ĺ�ҵ�Ʒ��У���ȷ����
A. �Ժ�ˮΪԭ���Ƶþ��Σ��ٵ�⾫�ε�ˮ��Һ��ȡ��
B. �ú�ˮ��ʯ�����Ϊԭ�ϣ���һϵ�й����Ƶ�����þ����H2��ԭ����þ�Ƶ�þ
C. ������ʯ����̿��������ʯ��ʯ��Ϊԭ�ϣ�ͨ����Ӧ������CO�ڸ����»�ԭ����ʯ�Ƶ���
D. ���������л�����������Ƶ��Ȼ������壬������ڵ��Ȼ����õ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʵ�����ø��������ȡ�����Ĺ����У�����ͼ������ȷ��ʾ��Ӧ�仯��ϵ����
A.  B.
B. 
C.  D.
D. 
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʽ�о���ѧϰ������ѧ������˼ά�����÷�����֣��һ��ѧϰС�齫����װ����ͼ���ӣ�D��F��X��Y ���Dz��缫��C��E �����缫������Դ��ͨ�������е����̪��Һ����F�������Ժ�ɫ���Իش�����������
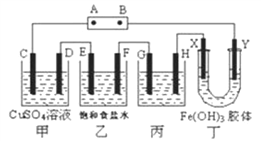
��1����ԴB ����������_______________��
��2����װ���е�ⷴӦ���ܻ�ѧ����ʽ����______________________��
��3����������Һ��������ͬһʱ��C��D �缫�ϲμӷ�Ӧ�ĵ��ʻ����ɵĵ��ʵ����ʵ���֮����________________��
��4�����ñ�װ�ý���ͭ(����������п������) ������G ������Ӧ����___________(������ͭ��������ͭ��)�����Һ��ԭ����ʵ����ʵ���Ũ�Ƚ�________(�������������С������������)��
��5��װ�ö��е�������__________________________��
��6����׳�����Һ������ڵ��ǰ����500ml�����ҳ���������������Ϊ4.48L (��״��) ʱ���׳������������ʵ����ʵ���Ũ��Ϊ__________mol��L-1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���¶�ΪT1��T1=25������T2ʱ��ˮ��Һ��ˮ�����ӻ�������ͼ��ʾ�������жϴ�����ǣ�������

A. T2��25�� B. x=1.0��10��7
C. KW��a��=KW��d�� D. b����Һ�ʼ��ԣ�c����Һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ��������������ˮ��Һ�еĵ�����ƽ�ⳣ�����������ѡ����ȷ���ǣ�������
�����ᣨHCN�� | ̼�ᣨH2C03�� | ����ᣨHF�� |
K=4.9��10��10 | K1=4.4��10��7 K2=4.7��10��11 | K=6.61��10��4 |
A. �軯����Һ��ͨ������CO2��2CN��+H2O+CO2�T2HCN+CO32��
B. NaCN��HCN�Ļ����Һ��һ���У�c��Na+����c��CN������c��HCN����c��H+����c��OH-��
C. 25��ʱCN-��ˮ��ƽ�ⳣ��ԼΪ1.6��10-5
D. NaCN��HCN�Ļ����Һ�У�2c(Na+)=c(CN����+c(HCN)
���𰸡�C
��������A�����ݵ���ƽ�ⳣ��֪������H2CO3��HCN��HCO3-�����ǿ����ȡ����֪���軯����Һ��ͨ������CO2ֻ�ܷ������·�ӦCN��+H2O+CO2=HCN+ HCO3-����A����B��NaCN��Һ�Լ��ԣ�HCN��Һ�����ԣ�ѡ����û����֪���ʱNaCN��HCN������Դ�С�����ж���Һ������ԣ�Ҳ���ж�����Ũ�ȴ�С����B����C��HCN�ĵ��볣��K��CN��ˮ�ⳣ��Kh�ij˻�����Kw������Kh=![]() ��1.6��10-5����C��ȷ��D���������Ũ�ȵ�NaCN��Һ��HCN��Һ���������Һ�������غ�Ϊ��2c(Na+)=c(CN)+c(HCN)����ѡ����û����֪NaCN��HCN������Դ�С�����жϣ���D����ѡC��
��1.6��10-5����C��ȷ��D���������Ũ�ȵ�NaCN��Һ��HCN��Һ���������Һ�������غ�Ϊ��2c(Na+)=c(CN)+c(HCN)����ѡ����û����֪NaCN��HCN������Դ�С�����жϣ���D����ѡC��
�����͡���ѡ��
��������
19
����Ŀ�������£���20.00 mL 0.8molL��1һԪ��HA��Һ�е���0.8 molL��1��NaOH��Һ����Һ��pH���¶������NaOH��Һ����ı仯������ͼ��ʾ�������й�˵����ȷ���ǣ�������
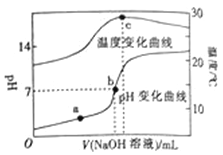
A. �����£�1.0 molL��1HA����Һ��pH=0
B. a��b��c���㣬a������Һ��c��Na+�����
C. a��b�������Һ��ˮ�����ӻ�Kw��a��=Kw��b��
D. c��ʱ����NaOH��Һ�����Ϊ20.00mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪![]() λ��ͬһ���ڣ����й�ϵ��ȷ����
λ��ͬһ���ڣ����й�ϵ��ȷ����
A. ��ԭ�ԣ�As3����S2����Cl��
B. ���ȶ��ԣ�HCl��AsH3��HBr
C. ԭ�Ӱ뾶��As��Cl��P
D. ���ԣ�H3AsO4��H2SO4��H3PO4
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com