
【题目】X2+ 和Y- 与氩(18Ar)的电子层结构相同,下列判断中不正确的是
A.原子半径: X>YB.原子序数: X>Y
C.最外层电子数: X>YD.电子层数: X>Y
 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:
【题目】某同学需要配制450 mL 0.5 mol·L-1的NaOH溶液。请回答下列问题:
(1)在实验过程中用到的玻璃仪器有:玻璃棒、量筒、烧杯、______________、胶头滴管、试剂瓶。
(2)用托盘天平称量时,应将NaOH放在________称量,称取的固体质量为_______。
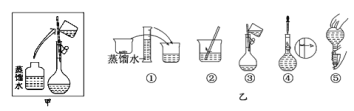
(3)配制时操作步骤如乙图所示,则甲图操作应在乙图中的___(填选项字母)之间。
A.①与② B.②与③ C.③与④ D.④与⑤
(4)配制过程中洗涤烧杯、玻璃棒2~3次的目的是______________________。
(5)定容滴加蒸馏水时,若不慎超过了刻度线,则处理的方法是______________。
(6)该同学实际配制NaOH溶液的浓度为0.6 mol·L-1,原因可能是____(填序号)。
a.砝码上有杂质
b.洗净的容量瓶中残留有少量水
c.称量NaOH固体时,采用了“左码右物”
d.定容时俯视刻度线
e.定容摇匀后发现液面低于刻度线又加入少许水调至刻度线
f.溶解固体的烧杯移液后未洗涤
g.定容前溶液未进行冷却
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)配平下列方程式
①___FeCl3 +___KI===____FeCl2+____KCl+_____I2
②____ClO-+_____Fe(OH)3+_____OH-===_____Cl-+____FeO![]() +____H2O
+____H2O
(2)用浓硫酸配制稀硫酸的过程中,下列操作会使配制的稀硫酸溶液浓度偏高的是___(填序号)。
①量取浓硫酸的量筒用蒸馏水洗涤2~3次,并把洗涤液转入容量瓶
②容量瓶使用时未干燥
③溶解后未经冷却就移液并定容
④定容时不小心有少量蒸馏水滴到瓶外
⑤定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务,如图是海水综合利用的一个方面。

Ⅰ.(1)上述过程中没有涉及到的四大基本反应类型是 ______;
a.化合反应 b.分解反应 c.置换反应 d.复分解反应
(2)步骤1中分离操作的名称是___________;
(3)粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用试剂为:
a.盐酸 b.BaCl2溶液 c.NaOH溶液 d.Na2CO3溶液
加入试剂的顺序是_____________;
II.实验室利用精盐配制480mL 2.0mol·L1NaCl溶液。
(4)除容量瓶外,还需要的玻璃仪器有___________________;
(5)用托盘天平称取固体NaCl________g;
(6)配制时,按以下几个步骤进行:①计算 ②称量 ③溶解 ④冷却 ⑤转移 ⑥定容 ⑦摇匀 ⑧装瓶。操作中还缺少一个重要步骤是______________________;
(7)下列错误操作可使所配制氯化钠溶液浓度偏低的是(_________)
a.容量瓶洗净后残留了部分的水
b.转移时溶液溅到容量瓶外面
c.定容时俯视容量瓶的刻度线
d.摇匀后见液面下降,再加水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向Ba(OH)2和NaOH的混合溶液中逐渐通入CO2气体至过量,生成沉淀的物质的量(n)和通入CO2气体的(V) 的关系如图所示,试回答:

(1)0到a点之间的反应的离子方程式__________
(2)a到b点之间的反应的离子方程式__________
(3)b点之后的反应的离子方程式______________
(4)c 点CO2的体积__________mL(同温同压下)。
(5) 混合溶液中Ba(OH)2和NaOH 的物质的量之比为__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是( )
甲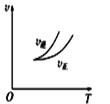 乙
乙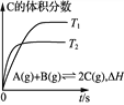 丙
丙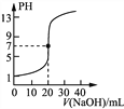 丁
丁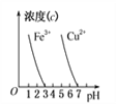
A. 由甲图甲可知正反应为放热反应
B. 乙表示在相同的密闭容器中,不同温度下的反应,该反应的ΔH>0
C. 丙表示0.1000mol·L-1NaOH溶液滴定20.00mL0.1000mol·L-1醋酸溶液的滴定曲线
D. 根据图丁,除去CuSO4溶液中的Fe3+,可加入NaOH调节pH至3~4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苹果汁是人们喜爱的饮料,由于此饮料中含有Fe2+ ,现榨的苹果汁在空气中会被氧化而由绿色变成棕黄色,若榨汁时加入某物质W,可有效防止这种现象发生。这说明物质W具有
A. 碱性 B. 酸性 C. 氧化性 D. 还原性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com