
【题目】向体积为2L的固定密闭容器中通入3molX气体,在一定温度下发生如下反应:2X(g) ![]() Y(g)+3Z(g)。
Y(g)+3Z(g)。
(1)经5min后达平衡,此时容器内压强为起始时的1.2倍,则用Y表示的速率为_____mol(L·min)。
(2)若上述反应在甲、乙、丙、丁四个同样的密闭容器中进行,在同一时间内测得的反应速率分别为:甲:ν(X)=3.5mol(L·min);乙:ν(Y)=2mol(L·min);丙:ν(Z)=4.5mol(L·min);丁:ν(X)=0.075mol(L·s)。若其他条件相同,温度不同,温度由高到低的顺序是(填序号)________________。
(3)若向达到(1)的平衡体系中充入氮气,则平衡向___(填“左”“右”或“不”,下同)移动。
(4)若在相同条件下向达到(1)所述平衡体系中再充入0.5molX气体,则平衡后X的转化率与(1)的平衡中X的转化率相比___。
A.无法确定 B.前者一定大于后者
C.前者一定等于后者 D.前者一定小于后者
【答案】0.03 丁>乙>甲>丙不B
【解析】
(1)达到平衡时容器内的压强为起始时的1.2倍,则反应后的气体物质的量为:3mol×1.2=3.6mol,增加了0.6mol,根据反应方程式可知
2X(g)![]() Y(g)+3Z(g) △n
Y(g)+3Z(g) △n
2 1 3 2
变化的物质的量 0.6mol 0.3mol 0.9mol 0.6mol
则用Y的物质的量浓度变化表示的速率为![]() =0.03 mol/(L·min);
=0.03 mol/(L·min);
(2)反应速率分别为甲:v(X)=3.5mol/(L·min),乙:v(Y)=2mol/(L·min),则用X表示为v(X)=4mol/(L·min),丙:v(Z)=4.5mol/(L·min),则用X表示为v(X)=3mol/(L·min),丁:v(X)=0.075mol/(L·s)=4.5mol/(L·min);其它条件相同,温度越高,速率越快,则温度由高到低的顺序是丁>乙>甲>丙;
(3)若向恒容的密闭容器中充入氮气,容积不变,浓度不变,则平衡不移动;
(4)若在相同条件下向达到(1)所述的平衡体系中再充入0.5molX气体,由于反应物只有一种,则相当于增大压强,平衡逆向移动,所以X的转化率降低,答案选B。


 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:
【题目】树脂交联程度决定了树脂的成膜性。下面是一种成膜性良好的醇酸型树脂的合成路线,如下图所示。

(1)A的系统命名为_______________;E中含氧官能团的名称是_____________。
(2)写出下列反应的反应类型:B→C____________;C→D:____________;
(3)C的结构简式为___________;1molC最多消耗NaOH_________mol。
(4)写出D、F在一定条件下生成醇酸型树脂的化学方程式_____________。
(5)![]() 的符合下列条件的同分异构体有_______种。
的符合下列条件的同分异构体有_______种。
①苯的二取代衍生物;②遇FeCl3溶液显紫色;③可发生消去反应
(6)利用上述反应原理,以丙烯为原料合成丙三醇,请你设计出合理的反应流程图:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某温度下可逆反应:Fe2(SO4)3+6KSCN![]() 2Fe(SCN)3+3K2SO4达到平衡状态后加入少量下列何种固体物质,该平衡几乎不发生移动( )
2Fe(SCN)3+3K2SO4达到平衡状态后加入少量下列何种固体物质,该平衡几乎不发生移动( )
A. NH4SCN B. K2SO4 C. NaOH D. FeCl3·6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应N2+3H2 ![]() 2NH3的能量变化下图所示,该反应的热化学方程式是
2NH3的能量变化下图所示,该反应的热化学方程式是
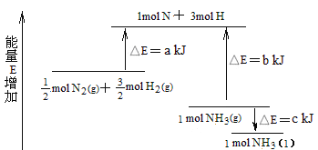
A.N2(g)+3H2(g) ![]() 2NH3(l) △H = 2(a-b+c) kJ/mol
2NH3(l) △H = 2(a-b+c) kJ/mol
B.N2(g)+3H2(g) ![]() 2NH3(l) △H = 2(a-b-c) kJ/mol
2NH3(l) △H = 2(a-b-c) kJ/mol
C.![]() N2(g)+
N2(g)+![]() H2(g)
H2(g) ![]() NH3(l) △H = (b+c-a) kJ/mol
NH3(l) △H = (b+c-a) kJ/mol
D.![]() N2(g)+
N2(g)+![]() H2(g)
H2(g) ![]() NH3(g) △H = (a+b) kJ/mol
NH3(g) △H = (a+b) kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关“绿色奥运”,下列环保建议中,你认为不能采纳的是
A.提倡生活垃圾分类收集
B.用天然气代替汽油和柴油作发动机燃料
C.禁止未经处理的工业废水和生活污水的任意排放
D.使用添加剂抑制水中所有动植物的生长
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z为短周期元素,X原子的质子数等于Z与Y的质子数之和;Z与Y位于同一周期,Y元素形成气态氢化物水溶液呈碱性,非金属Z的一种固体单质可导电。回答下列问题:
(1)Y在周期表中的位置是第_____周期、第____族,其原子结构示意图为_______.Y与Z之间形成的化学键属于___________(填离子键或共价键)。
(2) X、Y、Z三种元素中原子半径最大的是_______(填元素符号);X单质既可与盐酸反应,又可溶于氢氧化钠溶液,产生的气体为________(填分子式),该气体与Y单质反应的化学方程式______。
(3)Z的最价氧化物的电子式为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验设计或操作能达到实验目的是
A. 除去乙烷中的乙烯气体:加入氢气在催化剂的作用下发生加成反应
B. 检验溴乙烷消去产物:反应装置经水浴加热后,将生成物直接通入酸性高锰酸钾溶液中
C. 检验柠檬醛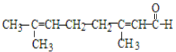 中含有碳碳双键:先加入银氨溶液充分反应后,再加入酸性高锰酸钾溶液检验
中含有碳碳双键:先加入银氨溶液充分反应后,再加入酸性高锰酸钾溶液检验
D. 除去甲苯中的少量苯酚:加入浓溴水,振荡、静置、过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由Li、Al、Si构成的某三元化合物固态晶胞结构如图所示,下列说法不正确的是
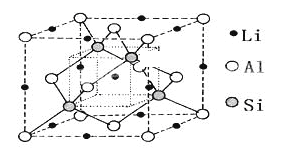
A. 晶体中Al和Si构成金刚石型骨架 B. 该化合物化学式可表示为LiAlSi
C. 晶体中与每个Al距离最近的Li为6个 D. 晶体中Al和Li构成CsCl型骨架
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com