
| |||||||||||
科目:高中化学 来源: 题型:
| 酸或碱 | 电离平衡常数(Ka或Kb) |
| CH3COOH | 1.8×10-3 |
| HNO3 | 4.6×10-4 |
| HCN | 5×10-10 |
| HClO | 3×10-8 |
| NH3?H2O | 1.8×10-5 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 1 |
| 2 |
| 1 |
| 2 |
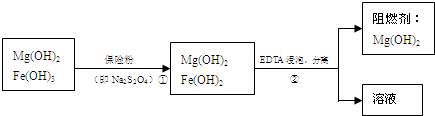
| 精制阻燃剂的条件 | 阻燃剂铁含量 | |||
| 序号 | 提纯体系温度T/℃ | 加入EDTA质量(g) | 加入保险粉质量(g) | W(Fe)/(10-4g) |
| 1 | 40 | 0.05 | 0.05 | 7.63 |
| 2 | 40 | 0.05 | 0.10 | 6.83 |
| 3 | 60 | 0.05 | 0.10 | 6.83 |
| 4 | 60 | 0.10 | 0.10 | 6.51 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
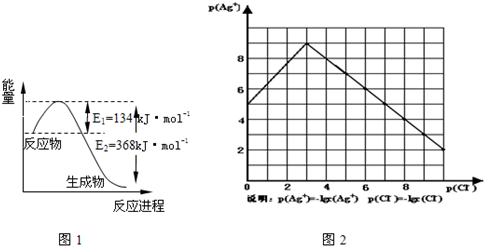
| t/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)合成氨反应的机理为
(1)合成氨反应的机理为 H2吸
H2吸 2H
2H 2H吸
2H吸 H2吸
H2吸 2H
2H 2H吸
2H吸 2N
2N 2N吸
2N吸 NH吸
NH吸 NH吸
NH吸 NH2吸;
NH2吸; NH3吸
NH3吸 NH3.
NH3. 2NH3(g);H=-92kJ?mol-1
2NH3(g);H=-92kJ?mol-1 2NH3(g);H=-92kJ?mol-1
2NH3(g);H=-92kJ?mol-1 NH4++NH2-(某温度下其离子积常数为10-30).液氨中的pNH4与水中的pH类似,则该温度下液氨的pNH4=
NH4++NH2-(某温度下其离子积常数为10-30).液氨中的pNH4与水中的pH类似,则该温度下液氨的pNH4= [N2H5?H2O]++H+
[N2H5?H2O]++H+ [N2H5?H2O]++H+
[N2H5?H2O]++H+查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 铜是人类最早使用的金属,被广泛应用于电气、轻工、机械制造和国防工业等.已知Cu2O与H2SO4能发生反应:Cu2O+H2SO4=Cu+CuSO4+H2O.
铜是人类最早使用的金属,被广泛应用于电气、轻工、机械制造和国防工业等.已知Cu2O与H2SO4能发生反应:Cu2O+H2SO4=Cu+CuSO4+H2O.
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com