
| A、X与Y可能形成XY化合物 |
| B、X与Y一定位于同一周期 |
| C、X与Y不可能位于同一主族 |
| D、X与Y都为主族元素 |


 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
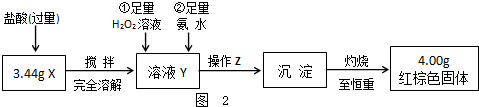
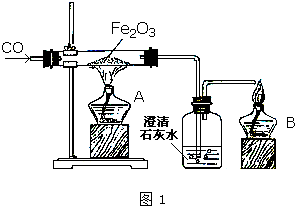 某研究性学习小组在用右图装置进行CO还原Fe2O3的探究实验.
某研究性学习小组在用右图装置进行CO还原Fe2O3的探究实验.| 实验编号 | 实 验 操 作 | 实 验 现 象 |
| ① | 取少量黑色粉末X放入试管1中,注入适量稀盐酸,微热. | 黑色粉末逐渐溶解, 有无色气体逸出. |
| ② | 向试管1所得溶液中滴加几滴 KSCN溶液,振荡. | 溶液未出现血红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
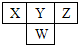 如图是元素周期表中短周期的一部分.已知Y和W原子能形成两种造成酸雨的有害气体,则下列说法不正确的是( )
如图是元素周期表中短周期的一部分.已知Y和W原子能形成两种造成酸雨的有害气体,则下列说法不正确的是( )| A、原子半径:W>Y>Z |
| B、X的氢化物不如Z的氢化物稳定 |
| C、Y的氢化物比W的氢化物沸点高,是因为存在氢键 |
| D、常见的X的氢化物具有正四面体结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:
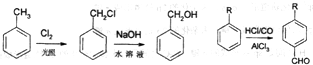 从A出发可发生如图所示的一系列反应,其中G为高分子化合物,化合物B的分子式为C8H8O,当以铁做催化剂进行氯化时,一元取代物只有两种.
从A出发可发生如图所示的一系列反应,其中G为高分子化合物,化合物B的分子式为C8H8O,当以铁做催化剂进行氯化时,一元取代物只有两种.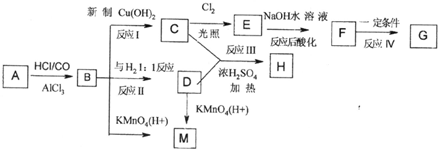
查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | 实验操作 | 预期现象和结论 |
| 步骤① | 取少量待测液加入试管中,加入过量的2mol?L-1盐酸,再滴加适量l mol?L-1BaCl2溶液. | 有白色沉淀生成,证明待测液中含SO42-. |
| 步骤② | ||
| 步骤③ |
| 序 号 | 所取Na2SO3溶液的体积 | 终点消耗KMnO4溶液的体积 |
| 1 | 25.00ml | 20.02ml |
| 2 | 25.00ml | 21.80ml |
| 3 | 25.00ml | 19.98ml |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com