
| A、v(A)=0.15 mol/(L?min) |
| B、v(B)=0.06 mol/(L?min) |
| C、v(C)=0.04 mol/(L?s) |
| D、v(D)=0.01 mol/(L?s)) |
| v(A) |
| 1 |
| v(B) |
| 3 |
| v(C) |
| 2 |
| v(D) |
| 2 |


 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案科目:高中化学 来源: 题型:
| A、加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32- |
| B、某溶液与NaOH溶液共热,产生使湿润蓝色石蕊试纸变红气体,说明原溶液中存在NH4+ |
| C、加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- |
| D、可用焰色反应实验检验溶液中是否含有K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、整个溶液变橙红色 |
| B、整个溶液变为紫红色 |
| C、上层为无色,下层为橙红色 |
| D、下层无色,上层紫红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定存在SO42-、CO32-、NH4+、Na+,可能存在K+、Cl- |
| B、一定存在SO42-、CO32-、NH4+、Na+、Cl-,一定不存在K+ |
| C、一定存在SO42-、CO32-、NH4+、Na+、Cl-,可能存在K+ |
| D、c(CO32-)=0.01 mol?L-1,c(NH4+)>c(SO42-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、充入1mol稀有气体氦(He),平衡将向正反应方向移动 |
| B、充入A、B、C各1mol,平衡将向正反应方向移动 |
| C、将A、B、C各物质的量都减半,C的百分含量变大 |
| D、加入一定量的A气体达平衡后,C的百分含量一定增加 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙烯、氯乙烯、聚乙烯均可使酸性高锰酸钾溶液褪色 |
| B、分子式为C4H7ClO2,可与NaHCO3产生CO2的有机物可能结构有3种 |
C、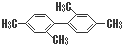 分子中至少有11个碳原子处于同一平面上 分子中至少有11个碳原子处于同一平面上 |
D、1mol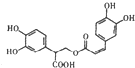 有机物 一定条件下能和7molNaOH反应 有机物 一定条件下能和7molNaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常数 | 1.70 | 1.10 | 1.00 | 0.60 | 0.40 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com