
����Ŀ����֪��H2��g��+I2��g��2HI��g����H=��14.9kJ/mol��ij�¶����ڼס������������ܱ������г��뷴Ӧ�����ʼŨ�����±���ʾ�����з�Ӧ�ﵽƽ��ʱ�����c��H2��=0.008mol/L�� �����ж���ȷ�ģ� ��
��ʼŨ�� | c��H2��/mol/L | c��I2��/mol/L | c��HI��/mol/L |
�� | 0.01 | 0.01 | 0 |
�� | 0.02 | 0.02 | 0 |
A.ƽ��ʱ������H2��ת�����Ǽ��е�2��
B.ƽ��ʱ�����л�������ɫ��������
C.ƽ��ʱ���ס����������ı仯ֵ���
D.���¶��£���Ӧ��ƽ�ⳣ��K=0.25
���𰸡�D
���������⣺A���÷�Ӧǰ�������������䣬���е�Ũ��Ϊ���е�2��������ѹǿΪ����2����ѹǿ��Ӱ��ƽ���ƶ�������Ϊ��Чƽ�⣬ƽ��ʱ��Ӧ����ֵ�ת������ͬ����A����B������Ϊ��Чƽ�⣬ƽ��ʱ����c��I2���Ǽ��е�2����ƽ��ʱ������ɫ�����B����
C������Ϊ��Чƽ�⣬��Ӧ��ת������ͬ�����вμӷ�ӦI2���Ǽ��е�2�������е������仯�Ǽ��е�2������C����
D��ƽ��ʱ������Ũ��Ϊ0.008mol/L����
H2��g��+I2��g��2HI��g����
��ʼ��mol/L����0.01 0.010
�仯��mol/L����0.002 0.0020.004
ƽ�⣨mol/L����0.008 0.0080.004
�ʸ��¶��¸÷�Ӧ��ƽ�ⳣ��k= ![]() =0.25����D��ȷ��
=0.25����D��ȷ��
��ѡD��
�����㾫�������û�ѧƽ�ⳣ���ĺ���ͻ�ѧƽ��״̬���ʼ���������Ŀ�����жϼ��ɵõ��𰸣���Ҫ��ָ֪��һ�������µĿ��淴Ӧ�����Ӧ���淴Ӧ��������ȣ���Ӧ������и���ֵ�Ũ�Ȳ����״̬����ѧƽ��״̬�����������ȡ��� V��=V��>0�����������Ƕ�̬ƽ�⣬ƽ��ʱ��Ӧ���ڽ��У�����������Ӧ������и���ְٷֺ������䣻���䡱�������ı䣬ƽ�ⱻ���ƣ������µ������½����µĻ�ѧƽ�⣻��;���أ�����������䣬���淴Ӧ�����Ǵ�����Ӧ��ʼ�����Ǵ��淴Ӧ��ʼ�����ɽ���ͬһƽ��״̬����Ч����


 ������״Ԫ��ҵϵ�д�
������״Ԫ��ҵϵ�д� ��ʱ�ƿ�������ϰϵ�д�
��ʱ�ƿ�������ϰϵ�д� һ��һ��һ��ͨϵ�д�
һ��һ��һ��ͨϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ж�������Ԫ�أ�������ѧ֪ʶ�ж�������������ǣ� ��
A. CH4B. HClC. NH3D. NaHSO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ѧ��ȤС��ѧ����ѧϰ������������ʺ�Ӧ�á�ʱ������������ʵ��̽����Ϊ����֤Ũ�����̼�ڼ��ȵ�����·�Ӧ���������ͼ��װ�ý���ʵ�顣

��1����д��̼��Ũ���ᷴӦ�Ļ�ѧ��Ӧ����ʽ_________________________________���÷�Ӧ���������뻹ԭ�������ʵ���֮��Ϊ_____________��
��2��ͼ����A�������ʵ���еı�Ҫװ�ã�������ͼ��ʾ�е�_________�������ţ�
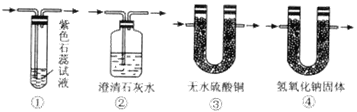
��3��ͼ����Cװ����Ӧʢ���Լ����Ϊ���㹻��_______________����������__________________��
��4��������_______________________ ��ʵ�����������ȷ�����ڶ�����̼���塣
��5����ʵ��С���ͬѧ��������ʵ�飬���ǽ����������������һ���ı���ͬʱͨ��Ʒ����Һ�У�һ��ʱ�����Ʒ����Һû����ɫ���Է���ʵ������У�Ʒ�첻��ɫ��ԭ��___________________�������ӷ�Ӧ����ʽ��ʾ��������Ϊ��ô����������Ʒ�����ɫԽ��Խdz��_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵı��淽������ȷ����
A. Ư��¶���ڿ����д��B. ��ˮ��������ɫ�Լ�ƿ��
C. ��������Ӧ�ܷⱣ��D. �����Ʊ�����ú����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������п�ͼ����������˵����ȷ���ǣ� �� 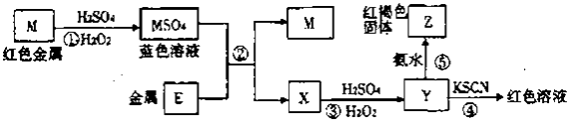
A.E2+�������Ա�M2+����������
B.�ڷ�Ӧ��������ȱ��������ԡ��ֱ�����������
C.��Ӧ�ܵ����ӷ���ʽ�ɱ�ʾΪ��3SCN��+E3+=E��SCN��3��
D.�ڢ۷�Ӧ��������ϡ������ܿ������ɫ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼʵ��װ���У�ʵ��ʱ���ȶϿ�K2 �� �պ�K1 �� �����������ݲ�����һ��ʱ��Ͽ�K1 �� �պ�K2 �� ���ֵ�����ָ��ƫת�������й�������ȷ���ǣ� �� 
A.�Ͽ�K2 �� �պ�K1ʱ���ܷ�Ӧ�����ӷ���ʽΪ��2H++2Cl�� ![]() Cl2��+H2��
Cl2��+H2��
B.�Ͽ�K2 �� �պ�K1ʱ�������ء�b��Cu���������Һ��ʯī��a����·������
C.�Ͽ�K2 �� �պ�K1ʱ��ͭ�缫������Һ���
D.�Ͽ�K1 �� �պ�K2ʱ��ͭ�缫�ϵĵ缫��ӦΪ��Cl2+2e��=2Cl��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȷ��ʾ���з�Ӧ�����ӷ���ʽ����(����)
A. ������NaOH��Һ��Ӧ��Al �� 2OH��===AlO![]() �� H2��
�� H2��
B. SiO2��NaOH��Һ��Ӧ��SiO2�� 2OH��===SiO![]() �� H2O
�� H2O
C. �Ȼ��Ũ��Һ��ŨNaOH��Һ��Ϻ���ȣ�NH![]() ��OH��
��OH��![]() NH3��H2O
NH3��H2O
D. ̼�������Һ��������NaOH��Һ��Ϻ���ȣ�NH![]() ��OH��
��OH��![]() NH3����H2O
NH3����H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���ѧϰС��ͬѧ�������ϵ�֪��Ư����������Һ��Ӧ����ȡ��������ѧ����ʽΪCa��ClO��2+CaCl2+2H2SO4 ![]() 2CaSO4+2Cl2��+2H2O�������������ͼ1��ʾ����ȡ��������֤�����ʵ�ʵ��װ�ã�
2CaSO4+2Cl2��+2H2O�������������ͼ1��ʾ����ȡ��������֤�����ʵ�ʵ��װ�ã� 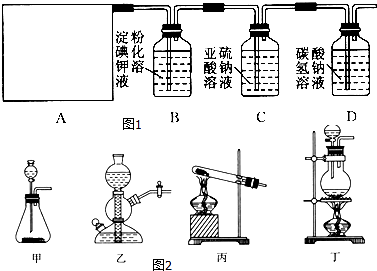
��ش��������⣺
��1����ʵ����A���ֵ�װ����ͼ2�е� ��
��2��A�з�����Ӧһ��ʱ���B�е������� �� B�з�����Ӧ�Ļ�ѧ����ʽΪ ��
����ʵ��װ�ô��ڵ�����ȱ���� ��
��3��д��Dװ���з�����Ӧ�����ӷ���ʽ ��
��4��������С��ͬѧ���һ��ʵ�飬֤��ϴ��ƿC�е�Na2SO3�ѱ�����ΪNa2SO4������ʵ�鲽�裩�� ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com