
【题目】(1)已知下列反应的焓变
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) △H1=-870.3kJ/mol
②C(s)+O2(g) =CO2(g) △H2=-393.5kJ/mol
③2H2(g)+O2(g) =2H2O(l) △H3=-285.8kJ/mol
试计算反应2C(s)+2H2(g)+O2(g) =CH3COOH(l)的焓变ΔH=_____________kJ/mol。
(2)实验测得,5g液态甲醇(CH3OH)在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,试写出甲醇燃烧的热化学方程式:_________________________。
(3)火箭推进器常以气态联氨(N2H4)为燃料、液态过氧化氢为助燃剂进行热能提供.反应过程中生成的气体可参与大气循环。测得当反应过程中有1mol水蒸气生成时放出161kJ的热量.试写出反应过程中的热化学方程式:___________________________。
【答案】 ΔH= -202.5 kJ/mol CH3OH(l) + 3/2O2(g) === CO2(g) + 2H2O(l) ΔH=-726.4kJ/mol N2H4(g) + 2H2O2(l) === N2(g) + 4H2O(g) ΔH=-644kJ/mol
【解析】(1)已知:
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) △H1=-870.3kJ/mol
②C(s)+O2(g)=CO2(g) △H2=-393.5kJ/mol
③2H2(g)+O2(g)=2H2O(l) △H3=-285.8kJ/mol
根据盖斯定律可知②×2+③-①即可得到反应2C(s)+2H2(g)+O2(g)=CH3COOH(l)的焓变ΔH=-202.5kJ/mol。
(2)实验测得,5g液态甲醇(CH3OH)在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,则1mol甲醇即32g甲醇完全燃烧放出的热量是![]() ,因此甲醇燃烧的热化学方程式为CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l) ΔH=-726.4kJ/mol。
,因此甲醇燃烧的热化学方程式为CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l) ΔH=-726.4kJ/mol。
(3)反应过程中生成的气体可参与大气循环,根据原子守恒可知应该是氮气和水蒸气。测得当反应过程中有1mol水蒸气生成时放出161kJ的热量,所以反应过程中的热化学方程式为N2H4(g)+2H2O2(l)=N2(g)+4H2O(g) ΔH=-644kJ/mol。


科目:高中化学 来源: 题型:
【题目】下列相关实验的叙述中,正确的是( )
A. HClO、活性炭均能使某些有色物质褪色,说明二者均有氧化性
B. 加热分别盛有NaHCO3和碘的两支试管,试管底部固体均减少,说明二者均发生升华
C. 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热,熔化后的液态铝滴落下来
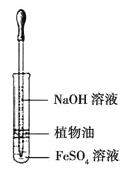
D. 用上图装置观察 Fe(OH)2 的生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如下的反应关系:
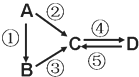
(1)若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体。写出②反应的离子方程式_________;④反应离子方程式__________。
(2)若A是应用最广泛的金属。④反应用到A,②⑤反应均用到同一种黄绿色气体单质。写出A与水高温下反应的化学方程式_______________________。④反应的离子方程式______________。D中加入氢氧化钠的现象__________。
(3)若A是太阳能电池用的光伏材料,B常用用于制作高档光学器材,C、D为钠盐,C的水溶液俗称泡花碱,D的溶液显碱性。④反应也是通入一种引起温室效应的主要气体。写出③反应的化学方程式________________________。⑤反应用到B,反应条件为高温,则⑤的化学方程式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于常温下pH=3的CH3COOH溶液,下列叙述不正确的是( )
A. c(H+)= c(CH3COO-)+ c(OH-)
B. 加入少量CH3COONa固体后,c(CH3COO-)降低
C. 该溶液中由水电离出的c(H+)是1.0×10-11mol/L
D. 与等体积pH =11的NaOH溶液混合后溶液显酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】84消毒液(有效成分是次氯酸钠)、漂白粉(有效成分是次氯酸钙)等物质是日常生活中常用的消毒剂,广泛应用于日常生活中。根据下列要求回答相关问题:
(1)在0.1 mol·L-1的84消毒液中滴加几滴酚酞试液,可能观察到的现象是______________,写出反应的离子方程式:______________________________。
(2)某同学测定漂白粉溶液pH的操作方法:将一小块pH试纸放在表面皿上,用玻璃棒蘸取少量待测液滴在试纸上,大约半分钟后,再与标准比色卡对照。你认为他能否达到实验目的?________(填“能”或“否”)。
(3)下列关于0.5 mol·L-1 NaClO溶液中各粒子浓度的关系式正确的是____________。
A.c(OH-)>c(H+)>c(Na+)>c(ClO-) B.c(Na+)=c(ClO-)+c(HClO)
C.c(Na+)>c(ClO-)>c(OH-)>c(H+) D.c(Na+)+c(H+)=c(ClO-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
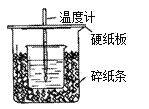
(1)从实验装置上看,图中尚缺少的一种玻璃用品是________。
(2)烧杯间填满碎纸条的作用是_______________________。
(3)大烧杯上如不盖硬纸板,求得的中和热数值__________(填“偏大、偏小、无影响”)。
(4)实验中改用60 mL 0.50 mol·L-1的盐酸跟50 mL 0.55 mol·L-1的NaOH溶液进行反应,与上述实验相比,所放出的热量_________(填“相等”或“不相等”),所求中和热_____________ (填“相等”或“不相等”)。
(5)此反应中和热的热化学方程式为:________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案合理的是( )
A. 可用酸性高锰酸钾溶液除去甲烷中混有的杂质乙烯
B. 可用溴水鉴别己烯、己烷和四氯化碳
C. 制备氯乙烷:将乙烷和氯气的混合气放在光照条件下反应
D. 证明溴乙烷与NaOH醇溶液共热生成了乙烯:用如图所示的实验装置

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】摩尔盐[(NH4)2Fe(SO4)2·6H2O]是一种重要的化工原料,可用于制取纳米Fe3O4和草酸合铁酸钾等。
(1)取一定质量摩尔盐样品与过量NaOH溶液反应。
①根据生成气体的体积计算得到摩尔盐的纯度小于实际值,其原因是______。
②向所得Fe(OH)2沉淀中加入NaNO2溶液可制得纳米Fe3O4,同时产生NO。该反应的离子方程式为______。
(2)摩尔盐经氧化后与KOH和H2C2O4反应可得到草酸合铁酸钾[KaFeb(C2O4)c·dH2O],其中Fe元素化合价为+3。
①已知25 ℃,H2C2O4的电离常数Ka1=5.6×10-2,Ka2=5.4×10-5。pH=4的H2C2O4溶液中c(C2O![]() ):c(HC2O)=______。
):c(HC2O)=______。
②为了确定草酸合铁酸钾的组成,准确称取4.910 g样品在氮气气氛下加热,固体样品的剩余质量随温度的变化如图所示。
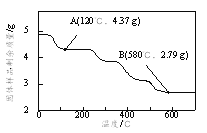
已知:a.120℃时已完全失去结晶水。
b.200℃~580℃分解产生的CO和CO2恢复至标准状况下体积为1.008 L。
c.580℃以上残留固体为FeO和K2CO3的混合物。
根据以上实验数据计算草酸合铁酸钾中的n(Fe3+):n(C2O42-)_____________(写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随原子序数的递增,八种短周期元素(用字母X表示)原子半径的相对大小、最高正价或最低负价的变化如下左图所示,根据判断出的元素回答问题:

⑴ f在元素周期表的位置是__________。
⑵ 比较d、e常见离子的半径的小(用化学式表示,下同)_______>__________比较g、h的最高价氧化物对应的水化物的酸性强弱是:_______>__________
⑶ 任选上述元素组成一种四原子共价化合物,写出其电子式____________________
⑷ 已知1mole的单质在足量d2中燃烧,恢复至室温,放出255.5kJ热量,写出该反应的热化学方程式____________
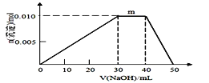
⑸ 上述元素可组成盐R:zx4f(gd4)2,向盛有10mL1mol·L-1R溶液的烧杯中滴加1mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如上右图所示:
① R溶液中离子浓度由大到小的顺序是________________
② 写出m点反应的而离子方程式________________________________
③ 若R溶液改加20mL1.2 mol·L-1Ba(OH)2溶液,充分中产生沉淀的物质的量为_______mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com