
【题目】如图装置中,小试管内为红墨水,带有支管的U型管中盛有pH=4的雨水和生铁片。经观察,装置中有如下现象:开始时插在小试管中的导管内的液面下降,一段时间后导管内的液面回升,略高于U型管中的液面。以下有关解释合理的是

A.生铁片中的碳是原电池的负极,发生还原反应
B.雨水酸性较强,生铁片始终发生析氢腐蚀
C.墨水液面回升时,正极反应式为:O2+2H2O+4e-===4OH-
D.U型管中溶液pH逐渐减小
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子一定能在指定溶液中大量共存的是 ( )
A. 水电离的![]() =1×10-13mol/L的溶液:K+、Na+、AlO2—、CO32—
=1×10-13mol/L的溶液:K+、Na+、AlO2—、CO32—
B. ![]() =1×10-12mol/L的溶液中:Cu2+、NH4+、Cl-、NO3-
=1×10-12mol/L的溶液中:Cu2+、NH4+、Cl-、NO3-
C. 与Al反应能放出H2的溶液:Cu2+、NO3—、K+、SO42—
D. 无色溶液中:Cr2O72—、Na+、H+、SO42—
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一可逆反应:2A(g)+3B(g) ![]() xC(g)+4D(g),若按下列两种配比在同温同体积的密闭容器中进行反应:①0.8 mol A+1.2 mol B+1.2 mol C+2.4 mol D②1.4 mol A+2.1 mol B+0.6 mol C+1.2 mol D达平衡后,C的质量分数相等,则方程式中x的值为( )
xC(g)+4D(g),若按下列两种配比在同温同体积的密闭容器中进行反应:①0.8 mol A+1.2 mol B+1.2 mol C+2.4 mol D②1.4 mol A+2.1 mol B+0.6 mol C+1.2 mol D达平衡后,C的质量分数相等,则方程式中x的值为( )
A. 1B. 2C. 3D. 4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下可逆反应:A(s)+2B(g)![]() 2C(g)+D(g);DH<0。现将1 mol A和2 mol B加入甲容器中,将4 mol C和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是
2C(g)+D(g);DH<0。现将1 mol A和2 mol B加入甲容器中,将4 mol C和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是



图1 图2 图3
A.保持温度和活塞位置不变,在甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍
B.保持活塞位置不变,升高温度,达到新的平衡后,甲中B的体积分数增大,乙中B的体积分数减小
C.保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍
D.保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以石墨为电极分别电解水和饱和食盐水,关于两个电解池反应的说法正确的是( )
A.阳极反应式相同
B.电解结束后所得液体的pH相同
C.阴极反应式相同
D.通过相同电量时生成的气体总体积相等(同温同压)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于NA下列说法正确的是
A. 常温常压下,17g羟基(—18OH)所含中子数为9NA
B. 0.1mol NH3溶于水形成的溶液中,微粒NH3·H2O和微粒NH4+的数目之和为0.1NA
C. 常温下电解饱和食盐水,当溶液pH值由7变为12时,电路中转移的电子数为0.01NA
D. 标准状况下,足量的甲烷与22.4LCl2(假设氯气完全反应)在光照条件下发生取代反应,形成C-Cl键的数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列叙述正确的是( )
A. 室温下,1LpH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA
B. 1mol硝基(-NO2)与46g二氧化氮所含的电子数均为23NA
C. 16.2g14C10H22中含有的共价键数目为3.2NA
D. 向含1molFeI2的溶液中通入1molCl2充分反应,该反应转移电子数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方法或操作正确的是( )
A.用标准氢氧化钠溶液滴定待测醋酸,选用酚酞作指示剂
B.配制![]() 溶液时,将
溶液时,将![]() 固体溶解在硫酸中,然后再加水稀释到所需的浓度
固体溶解在硫酸中,然后再加水稀释到所需的浓度
C.测定某溶液的pH时,用pH试纸蘸取待测液,然后和比色卡对比得出pH
D.将淀粉溶液加到饱和食盐水中,检验食盐是否是加碘食盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式碳酸铜[Cu2(OH)2CO3]是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的步骤如下:
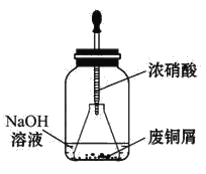
步骤一:废铜屑制硝酸铜
如图,用胶头滴管吸取浓硝酸缓慢加到锥形瓶内的废铜屑中(废铜屑过量),充分反应后过滤,得到硝酸铜溶液。
步骤二:碱式碳酸铜的制备
向大试管中加入碳酸钠溶液和硝酸铜溶液,水浴加热至70℃左右,用0.4 mol·L-1的NaOH溶液调节pH至8.5,振荡,静置,过滤,用热水洗涤,烘干,得到碱式碳酸铜产品。
完成下列填空:
(1)写出浓硝酸与铜反应的离子方程式_________________________________。
(2)上图装置中NaOH溶液的作用是____________________________________。
(3)步骤二中,水浴加热所需仪器有____________、____________(加热、夹持仪器、石棉网除外),水浴加热的优点是_________________________________。
(4)若实验得到2.42 g样品(只含CuO杂质),取此样品加热至分解完全后,得到1.80 g固体,此样品中碱式碳酸铜的质量分数是____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com