
����Ŀ�����ںͽ�������ᣬ����Դ�Ͳ��ϵ�������Խ��Խ������ѧϰ��ѧ��Ϊ����ʶ���ʣ��������ʣ���������Դ����չ�������δ�������������й���Դ�����⣺
��1��δ������Դ���ص�����Դ�ḻ����ʹ��ʱ�Ի�������Ⱦ����Ⱦ��С���ҿ�����������������δ������Դ�����ǣ�________
����Ȼ����ú��������ʯ����̫��������������������������
A���٢ڢۢ� B���ݢޢߢ� C���ۢݢޢߢ� D���ۢܢݢޢߢ�
��2���˶�����ʹ�õĻ���ȼ��һ���DZ���(C3H8)����������������Ŀ��
����֪11g����(C3H8)��298K��101Kpa��������ȫȼ������CO2��Һ̬ˮʱ�ų�������Ϊ555kJ����д������ȼ���ȵ��Ȼ�ѧ����ʽ��_____________��
���Ա���(C3H8)�Ϳ���Ϊԭ�ϣ�ϡ����Ϊ�������Һ_____________(���ܻ���)��Ƴɳأ�
���ܣ���д��ͨ�����(C3H8)����һ��Ϊ��_____________����������_____________��������Ӧ��
�����ܣ��������ǣ�_____________��
��������һ�������·������ⷴӦ���Եõ���ϩ��
��֪��C3H8(g)��CH4(g)��HC��CH(g)��H2(g)��H1=+156.6kJ��mol��1
CH3CH=CH2(g)��CH4(g)��HC��CH(g)��H2=+32.4kJ��mol��1
����ͬ�����£���ӦC3H8(g)��CH3CH=CH2(g)��H2(g)����H=_______
��3����֪��H��H���ļ���Ϊ436KJ/mol��H��N���ļ���Ϊ391KJ/mol�����ݻ�ѧ����ʽ��N2+3H2![]() 2NH3��H=-92.4KJ/mol��
2NH3��H=-92.4KJ/mol��
��������N��N���ļ���Ϊ_______________��
�������������Ȼ�ѧ����ʽ��ͬ�¶Ⱥ����һ���������У�ͨ��1molN2��3molH2����ַ�Ӧ�ָ�ԭ�¶�ʱ�ų�������_______________92.4KJ(����ڻ�С�ڻ����)��
���𰸡�
��1��C��
��2����C3H8(g)��5O2(g)=3CO2(g)��4H2O(l)��H=��2220kJ��mol��1��
���ܣ�������������H=124.2kJ��mol��1
��3����945.6KJ/mol����С�ڡ�
��������
�����������1��ú��ʯ�͡���Ȼ���ǻ�ʯ��Դ����������Դ����������Դ�У�̫���ܡ����ܡ������ܡ���ϫ�ܡ����ܡ����ܡ��������ܵ�����ѡC��
��2����11g��������ʵ���Ϊ��![]() =0.25mol����1mol������ȫȼ�շų�������Ϊ��55kJ ��
=0.25mol����1mol������ȫȼ�շų�������Ϊ��55kJ �� ![]() = 2220kJ�������ȼ�յ��Ȼ�ѧ����ʽΪ��C3H8(g) + 5O2(g) = 3CO2(g)+4H2O(l) ��H=-2220 kJmol-1��
= 2220kJ�������ȼ�յ��Ȼ�ѧ����ʽΪ��C3H8(g) + 5O2(g) = 3CO2(g)+4H2O(l) ��H=-2220 kJmol-1��
��ȼ�ϵ���У�������ȼ��C3H8�����ʧ���ӷ���������Ӧ���������������õ��ӷ�����ԭ��Ӧ�������缫��ӦʽΪC3H8-20e-+10CO32-=13CO2+4H2O��������ӦʽΪ��O2+2CO2+4e-=2CO32-���������ط�ӦʽΪC3H8+5O2�T3CO2+4H2O���ŵ�ʱ����������������ƶ���������������෴����̼����������ƶ����ʴ�Ϊ���ܣ���������
����֪����C3H8(g)�TCH4(g)+HC��CH(g)+H2(g) ��H1=156.6kJmol-1��
��CH3CH=CH2(g)�TCH4(g)+HC��CH(g) ��H2=32.4kJmol-1��
���ݸ�˹���ɣ���-����C3H8(g)�TCH3CH=CH2(g)+H2(g)����������H=��H1-��H2=156.6kJmol-1-32.4kJmol-1=124.2kJmol-1���ʴ�Ϊ��124.2kJmol-1��
��3������֪��H-H����Ϊ436kJ/mol��H-N����Ϊ391kJ/mol����N��N�ļ���Ϊx�����ڷ�ӦN2(g)+3H2(g)=2NH3(g)��H=-92.4kJ/mol����Ӧ��=��Ӧ����ܼ���-��������ܼ��ܣ���x+3��436kJ/mol-2��3��391kJ/mol=-92.4kJ/mol����ã�x=945.6kJ/mol���ʴ�Ϊ��945.6kJ/mol��
��N2��H2�ķ�Ӧ���ڿ��淴Ӧ��������ȫ���У����1molN2��3molH2����ַ�Ӧ�ָ�ԭ�¶�ʱ�ų�������С��92.4KJ���ʴ�Ϊ��С�ڡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڵ������Һ����������ȷ����( )
A��Na2CO3��NaHCO3��������Һ�У����������ͬ
B�������£�1 mol��L-1��CH3COOH��Һ��1 mol��L-1��NaOH��Һ�������Ϻ����û��Һ�У�c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
C�����ʵ���Ũ����ͬ��NH4Cl��NH4HSO4������Һ�У�c(NH![]() )ǰ��С�ں���
)ǰ��С�ں���
D�������£�ij��Һ����ˮ�������c(H+)��10-5 mol��L-1�������Һ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���谢��٤��������ֵΪNA������˵����ȷ���ǣ�
A��0.5mol��NaHSO4�����к��е�����������ΪNA
B��0.1mol/L FeCl3����Һ�У���Cl-��ĿΪ0��3 NA
C����״����22��4LNO2������ˮ��ȫ��Ӧʱ��ת�Ƶ�����ĿΪNA
D�����³�ѹ�£�23gNO2��N2O4�Ļ����������ԭ����ĿΪ1.5 NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ӽ������õ���ʷ������������ͭ��ʱ��������������ʱ�������������ǽ�������¡�����Ⱥ�˳��������йص��ǣ�
���ؿ��еĽ���Ԫ�صĺ�������������ԣ��������ĵ����ԣ�������ұ�������׳̶ȣ�����������չ�ԣ�
A. �٢� B. �ڢ� C. �ۢ� D. �ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��һ����ѧ���̵�ʾ��ͼ��
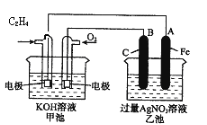
����ݸ�ʾ��ͼ���������Ŀ��
��1�����ʣ��׳���________װ�ã��ҳ���________װ�á�
��2���ڼ׳��У�ͨ��C2H4�ĵ缫������___________��ͨ��O2�ĵ缫�ĵ缫��Ӧʽ��________���׳��з����ķ�Ӧ�Ļ�ѧ����ʽΪ��________��
��3�����ҳ��У�B(ʯī)������������________��A(Fe)�缫�ĵ缫��ӦʽΪ________��
��4���ҳ��з�Ӧ�Ļ�ѧ����ʽΪ________��
��5�����ҳ���A(Fe)������������5.40gʱ���׳�������������O2________mL(��״����)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼʾ���Ӧ������������ǣ�������
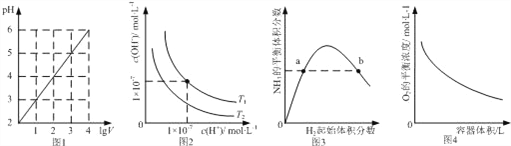
A. ͼ1��ʾ1 LpH=2��CH3COOH��Һ��ˮϡ����V L��pH��lgV�ı仯
B. ͼ2��ʾ��ͬ�¶���ˮ��Һ��H+��OH��Ũ�ȵı仯�����ߣ�ͼ���¶�T2��T1
C. ͼ3��ʾһ�������µĺϳɰ���Ӧ�У�NH3��ƽ�����������H2��ʼ���������N2����ʼ���㶨���ı仯��ͼ��a��N2��ת����С��b��
D. ͼ4��ʾͬһ�¶��£��ڲ�ͬ�ݻ��������н��з�Ӧ2BaO2��s��![]() 2BaO��s��+O2��g����O2��ƽ��Ũ���������ݻ��Ĺ�ϵ
2BaO��s��+O2��g����O2��ƽ��Ũ���������ݻ��Ĺ�ϵ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NO���������������Ѹ�ٷ�����Ӧ����ѧ�ҷ������������в��ϵز���NO������ϸ���䴫����Ϣ��NO��������Ѫ��ϵͳ������ϵͳ�Լ��������Χ��ϵͳ�ĵ��ء�
��.(1)ʵ�����ý���ͭ��ϡ������ȡNO�����ӷ���ʽΪ
___________________________________________________��
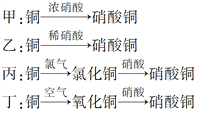
(2)NO���ж����壬ijѧ��Ϊ��ֹ��Ⱦ���÷�Һ©�����ձ�װ����һ���ġ����濪���á������ͣ��NO���巢��װ�ã���ͼ����ʾ��
��ʵ������û��ͭ˿����ֻ��Сͭ������ʹ������װ�ý���ʵ��ʱ������˿״���ϰ���ͭ���Դ���ͭ˿����ʵ�飬����˿״���ϵijɷֿ�����________(��ѡ����)��
A���� B���� C���� D������
�ڴ�Һ©���Ļ���ʹ��Ӧ���У��ڷ�Һ©����ʵ�ʿ����������Ǻ���ɫ�ģ�ԭ����____________________(�ѧ����ʽ)��
(3)Ϊ֤��ͭ˿��ϡ���ᷴӦ���ɵ�ȷʵ��NO��ijѧ���������һ����ͼ����ʾ��װ����ȡNO�����Ϳ�ʼ������U�ι��Ҷ˹۲쵽��ɫ��NO���塣
�ٳ������ܵ�������___________________________________��
���÷�Ӧֹͣ�IJ���������ԭ����________________________��
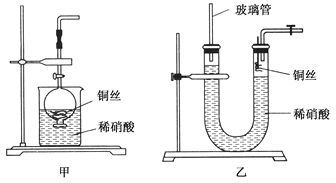
(4)�����ռ�NO�����װ�ã���������________(��ѡ�����)��
(5)����ʵ����12.8 g Cuȫ���ܽ⣬��Ҫͨ������________mL O2����ʹNOȫ������ˮ��
��.�ý���ͭ��ȡ����ͭ���ӽ�Լԭ�Ϻͷ�ֹ������Ⱦ�ĽǶȿ��ǣ�����4�ַ�������õ���________(��ס������ҡ�������������)��������___________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
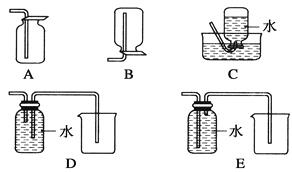
����Ŀ��ʵ����ģ��ϳɰ��Ͱ����������������£�

��֪ʵ���ҿ��ñ�����������(NaNO2)��Һ�뱥���Ȼ����Һ�����Ⱥ�Ӧ��ȡ������
(1)����ͼ��ѡ����ȡ����ĺ���װ�ã�����________������________��
(2)����������ͨ����װ�ã���װ�õ����ó��˽��������⣬����________��________��

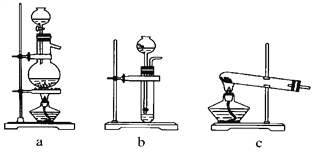
(3)���ϳ�����������ȴ����������ͨ����װ�õ�ˮ�����հ���________(���ᡱ���ᡱ)����������ԭ����_________________��
(4)����װ������һ��ʱ�䰱����ͨ�������ͬʱ�������ȵIJ�˿������װ�õ���ƿ�ڣ���ʹ��˿���ֺ��ȵ�ԭ����________����ƿ�л��ɹ۲쵽��������____________________________��
(5)д����װ���а������Ļ�ѧ����ʽ��_____________________________________________��
(6)��Ӧ��������ƿ�ڵ���Һ����H����OH����______��________���ӡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2016��10��17�գ��ҹ��ɹ���������ʮһ�����˷ɴ����ɴ����ٽ����������¶Ȼ�Ѹ�����ߣ������ĸ��ϲ��Ͽɱ����ɴ������ƻ����������˸ø��ϲ��Ͼ��е��ص���
A�������� B�������� C����ʴ D���ͼ���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com