
【题目】某硫酸铵样品中混有硫酸氢铵。称取不同质量的样品分别于100mL 2.300mol/L的氢氧化钠溶液充分反应,得到的实验数据入下表:
实验序号 | Ⅰ | Ⅱ |
样品质量(g) | 14.35 | 28.70 |
氨气质量(g) | 3.570 | 3.570 |
下列说法错误的是
A. 样品中硫酸铵与硫酸氢铵的物质的量之比为9:1
B. 实验Ⅰ中氢氧化钠一定过量
C. 要使实验Ⅱ的样品完全反应,需要再加入氢氧化钠0.2100mol
D. 样品中氮元素的质量分数是20.49%
【答案】A
【解析】
A.实验Ⅰ中固体混合物完全反应,令硫酸铵、硫酸氢铵的物质的量分别为xmol、ymol,根据二者质量及生成氨气质量列方程,则:132x+115y=14.35、2x+y=3.5717,解得x=0.1、y=0.01,故样品中硫酸铵与硫酸氢铵的物质的量之比为0.1mol:0.01mol=10:1,故A错误;
B.首先发生反应:H++OH-=H2O,然后发生反应:NH4++OH-![]() NH3↑+H2O,NaOH的量一定,实验Ⅰ、Ⅱ都是生成氨气,说明混合物中H+完全反应,实验Ⅱ中固体混合物质量较大,而生成氨气相等,说明实验Ⅰ中氢氧化钠有剩余,否则,实验Ⅱ中生成的氨气应较少,故B正确;
NH3↑+H2O,NaOH的量一定,实验Ⅰ、Ⅱ都是生成氨气,说明混合物中H+完全反应,实验Ⅱ中固体混合物质量较大,而生成氨气相等,说明实验Ⅰ中氢氧化钠有剩余,否则,实验Ⅱ中生成的氨气应较少,故B正确;
C.28.70g固体中硫酸铵的物质的量=0.1mol×28.7g/14.35g=0.2mol、硫酸氢铵的物质的量=0.01mol×28.7g/14.35g=0.02mol,完全反应时,溶液中溶质为硫酸钠,根据守恒可知,n(NaOH)=2n(Na2SO4)=(0.2mol+0.02mol)×2=0.44mol,故需要加入NaOH的物质的量=0.44mol-0.1L×2.3mol/L=0.2100mol,故C正确;
D.利用实验Ⅰ中的数据计算,根据氮元素守恒可知,混合物中N元素质量=14g/mol×3.57g÷17g/mol=2.94g,故混合物中N元素质量分数=2.94g÷14.35g×100%=20.49%,故D正确。
故选A。


科目:高中化学 来源: 题型:
【题目】一种气态烷烃和一种气态烯烃,它们分子里的碳原子数相等.将1.0体积这种混合气体在氧气中完全燃烧,生成2.0体积的CO2和2.4体积的水蒸气(气体体积均在相同状况下测定),则混合气体中烷烃和烯烃的体积比为( )
A.3:1 B.1:3 C.2:3 D.3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知C—C可以绕键轴旋转,对于结构简式如图所示的烃,下列说法正确的是
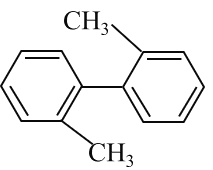
A.该物质不能发生加成反应
B.分子中至少有9个碳原子处于同一平面上
C.该烃的一氯取代物最多有5种
D.该烃是苯的同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组探究石蜡油分解产物,设计了如图实验方案。下列说法错误的是
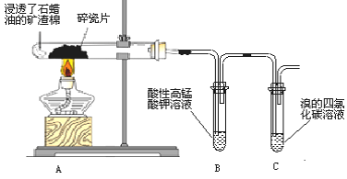
A.碎瓷片有催化和积蓄热量的作用
B.点燃C 出口处,火焰明亮,伴有黑烟
C.B、C 中溶液均褪色,反应类型相同
D.结束反应时,先撤出导管,再停止加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关铜的化合物说法正确的是( )
A. 根据铁比铜金属性强,在实际应用中可用FeCl3腐蚀Cu刻制印刷电路板
B. CuSO4溶液与H2S溶液反应的离子方程式为:Cu2++S2-![]() CuS↓
CuS↓
C. 用稀盐酸除去铜锈的离子方程式为CuO+2H+===Cu2++H2O
D. 化学反应:CuO+CO![]() Cu+CO2的实验现象为黑色固体变成红色固体
Cu+CO2的实验现象为黑色固体变成红色固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、Q、R 皆为前20号元素,其原子半径与化合价的关系如图所示。下列说法错误的是

A.QX 中只存在离子键
B.简单离子半径:r(M-)>r(Q+)>r(R2+)
C.X、Y、Z 三种元素组成的化合物可能是盐或碱
D.ZM3 各原子最外层电子数均满足8 电子结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F是核电荷数依次增大的六种短周期主族元素,A元素的原子核内只有1个质子;B元素的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层多4;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C;C、E同主族。
(1)B在周期表中的位置_________
(2)F元素的最高价氧化物对应的水化物的化学式为________。
(3)元素C、D、E形成的简单离子半径由小到大的顺序________(用离子符号表示)。
(4)写出化合物D2C2的电子式:________。
(5)E、F的简单离子的还原性大小顺序为:_________。
(6)已知E单质和F单质的水溶液反应会生成两种强酸,其离子方程式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室从含碘废液(除H2O外,含有CCl4、I2、![]() 等)中回收碘,实验过程如下:
等)中回收碘,实验过程如下:

(1)向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其离子方程式为_______;该操作将I2还原为I-的目的是___________________。
(2)操作![]() 的名称为__________。
的名称为__________。
(3)氧化时,在三颈瓶中将含I-的水溶液用盐酸调至pH约为2,缓慢通入Cl2,在40℃左右反应(实验装置如图所示)。实验控制在较低温度下进行的原因是__________________;仪器a的名称为________;仪器b中盛放的溶液为__________。

(4)已知:![]() ;某含碘废水(pH约为8)中一定存在I2,可能存在I-、IO3-中的一种或两种。请补充完整检验含碘废水中是否含有I-、IO3-的实验方案(实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液、Na2SO3溶液)。
;某含碘废水(pH约为8)中一定存在I2,可能存在I-、IO3-中的一种或两种。请补充完整检验含碘废水中是否含有I-、IO3-的实验方案(实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液、Na2SO3溶液)。
①取适量含碘废水用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出有碘单质存在;
②_______________________________________________________________________________;
③另从水层中取少量溶液,加入1-2mL淀粉溶液,加盐酸酸化后,滴加Na2SO3溶液,若溶液变蓝说明废水中含有IO3-;否则说明废水中不含有IO3-。
(5)二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂和水处理剂。现用ClO2氧化酸性含废液回收碘。完成ClO2氧化I-的离子方程式:________________________________。
(6)“碘量法”是一种测定S2-含量的有效方法。立德粉ZnS·BaSO4是一种常用的白色颜料,制备过程中会加入可溶性的BaS,现用“碘量法”来测定立德粉样品中S2-的含量。称取m g样品,置于碘量瓶中,移取25.00 mL 0.1000 mol/L 的I2-KI溶液于其中,并加入乙酸溶液,密闭,置暗处反应5min,有单质硫析出。以淀粉为指示剂,过量的I2用0.1000 mol/L Na2S2O3 滴定,反应式为I2 + 2S2O32-=2I-+ S4O62-。测定消耗Na2S2O3溶液体积V mL。立德粉样品S2-含量为__________(写出表达式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】爱国实业家侯德榜在氨碱法的基础上,发明了“联合制碱法”,简单流程如图。完成下列问题:

(1)在饱和食盐水中通入X和Y,则X____(填物质名称)
(2)写出通入X和Y的化学反应方程式_____。
(3)操作Z____(填名称),为了得到化肥(NH4Cl),需要在溶液B中通入NH3、加食盐,其中通入NH3的作用一____,作用二____。
(4)工业生产的纯碱常会含少量NaCl杂质。现用重量法测定其纯度,步骤如下:①称取样品ag,加水溶解;②加入足量的BaCl2溶液;③过滤、___、烘干、冷却、称量、烘干、冷却、___,最终得到固体bg。样品中纯碱的质量分数为____(用含a、b的代数式)
(5)某课外活动小组要用NaOH溶液和CO2来制备Na2CO3固体,他们只有未知浓度的NaOH溶液50毫升和足量的CO2,他们的设计方案是:首先_____,然后_____,加热_____后,再____,最后加热浓缩,冷却结晶,过滤得固体Na2CO3 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com